解题方法
1 . 研究化学反应中的能量变化,有助于帮助我们更好地利用化学反应为生产和生活服务。
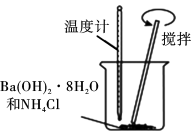
(1)某同学设计如图所示的实验探究化学反应中的能量变化。实验中发现反应后温度降低,该反应中反应物的总能量_______ (填“高于”、“等于”或“低于”)生成物的总能量。
(2)从断键和成键的角度分析反应 中能量的变化。断开1mol化学键需要的能量如表所示,则该反应生成
中能量的变化。断开1mol化学键需要的能量如表所示,则该反应生成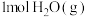
_______ (填“吸收”或“释放”)的能量为_______ kJ。
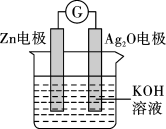
(3)利用Fe和 溶液的反应设计原电池,则正极材料为
溶液的反应设计原电池,则正极材料为_______ ,负极材料为_______ 。
(4)银锌电池是一种常见的化学电源,反应原理为: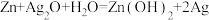 ,其工作示意图如图所示。在装置中
,其工作示意图如图所示。在装置中 作
作_______ (填“正”或“负”)极,溶液中的 向
向_______ (填“Zn”或“ ”)电极移动;负极的电极反应式为
”)电极移动;负极的电极反应式为_______ 。
(1)某同学设计如图所示的实验探究化学反应中的能量变化。实验中发现反应后温度降低,该反应中反应物的总能量

(2)从断键和成键的角度分析反应
 中能量的变化。断开1mol化学键需要的能量如表所示,则该反应生成
中能量的变化。断开1mol化学键需要的能量如表所示,则该反应生成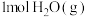
| 化学键 | H-H | O=O | H-O |
键能 | 436 | 496 | 463 |
(3)利用Fe和
 溶液的反应设计原电池,则正极材料为
溶液的反应设计原电池,则正极材料为(4)银锌电池是一种常见的化学电源,反应原理为:
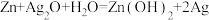 ,其工作示意图如图所示。在装置中
,其工作示意图如图所示。在装置中 作
作 向
向 ”)电极移动;负极的电极反应式为
”)电极移动;负极的电极反应式为
您最近一年使用:0次
21-22高一·全国·假期作业
2 . 已知铅蓄电池放电过程的总反应为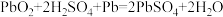 。下列关于铅蓄电池的说法正确的是
。下列关于铅蓄电池的说法正确的是
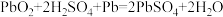 。下列关于铅蓄电池的说法正确的是
。下列关于铅蓄电池的说法正确的是| A.Pb为正极,PbO2为负极 |
B.正极的电极反应式为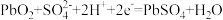 |
| C.硫酸溶液中,H+移向负极 |
D.放电一段时间后, 浓度减小 浓度减小 |
您最近一年使用:0次
3 . 如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细。由此判断下列M、N、P物质可以成立的是
| A.M为Mg,N为Al,P为NaOH溶液 |
| B.M为Cu,N为Fe,P为稀盐酸 |
C.M为Zn,N为C(石墨),P为 溶液 溶液 |
D.M为Ag,N为Zn,P为 溶液 溶液 |
您最近一年使用:0次
2022-07-20更新
|
863次组卷
|
4卷引用:陕西省渭南市白水县2021~2022学年高一下学期期末质量检测化学试题
陕西省渭南市白水县2021~2022学年高一下学期期末质量检测化学试题(已下线)化学(人教版2019A卷)-学易金卷:2022-2023学年高一下学期期中考前必刷卷第六章 化学反应与能量(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)云南省红河哈尼族彝族自治州第一中学2022-2023学年高一下学期5月期中化学试题
解题方法
4 . 电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息完成下列各题。
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一 组插入烧碱溶液中,分别构成了原电池,在这两个原电池中,负极分别为_______ (填字母)。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(2)铅蓄电池在放电时发生的反应方程式为Pb+PbO2+2H2SO4=2PbSO4 +2H2O正极的电极反应式为_______ 。
(3)FeCl3溶液常用于腐蚀印刷电路铜板,反应原理为2FeCl3 +Cu=2FeCl2 +CuCl2,若将此反应设计成原电池,则负极所用电极材料为_______ ,当电路中转移0.2 mol电子时,被腐蚀的铜的质量为_______ g。
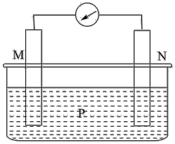
(4)燃料电池是一种高效、环境友好的供电装置。如图是电解质为稀硫酸的氢氧燃料电池原理示意图。
①正极的电极反应式为_______ 。
②电池工作一段时间后硫酸溶液的浓度_______ (填“增大”、“减小”或“不变”)。
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一 组插入烧碱溶液中,分别构成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(2)铅蓄电池在放电时发生的反应方程式为Pb+PbO2+2H2SO4=2PbSO4 +2H2O正极的电极反应式为
(3)FeCl3溶液常用于腐蚀印刷电路铜板,反应原理为2FeCl3 +Cu=2FeCl2 +CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(4)燃料电池是一种高效、环境友好的供电装置。如图是电解质为稀硫酸的氢氧燃料电池原理示意图。

①正极的电极反应式为
②电池工作一段时间后硫酸溶液的浓度
您最近一年使用:0次
名校
解题方法
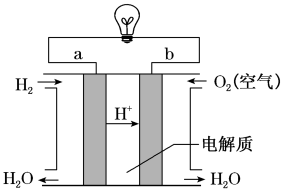
5 . 如图是某化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是

| A.锌片为负极,发生氧化反应 |
| B.该装置可将电能转化成化学能 |
| C.电子由铜片通过导线流向锌片 |
| D.铜片为正极,其附近的溶液变蓝,溶液中有Cu2+产生 |
您最近一年使用:0次
名校
解题方法
6 . 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是


A.Zn为正极,电极反应式为: |
B.电池工作时 向Cu电极移动 向Cu电极移动 |
| C.电子由Zn电极经稀硫酸溶液流向Cu电极 |
D.Zn电极质量每减少65g,则在该电极产生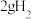 |
您最近一年使用:0次
2022-07-15更新
|
127次组卷
|
2卷引用:陕西省西安市第八十五中学2022-2023学年高一下学期期中考试化学试题
名校
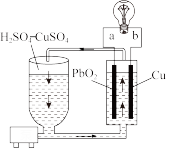
7 . 流动电池是一种新型电池,其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。某种流动电池装置如图所示,电池总反应为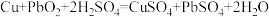 。下列说法不正确的是
。下列说法不正确的是
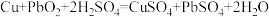 。下列说法不正确的是
。下列说法不正确的是
| A.a为正极,b为负极 |
B.该电池工作时 电极附近溶液的pH增大 电极附近溶液的pH增大 |
C.b极的电极反应为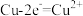 |
| D.电流由b极流出,经导线流向a极 |
您最近一年使用:0次
2022-07-13更新
|
177次组卷
|
2卷引用:陕西省汉中市6校联考2021-2022学年高一下学期期末考试化学试题
解题方法
8 . 将 转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入
转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入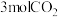 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。
的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。
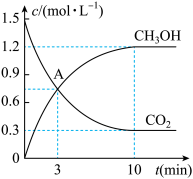
(1)在前 内,以
内,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是_______ 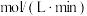 ;能加快此反应速率的措施有
;能加快此反应速率的措施有_______ (任一个措施)。
(2)a=_______ ;A点的正反应速率_______ (填“>”、“<”或“=”)逆反应速率。
(3)平衡时, 的浓度为
的浓度为_______  ;体系的压强与始反应的压强之比为
;体系的压强与始反应的压强之比为_______ 。
(4) 可以作燃料电池的燃料。
可以作燃料电池的燃料。 燃料电池是目前开发最成功的燃料电池之。
燃料电池是目前开发最成功的燃料电池之。 燃料电池由
燃料电池由 、空气(氧气)、
、空气(氧气)、 (电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
(电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
 转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入
转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入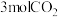 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。
的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。| 时间 | 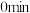 |  |  |  | 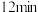 |
 | 3 | 1.5 | 09 | a | 0.6 |
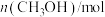 | 0 | 1.5 | 2.1 | 2.4 | 2.4 |

(1)在前
 内,以
内,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是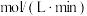 ;能加快此反应速率的措施有
;能加快此反应速率的措施有(2)a=
(3)平衡时,
 的浓度为
的浓度为 ;体系的压强与始反应的压强之比为
;体系的压强与始反应的压强之比为(4)
 可以作燃料电池的燃料。
可以作燃料电池的燃料。 燃料电池是目前开发最成功的燃料电池之。
燃料电池是目前开发最成功的燃料电池之。 燃料电池由
燃料电池由 、空气(氧气)、
、空气(氧气)、 (电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
(电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
| A.电池放电时,通入空气的电极为正极 |
B.电池放电时,每消耗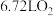 时转移 时转移 电子 电子 |
| C.电池放电时,电解质溶液的碱性逐渐减弱 |
D.负极的电极反应式为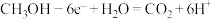 |
您最近一年使用:0次
名校
解题方法
9 . 电池在通讯、交通及日常生活中有着广泛的应用。被称之为“软电池”的纸质电池,采用一个薄层纸片(在其一边镀锌,而在其另一边镀二氧化锰)作为传导体。在纸内的离子“流过”水和氧化锌组成的碱性电解液。电池总反应为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.Zn电极反应为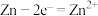 |
B. 为正板,发生氧化反应 为正板,发生氧化反应 |
| C.当6.5g负极材料完全溶解时,转移0.2mol电子 |
| D.电池工作时,电能转化为化学能 |
您最近一年使用:0次
2022-07-12更新
|
146次组卷
|
3卷引用:陕西省西安市周至县第四中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
10 . 我国科学家最新开发基于四电子反应的可快充Zn-Se(硒)电池,工作原理如图所示(aq代表水溶液,Se@C代表以石墨烯为载体的吸附硒)。下列说法错误的是


| A.Zn极为负极 |
| B.电子流向:Zn极→用电器→Se@C极 |
C.正极上的电极反应式为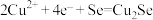 |
D.每生成0.1mol 时,理论上负极质量净减6.5g 时,理论上负极质量净减6.5g |
您最近一年使用:0次
2022-07-11更新
|
242次组卷
|
4卷引用:陕西省商洛市2021-2022学年高一下学期期末教学质量检测化学试题



