名校
解题方法
1 . I.在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol−1表示。
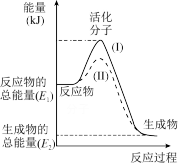
请认真观察如图,然后回答问题。
(1)下列变化中满足如图图示的是___________ (填选项字母);
A.镁和稀盐酸的反应
B.Ba(OH)2•8H2O与NH4Cl的反应
C.NaOH固体加入水中
D.乙醇燃烧
Ⅱ.人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___________ (填选项字母);
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为___________ g;
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
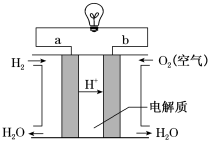
①氢氧燃料电池的正极反应化学方程式是:___________ ;
②电池工作一段时间后硫酸溶液的pH___________ (填“增大”“减小”或“不变”)。

请认真观察如图,然后回答问题。
(1)下列变化中满足如图图示的是
A.镁和稀盐酸的反应
B.Ba(OH)2•8H2O与NH4Cl的反应
C.NaOH固体加入水中
D.乙醇燃烧
Ⅱ.人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的正极反应化学方程式是:
②电池工作一段时间后硫酸溶液的pH
您最近一年使用:0次
名校
2 . 如下图所示的原电池:当电解质溶液为稀H2SO4时,回答下列问题:

(1)Zn电极是_______ 极(填“正”或“负”)极
(2)负极反应为_______ (填“氧化”或“还原”),电极反应式_______ 。
(3)电子移动方向_______ ,溶液中氢离子向_______ (填“正”或“负”)极移动。

(1)Zn电极是
(2)负极反应为
(3)电子移动方向
您最近一年使用:0次
名校
解题方法
3 . 将锌片和铜片用导线相连,插入某种电解质溶液形成原电池装置。
(1)若电解质溶液是稀硫酸,发生氧化反应的是_______ 极(填“锌”或“铜”),铜极上的实验现象是:_______ ,该电池的总电极反应式是_______ 。
(2)若电解质溶液是硫酸铜溶液,在导线中电子是由_______ 极流向_______ 极,铜极上发生的电极反应式是_______ ,锌极的实验现象是_______ ,电解质溶液里的实验现象是_______ 。
(1)若电解质溶液是稀硫酸,发生氧化反应的是
(2)若电解质溶液是硫酸铜溶液,在导线中电子是由
您最近一年使用:0次
4 . 在甲、乙、丙三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:

(1)甲中反应的离子方程式为______ 。
(2)乙中Sn极的电极反应式为______ ,Sn极附近溶液的pH______ (填“增大”“减小”或“不变”)。
(3)丙中被腐蚀的金属是______ ,总反应式为______ (写离子方程式)。

(1)甲中反应的离子方程式为
(2)乙中Sn极的电极反应式为
(3)丙中被腐蚀的金属是
您最近一年使用:0次
2021-04-01更新
|
242次组卷
|
3卷引用:甘肃省天水市田家炳中学2020-2021学年高一下学期期末考试化学试题
5 . 在银锌原电池中,以硫酸铜为电解质溶液:
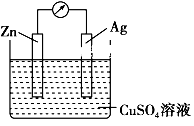
锌为_______ 极,电极上发生的是_______ 反应(“氧化”或“还原”)电极反应式为_______ ;银电极电极反应式是_______ ;银片上观察到的现象是_______ 。

锌为
您最近一年使用:0次
20-21高一下·全国·课时练习
解题方法
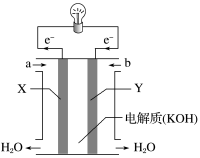
6 . (1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从________ 口通入(填“a”或“b”),X极为电池的______ (填“正”或“负”)极。
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的______ 极;电子从该极________ (填“流入”或“流出”)。
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是_______ 极,Ag2O发生________ 反应。
②电子由_____ 极流向_____ 极(填“Zn”或“Ag2O”),当电路通过1 mol电子时,负极消耗物质的质量是________ g。
③在使用过程中,电解质溶液中KOH的物质的量_____ (填“增大”“减小”或“不变”)。

(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是
②电子由
③在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
2021-03-10更新
|
2334次组卷
|
3卷引用:6.1.3 原电池原理的应用与化学电源(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
(已下线)6.1.3 原电池原理的应用与化学电源(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)(已下线)期中检测卷1 -2020-2021学年高一化学必修2章末集训必刷卷(人教版)(已下线)第12讲 化学电池(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
名校
解题方法
7 . 如图所示,组成一个原电池。

(1)当电解质溶液为稀硫酸时:
①Zn电极是______ (填“正”或“负”)极,其电极反应为______ 。
②Cu电极是______ 极,其电极反应为______ 。
(2)由铜、铁和稀硫酸组成的原电池中,铁是______ 极,电极反应式是______ ;原电池总反应方程式是_____ 。(写离子方程式)。

(1)当电解质溶液为稀硫酸时:
①Zn电极是
②Cu电极是
(2)由铜、铁和稀硫酸组成的原电池中,铁是
您最近一年使用:0次
2021-03-05更新
|
362次组卷
|
2卷引用:河北省张家口市宣化第一中学2020-2021学年高一下学期期中考试化学试题
8 . 观察如图A、B、C三个装置,回答下列问题:
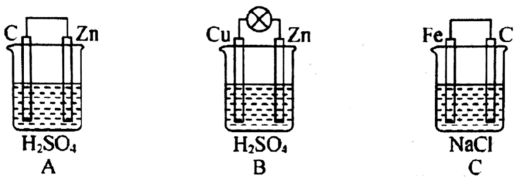
(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一碳棒,可观察到碳棒上__ (填“有”或“没有”)气泡产生。用导线把锌片和碳棒连接起来组成一个原电池(图A),正极的反应式为___ 。
(2)如果烧杯中最初装入的是500 mL2 mol•L-1硫酸溶液,构成铜锌原电池(图B,假设产生的气体没有损失),当收集到11.2 L(标准状况下)H2时,溶液体积变化忽略不计,则烧杯内溶液中溶质及其物质的量浓度为______ 。
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图C),放置数天后,铁片生锈。负极反应式为__ 。
(4)将铜粉末用10%H2O2和3.0 mol•L-1的H2SO4混合溶液处理,测得不同温度下铜的平均溶解速率如表:
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是___ 。

(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一碳棒,可观察到碳棒上
(2)如果烧杯中最初装入的是500 mL2 mol•L-1硫酸溶液,构成铜锌原电池(图B,假设产生的气体没有损失),当收集到11.2 L(标准状况下)H2时,溶液体积变化忽略不计,则烧杯内溶液中溶质及其物质的量浓度为
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图C),放置数天后,铁片生锈。负极反应式为
(4)将铜粉末用10%H2O2和3.0 mol•L-1的H2SO4混合溶液处理,测得不同温度下铜的平均溶解速率如表:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率/(×10-3 mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是
您最近一年使用:0次
解题方法
9 . 燃料电池在日常生活和科学研究中越来越得到广泛使用。镁-空气燃料电池是一种新型的燃料电池,可应用于电动汽车,其工作原理如图所示:
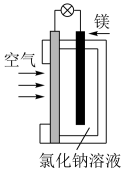
回答下列问题:
(1)通入空气的电极是______ (填“正”或“负”)极。
(2)镁电极发生______ (填“氧化”或“还原”)反应。
(3)电池总反应方程式为______ 。

回答下列问题:
(1)通入空气的电极是
(2)镁电极发生
(3)电池总反应方程式为
您最近一年使用:0次
名校
10 . 利用生活中常见的物品,也可以自己动手设计一个原电池。假设你按照以下原理设置一个原电池,请填写下列空白:
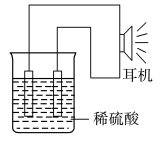
(1)实验原理:Fe+2H+=Fe2++H2↑。
(2)实验仪器:电极(铁钉、____ )、_____ 、_____ 、稀硫酸、耳机。
(3)原电池设计及注意的问题:
①若按如图所示连接好实验仪器,注意听耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触在耳机插头上慢慢挪动,这时可以听见耳机发出“嚓嚓嚓……”的声音。其原因是:在原电池中,由化学能转化为________ ,在耳机中又转化为声音这种能量。
②装置中铁钉应该是原电池的_____ 极,电极反应式是_______ ,发生了______ 反应。
③由所学原电池知识可知,溶液中的________ 离子移向铁钉电极(填写具体离子)。

(1)实验原理:Fe+2H+=Fe2++H2↑。
(2)实验仪器:电极(铁钉、
(3)原电池设计及注意的问题:
①若按如图所示连接好实验仪器,注意听耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触在耳机插头上慢慢挪动,这时可以听见耳机发出“嚓嚓嚓……”的声音。其原因是:在原电池中,由化学能转化为
②装置中铁钉应该是原电池的
③由所学原电池知识可知,溶液中的
您最近一年使用:0次



