解题方法
1 . 分别按如图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中Ⓐ为电流表。请回答下列问题:
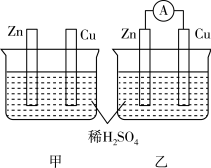
(1)以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)某同学依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示:
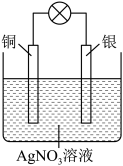
①正极的材料是_______ ,负极发生的电极反应式为:_______ 。
②外电路中的电子流向是:_______ 。
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是_______ 。
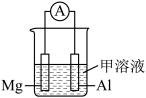
(3)Mg、Al设计成如图所示原电池装置:若电解液为盐酸,正极的电极反应式为:_______ 。若电解液为氢氧化钠溶液,负极的电极材料为_______ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)某同学依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示:

①正极的材料是
②外电路中的电子流向是:
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是
(3)Mg、Al设计成如图所示原电池装置:若电解液为盐酸,正极的电极反应式为:

您最近一年使用:0次
解题方法
2 . 已知可逆反应: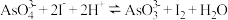 据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路)。进行如下操作:
据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路)。进行如下操作:
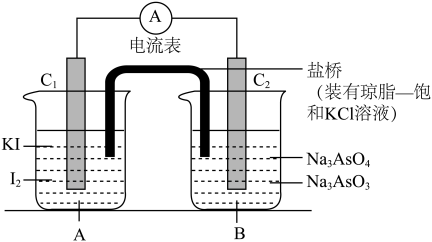
a.向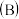 烧杯中逐滴加入浓盐酸,发现微安表指针偏转;
烧杯中逐滴加入浓盐酸,发现微安表指针偏转;
b.若改向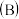 烧杯中滴加
烧杯中滴加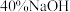 溶液,发现微安表指针向前述相反方向偏转。
溶液,发现微安表指针向前述相反方向偏转。
试回答下列问题:
(1)两次操作过程中微安表指针为什么会发生偏转?_______
(2)两次操作过程中指针偏转方向为什么相反?_______
(3)a操作过程中,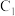 棒发生的反应为
棒发生的反应为_______
(4)b操作过程中,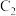 棒发生的反应为
棒发生的反应为_______
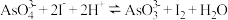 据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路)。进行如下操作:
据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路)。进行如下操作:
a.向
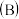 烧杯中逐滴加入浓盐酸,发现微安表指针偏转;
烧杯中逐滴加入浓盐酸,发现微安表指针偏转;b.若改向
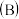 烧杯中滴加
烧杯中滴加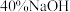 溶液,发现微安表指针向前述相反方向偏转。
溶液,发现微安表指针向前述相反方向偏转。试回答下列问题:
(1)两次操作过程中微安表指针为什么会发生偏转?
(2)两次操作过程中指针偏转方向为什么相反?
(3)a操作过程中,
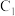 棒发生的反应为
棒发生的反应为(4)b操作过程中,
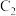 棒发生的反应为
棒发生的反应为
您最近一年使用:0次
解题方法
3 . 一种简单的原电池装置示意图如图所示。请据图回答下列问题。
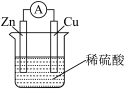
(1)锌是该电池的____ (填“正”或“负”)极。
(2)装置中锌的作用是____ ,稀硫酸的作用是____ 。
A.电极材料 B.电极反应物 C.电子导体 D.离子导体
(3)从化学的角度分析,该装置能产生电流的原因是____ 。

(1)锌是该电池的
(2)装置中锌的作用是
A.电极材料 B.电极反应物 C.电子导体 D.离子导体
(3)从化学的角度分析,该装置能产生电流的原因是
您最近一年使用:0次
解题方法
4 . 氢气是未来最理想的能源;科学家最近研制出利用太阳能产生激光,并在二氧化光钛( )表面作用使海水分解得到复气的新技术:
)表面作用使海水分解得到复气的新技术: 。制得的氢气可用于燃料电池。试回答下列问题:
。制得的氢气可用于燃料电池。试回答下列问题:
(1)分解海水时,_______ 能转变为_______ 能,二氧化钛作_______ 。水分解时,断裂的化学键为_______ 键,分解海水的反应属于_______ 反应(填“放热”或“吸热”)。
(2)火箭推进器中盛有强还原剂液态肼( )和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。
)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。
①反应的热化学方程式为_______ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是_______ 。
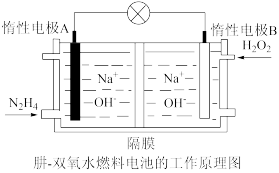
(3)肼-双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。则电池负极反应式为_______ 。
 )表面作用使海水分解得到复气的新技术:
)表面作用使海水分解得到复气的新技术: 。制得的氢气可用于燃料电池。试回答下列问题:
。制得的氢气可用于燃料电池。试回答下列问题:(1)分解海水时,
(2)火箭推进器中盛有强还原剂液态肼(
 )和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。
)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。①反应的热化学方程式为
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
(3)肼-双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。则电池负极反应式为

您最近一年使用:0次
解题方法
5 . 某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,得到的实验数据如下表所示:
(1)水果电池中,水果的作用是_______ 。
(2)能表明电极间距离对电流大小有影响的实验编号是_______ 和_______ ,电极间距离越_______ ,电流越大。
(3)请你再提出一个可能影响水果电池电流大小的因素_______ 。
(4)下图是番茄水果电池,电池工作时,将_______ 转化成_______ ,负极电极材料是_______ ,电极反应式为_______ 。
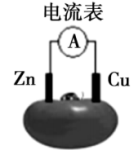
| 实验编号 | 水果种类 | 电极间距离/cm | 电流/uA |
| 1 | 番茄 | 1 | 98.7 |
| 2 | 番茄 | 2 | 72.5 |
| 3 | 苹果 | 2 | 27.2 |
(2)能表明电极间距离对电流大小有影响的实验编号是
(3)请你再提出一个可能影响水果电池电流大小的因素
(4)下图是番茄水果电池,电池工作时,将

您最近一年使用:0次
名校
6 . 按要求回答问题:
(1)以Fe和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①SO 向
向_______ 极移动(填“正”或“负”)。
②电子流动方向由_______ 极流向_______ 极(填“正”或“负”)。
③若有1mole-流过导线,则理论上正极析出标准状态下的气体_______ L。
④若将稀硫酸换成浓硝酸,一段时间后,正极电极方程式为_______ 。
(2)丙烷(C3H8)燃料电池是一种高效无污染的清洁电池,它用KOH做电解质。则负极反应方程式是_______ 。
(3)一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
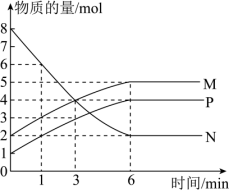
①反应化学方程式中各物质的系数比为a︰b︰c=_______ 。
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为_______ 。
(1)以Fe和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①SO
 向
向②电子流动方向由
③若有1mole-流过导线,则理论上正极析出标准状态下的气体
④若将稀硫酸换成浓硝酸,一段时间后,正极电极方程式为
(2)丙烷(C3H8)燃料电池是一种高效无污染的清洁电池,它用KOH做电解质。则负极反应方程式是
(3)一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a︰b︰c=
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为
您最近一年使用:0次
名校
解题方法
7 . 近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇(CH3OH)是其中的一个研究项目。该研究发生的主要反应如下:
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)上述反应符合原子经济性的是反应___________ (I或II)。
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是___________。
(4)H2还原CO电化学法制备甲醇(CO + 2H2 = CH3OH)的工作原理如图所示:
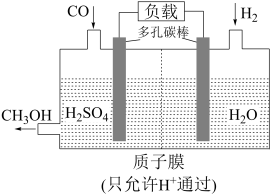
通入H2的一端是电池的___________ 极(填“正”或“负”),电池工作过程中H+通过质子膜向___________ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________ 。
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)(1)上述反应符合原子经济性的是反应
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
| A.恒温恒容下,再充入CO | B.升高温度 |
| C.恒温恒容下,向其中充入Ar | D.恒温恒压下,向其中充入Ar |
| A.单位时间内消耗3molH2,同时生成1mol的CH3OH |
| B.CH3OH的体积分数不再发生变化 |
| C.3v(CO2)=v(H2) |
| D.容器内气体密度不再改变 |

通入H2的一端是电池的
您最近一年使用:0次
2022-03-31更新
|
1312次组卷
|
5卷引用:重庆市主城区六校2020-2021学年高一下学期期末联考化学试题
重庆市主城区六校2020-2021学年高一下学期期末联考化学试题(已下线)【期末复习】必刷题(2)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)安徽省合肥市庐江县2021-2022学年高一下学期期末考试化学试题陕西西安三中2022-2023学年高一下学期第二次月考化学试题江苏省常州市联盟学校2022-2023学年高一下学期期末考试化学试题
名校
解题方法
8 . 填空。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O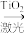 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为_______ 能;分解海水的反应属于_____ 反应(填“放热”或“吸热”)
(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式_______ 。
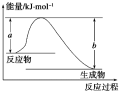
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=_______ kJ∙mol−1,x=________ 。
(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O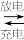 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为_____ 。
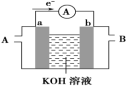
(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为______ 。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
| A.氢气分子内每个氢原子都达到稳定结构 |
| B.氢气分子的能量比两个氢原子的能量低 |
| C.1molH2离解成2molH要放出437.6kJ热量 |
| D.氢原子比氢气分子稳定 |
 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=

(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为

您最近一年使用:0次
名校
解题方法
9 . 根据化学能转化电能的相关知识,回答下列问题:
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_______ ,发生_______ 反应,电解质溶液是_______ 。
(2)正极上出现的现象是___________________ 。
(3)若导线上转移电子1 mol,则生成银___________________ g。
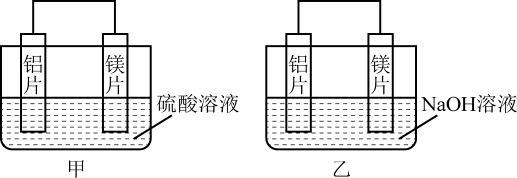
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
(4)写出甲中正极的电极反应式:___________________ 。
(5)乙中负极为___________________ ,总反应的离子方程式:___________________ 。
(6)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有___________________。
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子1 mol,则生成银
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。

(4)写出甲中正极的电极反应式:
(5)乙中负极为
(6)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有___________________。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析 |
您最近一年使用:0次
2022-01-07更新
|
92次组卷
|
3卷引用:湖北省黄石市有色一中2020-2021学年高一下学期期末考试化学试题
名校
10 . 一定温度下,在体积为0.5L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:

(1)曲线___ (填“X”或“Y”)表示N2O4的物质的量随时间的变化曲线。
(2)在0~3min内,用NO2表示的反应速率为___ 。
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1mol N2O4(g)的能量___ (填“高”或“低”)。
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)___ (填“增大”“减小”或“不变”,下同),v(逆)___ 。
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生___ (填“氧化”或“还原”)反应,Pt电极是电池___ (填“正极”或“负极”)。

 N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(1)曲线
(2)在0~3min内,用NO2表示的反应速率为
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1mol N2O4(g)的能量
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生

您最近一年使用:0次
2021-10-10更新
|
328次组卷
|
2卷引用:广东省茂名高州市2020-2021学年高一下学期期末考试化学试题



