1 . 根据如图所示的装置,完成下列各空。
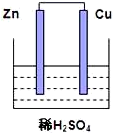
(1)该装置中的总反应式为___________ 。
(2)溶液中的H+移向___________ (填“Cu片”或“Zn片”)
(3)Zn电极的反应式为___________ ,发生 ___________ 反应,(填“氧化”或“还原”)
(4)Cu片为原电池的___________ 极(填“正”或“负”),现象为___________ 。

(1)该装置中的总反应式为
(2)溶液中的H+移向
(3)Zn电极的反应式为
(4)Cu片为原电池的
您最近一年使用:0次
2 . (1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从__ 口通入(填“a”或“b”),X极为电池的___ (填“正”或“负”)极。
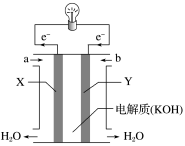
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的___ 极;电子从该极__ (填“流入”或“流出”)。电池总反应为:___ 。

(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
您最近一年使用:0次
解题方法
3 . 如图所示的原电池:当电解质溶液为稀H2SO4时,回答下列问题:
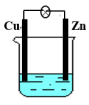
(1)Zn电极是___________ (填“正”或“负”)极,其电极反应为___________ ,该反应是___________ (填“氧化”或“还原”,下同)反应;
(2)Cu电极是___________ 极,其电极反应为___________ ,该反应是___________ 反应。
(3)装置中锌的作用是___________ ,稀硫酸的作用是___________
A.电极材料 B.电极反应物
C.电子导体 D.离子导体

(1)Zn电极是
(2)Cu电极是
(3)装置中锌的作用是
A.电极材料 B.电极反应物
C.电子导体 D.离子导体
您最近一年使用:0次
名校
解题方法
4 . (1)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a、b相连,a为正极;c、d相连,c为负极;a、c相连,c上产生气泡;b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:___________ 。
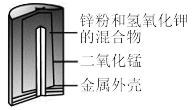
(2)碱性锌锰干电池比普通锌锰电池的使用寿命长且性能高,其构造如图所示,电池反应为: ,其中
,其中 作
作___________ 极,发生___________ 反应,电极反应式为___________ 。
(3)甲烷燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:
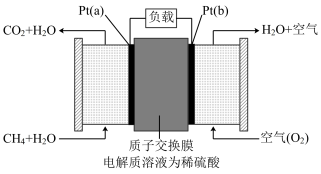
①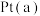 电极是电池的
电极是电池的___________ 极,电极反应式为___________ 。
②电解质溶液中的 向
向___________ (填“a”或“b”)极移动,电子流入的电极是___________ (填“a”或“b”)极。
③该电池工作时消耗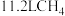 (标准状况下),则电路中通过
(标准状况下),则电路中通过___________ mol电子。
(2)碱性锌锰干电池比普通锌锰电池的使用寿命长且性能高,其构造如图所示,电池反应为:
 ,其中
,其中 作
作
(3)甲烷燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:

①
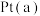 电极是电池的
电极是电池的②电解质溶液中的
 向
向③该电池工作时消耗
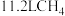 (标准状况下),则电路中通过
(标准状况下),则电路中通过
您最近一年使用:0次
2021-05-31更新
|
1187次组卷
|
8卷引用:河北省临漳县第一中学2020-2021学年高一下学期3月份月考化学试题
河北省临漳县第一中学2020-2021学年高一下学期3月份月考化学试题河北省石家庄一中东校区2020-2021学年高一第二学期教学质量检测(二)化学试题(已下线)作业11 原电池-2021年高二化学暑假作业(人教版2019)(已下线)1.2.1 原电池的工作原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)福建省南安市柳城中学2021-2022学年高二上学期第一次月考化学试题(已下线)4.1.2 化学电源(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)新疆石河子第一中学2021-2022学年高一5月月考化学试题(已下线)第四章 化学反应与电能(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
解题方法
5 . 电能是现代社会应用最广泛的能源之一,某原电池装置如图所示。

其中,Zn电极为原电池的___________ 极(填“正”或“负”),电极反应式是___________ 。Cu电极上发生的反应属于___________ (填“氧化”或“还原”) 反应,当铜表面析出22.4 L氢气(标准状况)时,导线中通过了___________ mol电子。

其中,Zn电极为原电池的
您最近一年使用:0次
解题方法
6 . 化学能在一定条件下可转化为电能。
(1)将锌片放入盛有稀硫酸的烧杯中,反应的化学方程式为_______ 。
(2)将锌片、铜片按照如图所示装置连接,锌片是_______ (填“正极”或“负极”)。能证明化学能转化为电能的实验现象是:_______ 、_______ 。锌片上的电极反应式为_______ 铜片上的电极反应式为_______ 。稀硫酸在如图所示装置中的作用是:传导离子、_______ 。
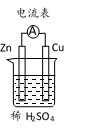
(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是_______ (填序号)。
①2H2+O2 2H2O
2H2O
②Fe+Cu2+=Cu+Fe2+
③CaO+H2O=Ca(OH)2
(1)将锌片放入盛有稀硫酸的烧杯中,反应的化学方程式为
(2)将锌片、铜片按照如图所示装置连接,锌片是

(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①2H2+O2
 2H2O
2H2O②Fe+Cu2+=Cu+Fe2+
③CaO+H2O=Ca(OH)2
您最近一年使用:0次
名校
解题方法
7 . 电池的发展是化学对人类的一项重大贡献。
I.用图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
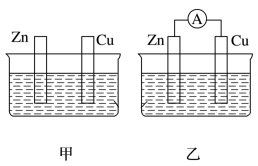
(1)以下叙述中,正确的是___________ (填选项字母)。
a.甲中锌片是负极,乙中铜片是正极
b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的c(H+)均减小
d.乙中电流从铜片经导线流向锌片
e.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的形式主要是:甲为___________ ;乙为___________ 。
(3)乙装置中负极的电极反应式为:___________ ;当乙中产生1.12 L标准状况下气体时,通过导线的电子数为___________ ;若电路导线上通过电子1 mol,则理论上两极的变化是___________ (填选项字母)。
a.锌片减少32.5 g b.锌片增重32.5 g
c.铜片析出1 g H2 d.铜片上析出1 mol H2
(4)为了避免锌片与Cu2+直接接触发生反应而影响原电池的放电效率,人们设计了如图装置。a处装置的名
称为___________ ,在工作时,其内部的阳离子移向___________ (填“正极”或“负极”)。
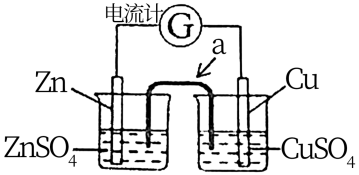
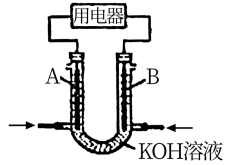
II.将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则___________ (填A或B)处电极入口通CH4,其电极反应式为:___________ 。
I.用图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是
a.甲中锌片是负极,乙中铜片是正极
b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的c(H+)均减小
d.乙中电流从铜片经导线流向锌片
e.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的形式主要是:甲为
(3)乙装置中负极的电极反应式为:
a.锌片减少32.5 g b.锌片增重32.5 g
c.铜片析出1 g H2 d.铜片上析出1 mol H2
(4)为了避免锌片与Cu2+直接接触发生反应而影响原电池的放电效率,人们设计了如图装置。a处装置的名
称为

II.将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则

您最近一年使用:0次
名校
8 . 图为某同学设计的原电池装置

(1)当电解质溶液为稀硫酸时:①Fe电极是__ (填“正”或“负”)极,其电极反应为__
②Cu电极的电极反应为_____ ,该电极发生______ 反应(填“氧化”或“还原”)反应。原电池工作一段时间后,铁片的质量减少了2.8克,铜片表面产生气体____ L(标准状况下),导线中通过_____ mol电子。
(2)当电解质溶液为浓硫酸时:①Fe电极是______ 极,其电极反应为____ ,
②Cu电极是_____ 极,其电极反应为_______

(1)当电解质溶液为稀硫酸时:①Fe电极是
②Cu电极的电极反应为
(2)当电解质溶液为浓硫酸时:①Fe电极是
②Cu电极是
您最近一年使用:0次
解题方法
9 . 铜、银和硝酸银溶液组成原电池,回答下列问题:
(1)负极反应式是_______ 。
(2)正极反应式是_______ 。
(3)当有1.6g铜溶解时,银棒增重_______ g。
(1)负极反应式是
(2)正极反应式是
(3)当有1.6g铜溶解时,银棒增重
您最近一年使用:0次
解题方法
10 . 氮是动植物生长不可缺少的元素,氨的制备及应用对农业生产及国防建设均有重大意义,反应如下:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)合成氨的反应中的能量变化如图所示。
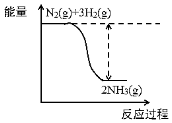
该反应是___ 反应(填“吸热”或“放热”),该热效应来源于反应过程中断裂旧化学键并形成新化学键时的能量变化。已知:断裂1molN≡N键需吸945.6kJ能量,断裂1molH—H键需吸收436kJ能量,形成1molH—N键可放出391kJ能量。试写出NH3的电子式___ ,若生成2molNH3(g),放出___ kJ热量。
(2)一种用于潜艇的液氨—液氧燃料电池原理示意图如图所示。
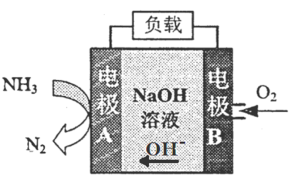
①电极A上,氮元素的化合价___ (填“升高”或“降低”),电极A是___ 极(填“正”或“负”)。
②电极B上发生的电极反应为___ 。
a.O2+H2O+2e-=4OH-
b.O2+2H2O+4e-=4OH-
c.O2+4H++4e-=2H2O
 2NH3(g)。
2NH3(g)。(1)合成氨的反应中的能量变化如图所示。

该反应是
(2)一种用于潜艇的液氨—液氧燃料电池原理示意图如图所示。

①电极A上,氮元素的化合价
②电极B上发生的电极反应为
a.O2+H2O+2e-=4OH-
b.O2+2H2O+4e-=4OH-
c.O2+4H++4e-=2H2O
您最近一年使用:0次



