名校
解题方法
1 . 某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同___________ (填“相同”或“不相同”)。
(2)实验3中铝为___________ 极,电极反应式为___________ ;石墨为___________ 极,电极反应式为___________ ;电池总反应为(离子方程式)___________ 。
(3)实验4中铝为___________ 极,原因是___________ ;写出铝电极的电极反应式:___________ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)实验1、2中Al电极的作用是否相同
(2)实验3中铝为
(3)实验4中铝为
您最近一年使用:0次
2021-06-29更新
|
252次组卷
|
3卷引用:天津市河北区2020-2021学年高一下学期期末考试化学试题
天津市河北区2020-2021学年高一下学期期末考试化学试题(已下线)重难点03 原电池的工作原理与相关判断-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)四川省达州市渠县中学2018-2019学年高二下学期化期中考试化学试题
名校
解题方法
2 . 在一定条件下,化学能与电能可以相互转化。
(1)二甲醚燃料电池工作原理如图所示
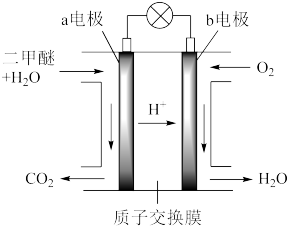
①电极a为电池的_____ (填“正”或“负”)极。
②电极b的电极反应式:_____ 。
③标准状况下,消耗11.2LO2时,转移的电子数为____ mol。
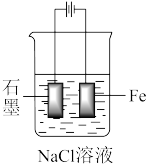
(2)①下图装置中石墨上发生_____ 反应,电极反应式为____ 。
②装置中Fe片____ (填“不易”或“容易”)被腐蚀,电极反应式为____ 。
③一段时间后,烧杯中的溶液的pH将____ (填“变大”、“变小”或“不变”)。
(1)二甲醚燃料电池工作原理如图所示

①电极a为电池的
②电极b的电极反应式:
③标准状况下,消耗11.2LO2时,转移的电子数为
(2)①下图装置中石墨上发生
②装置中Fe片
③一段时间后,烧杯中的溶液的pH将

您最近一年使用:0次
3 . I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。

(1)①该反应的化学方程式是___ 。
②在t1min时,该反应达到了___ 状态,下列可作为判断反应已达到该状态的是__ 。
A.X、Y、Z的反应速率相等 C.生成3molY的同时生成1molZ
B.X、Y的反应速率比为2∶3 D.生成1molZ的同时生成2molX
(2)若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则至t1min时,该反应吸收的热量为___ 。
II.如图所示,组成一个原电池。

(1)当电解质溶液为稀硫酸时。Fe电极是___ (填“正”或“负”)极,其Cu电极反应式为___ ,该反应是___ (填“氧化”或“还原”)反应。
(2)当电解质溶液为浓硝酸时。Cu电极是___ 极(填“正”或“负”),其电极反应式为___ ,该反应是___ (填“氧化”或“还原”)反应。

(1)①该反应的化学方程式是
②在t1min时,该反应达到了
A.X、Y、Z的反应速率相等 C.生成3molY的同时生成1molZ
B.X、Y的反应速率比为2∶3 D.生成1molZ的同时生成2molX
(2)若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则至t1min时,该反应吸收的热量为
II.如图所示,组成一个原电池。

(1)当电解质溶液为稀硫酸时。Fe电极是
(2)当电解质溶液为浓硝酸时。Cu电极是
您最近一年使用:0次
名校
解题方法
4 . I.实验室以K2MnO4为原料,用两种方法制备高锰酸钾。已知:K2MnO4在浓强碱溶液中可稳定存在,溶液呈墨绿色,当溶液碱性减弱时易发生反应:3 +2H2O=2
+2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。
(1)CO2法。实验装置如图。
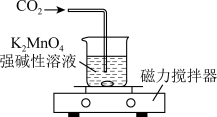
①反应一段时间后,用玻璃棒蘸取溶液滴在滤纸上,仅有紫红色而没有绿色痕迹,由此可知___ 。
②停止通入CO2,过滤除去___ (填化学式,下同),将滤液蒸发浓缩、冷却结晶,抽滤得到KMnO4粗品。若CO2通入过多,产品中可能混有的杂质是___ 。
(2)电解法。实验装置如图。
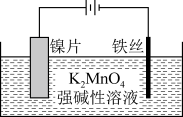
①阳极的电极反应式为___ ,阴极产生的气体为___ (填化学式)。
②与CO2法相比,电解法的主要优点是___ (写一条)。,
(3)如用氨燃料电池电解溶液,已知氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O2 2N2+6H2O。则其负极反应式为
2N2+6H2O。则其负极反应式为___ 。
II.(4)若用钢铁(含Fe、C)制品盛装NaClO溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化学腐蚀过程中的正极反应式为___ 。
(5)铁器深埋地下,也会发生严重的电化学腐蚀,原因是一种称为硫酸盐还原菌的细菌,能提供正极反应的催化剂,将土壤中的 还原为S2-,试写出该电化学腐蚀的正极反应式
还原为S2-,试写出该电化学腐蚀的正极反应式___ 。
 +2H2O=2
+2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。(1)CO2法。实验装置如图。

①反应一段时间后,用玻璃棒蘸取溶液滴在滤纸上,仅有紫红色而没有绿色痕迹,由此可知
②停止通入CO2,过滤除去
(2)电解法。实验装置如图。

①阳极的电极反应式为
②与CO2法相比,电解法的主要优点是
(3)如用氨燃料电池电解溶液,已知氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O2
 2N2+6H2O。则其负极反应式为
2N2+6H2O。则其负极反应式为II.(4)若用钢铁(含Fe、C)制品盛装NaClO溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化学腐蚀过程中的正极反应式为
(5)铁器深埋地下,也会发生严重的电化学腐蚀,原因是一种称为硫酸盐还原菌的细菌,能提供正极反应的催化剂,将土壤中的
 还原为S2-,试写出该电化学腐蚀的正极反应式
还原为S2-,试写出该电化学腐蚀的正极反应式
您最近一年使用:0次
解题方法
5 . 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

(1)电极X的材料是_______ ;电解质溶液Y是_______ ;
(2)银电极为电池的_______ 极,发生的电极反应式为_______ ;X电极上发生的电极反应为_______ 反应;(填“氧化”或“还原”)
(3)外电路中的电子_______ (填“流出”或“流向”)Ag电极。

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子
您最近一年使用:0次
解题方法
6 . 化学能在一定条件下可转化为电能。
(1)锌与稀硫酸发生的氧化还原反应中,得电子的反应物为___________ 。
(2)将锌片、铜片按照如图所示装置连接,锌片是___________ (填“正极”或“负极”)。能证明化学能转化为电能的实验现象是:___________ 、铜片上产生大量气泡。
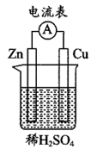
(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
①
②
③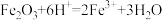
(1)锌与稀硫酸发生的氧化还原反应中,得电子的反应物为
(2)将锌片、铜片按照如图所示装置连接,锌片是

(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①

②

③
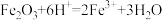
您最近一年使用:0次
7 . 原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计了如图所示装置。
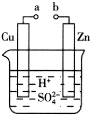
(1)a和b不连接时,烧杯中现象是_______ 。
(2)a和b用导线连接,Cu极为原电池___ (“正”或“负”)极,电极反应式为___ ;溶液中H+移向__ (填“Cu”或“Zn”)极。
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为_____ 。

(1)a和b不连接时,烧杯中现象是
(2)a和b用导线连接,Cu极为原电池
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)_______ (填“相同”或“不相同”)。
(2)对实验3完成下列填空:
①铝电极反应式:_______ 。
②石墨电极反应式:_______ 。
③电池总反应方程式:_______ 。
(3)实验4中铝作_______ ,写出铝电极的电极反应式:_______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)
(2)对实验3完成下列填空:
①铝电极反应式:
②石墨电极反应式:
③电池总反应方程式:
(3)实验4中铝作
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
9 . 将反应2H++Zn=Zn2++H2↑为依据设计一个原电池。
可选:Zn片、Mg片、A1片、石墨棒、稀硫酸、稀硝酸、导线、烧杯、U形管。
(1)画出原电池装置,标明正负极和电核材料,以及电解质溶液,标出电子转移的方向___ 。

(2)写出正极的电极反应式:___ 。
(3)H+离子向___ 极移动,阴离子向__ 极移动。(填“正”或““负”)。
可选:Zn片、Mg片、A1片、石墨棒、稀硫酸、稀硝酸、导线、烧杯、U形管。
(1)画出原电池装置,标明正负极和电核材料,以及电解质溶液,标出电子转移的方向

(2)写出正极的电极反应式:
(3)H+离子向
您最近一年使用:0次
解题方法
10 . 目前汽车上使用的铅蓄电池如图所示,根据图示回答下列问题:

(1)铅蓄电池的负极是___________ ,铅蓄电池的正极是___________ 。
(2)铅蓄电池的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则负极发生___________ (填“氧化”或“还原”)反应,由___________ 生成___________ ;正极发生___________ (填“氧化”或“还原”)反应,由___________ 生成___________ 。
(3)电解质溶液是H2SO4,那么在铅蓄电池中H+向___________ (填“正”或“负”)极移动, 向
向___________ (填“正”或“负”)极移动。

(1)铅蓄电池的负极是
(2)铅蓄电池的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则负极发生
(3)电解质溶液是H2SO4,那么在铅蓄电池中H+向
 向
向
您最近一年使用:0次
2021-06-11更新
|
364次组卷
|
3卷引用:黑龙江省嫩江市第一中学校等五校2020-2021学年高一下学期期中联考化学试题
黑龙江省嫩江市第一中学校等五校2020-2021学年高一下学期期中联考化学试题(已下线)第12讲 化学电池(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题



