解题方法
1 . 分别按如图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中Ⓐ为电流表。请回答下列问题:
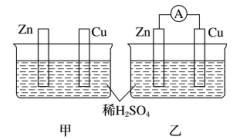
(1)以下叙述中,正确的是___________ (填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为___________ ;乙为___________ 。
(3)某同学依据氧化还原反应: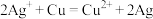 设计的原电池如图所示:
设计的原电池如图所示:
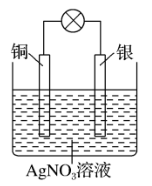
①负极的材料是___________ ,发生的电极反应为___________ ;
②外电路中的电子是从___________ 电极流向___________ 电极。(写出电极材料的名称)
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是___________ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的主要形式:甲为
(3)某同学依据氧化还原反应:
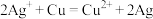 设计的原电池如图所示:
设计的原电池如图所示:
①负极的材料是
②外电路中的电子是从
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是
您最近一年使用:0次
2021-04-26更新
|
429次组卷
|
2卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
名校
解题方法
2 . 一种新型的燃料电池可用于制取乙醛(CH3CHO),总反应式为 ,电池的主要构成要素如图所示,请回答下列问题:
,电池的主要构成要素如图所示,请回答下列问题:
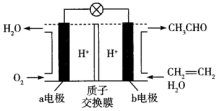
(1)该装置的能量转化形式为_______ 。
(2)a电极为燃料电池的_______ 极,该电极的电极反应式为_______ 。
(3)电池工作时,H+由_______ (填“a电极”或“b电极”,下同)移向_______ 。
(4)生成3.3g乙醛时,需要消耗标准状况下的氧气_______ mL。
 ,电池的主要构成要素如图所示,请回答下列问题:
,电池的主要构成要素如图所示,请回答下列问题:
(1)该装置的能量转化形式为
(2)a电极为燃料电池的
(3)电池工作时,H+由
(4)生成3.3g乙醛时,需要消耗标准状况下的氧气
您最近一年使用:0次
2021-04-24更新
|
241次组卷
|
3卷引用:河南省天一大联考2020-2021学年高一下学期期中考试化学试题
名校
解题方法
3 . 根据化学能转化电能的相关知识,回答下列问题:
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是___________ ,发生___________ (填“氧化”或“还原”)反应,电解质溶液是___________ 。
(2)正极上出现的现象是___________ 。
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。

(1)写出甲中正极的电极反应式:___________ 。
(2)乙中负极为___________ ,总反应的离子方程式:___________ 。
(3)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有___________ 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。

(1)写出甲中正极的电极反应式:
(2)乙中负极为
(3)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
您最近一年使用:0次
名校
解题方法
4 . 燃料电池的能量转化率可高达90%。CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)和惰性电极构成。
(1)其中负极反应式为___ 。
(2)则下列说法正确的是___ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
(1)其中负极反应式为
(2)则下列说法正确的是
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
5 . 如图所示。请回答:
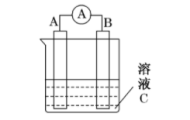
(1)若C为稀H2SO4溶液,电流表指针发生偏转,A极材料为铜,B电极材料为Zn,A为_____ 极,此电池所发生的反应化学方程式为_________ ,反应进行一段时间后溶液C中c(H+)将______ (填“变大”“变小”或“基本不变”)。溶液中的 移向
移向________ 极(填“A”或“B”)
(2)若C为CuSO4溶液,A极材料为石墨,B电极材料为Fe。则B为_____ 极,B极上电极反应属于____ (填“氧化反应”或“还原反应”),B电极上发生的电极反应式为_______ ;A极产生的现象是_______ ;若AB两电极质量都为50.0g且反应过程中有0.2mol的电子发生转移,理论上AB两电极质量差为______ g。

(1)若C为稀H2SO4溶液,电流表指针发生偏转,A极材料为铜,B电极材料为Zn,A为
 移向
移向(2)若C为CuSO4溶液,A极材料为石墨,B电极材料为Fe。则B为
您最近一年使用:0次
20-21高一下·浙江·阶段练习
6 . 能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
①哪一段时间内反应速率最大:___________ min。(填“0~ 1” “1~2”“2~3”“3~4”或“4~ 5”)
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是___________ 。(填字母序号)
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是___________ 反应 (填“放热”或“吸热”)
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称___________ , B 电极反应式:___________ ,该电池在工作时,溶液中Fe3+向___________ (填“A”、“B” )移动,A电极的质量将___________ 。 (填“增加”、“减小”或“不变”)
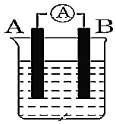
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
| 时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL (标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称

您最近一年使用:0次
解题方法
7 . 利用反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池。回答下列问题:
(1)该电池的负极材料是_______ ,发生_______ 反应(填“氧化”或“还原”);
(2)电解质溶液是_______ ;
(3)正极上出现的现象是_______ ;
(4)在外电路中,电子从_______ 极流向_______ 极。
(5)负极反应式:_______ ;正极反应式:_______ 。
(1)该电池的负极材料是
(2)电解质溶液是
(3)正极上出现的现象是
(4)在外电路中,电子从
(5)负极反应式:
您最近一年使用:0次
名校
解题方法
8 . 下面有四种原电池装置:

回答下面问题:
(1)装置①的负极是___________ (填元素符号,下同),原电池反应的离子方程式为___________ 。
(2)装置②的正极是___________ ,负极发生的电极反应为___________ 。
(3)装置③中有电子流出的电极是___________ ,原电池反应的离子方程式为___________ 。
(4)装置④发生还原反应的电极是___________ ,该极的电极反应为___________ 。

回答下面问题:
(1)装置①的负极是
(2)装置②的正极是
(3)装置③中有电子流出的电极是
(4)装置④发生还原反应的电极是
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
9 . 分别按图甲、乙所示装置进行实验,两个烧杯里的溶液为同浓度的稀硫酸,甲中A为电流表。请回答下列问题:
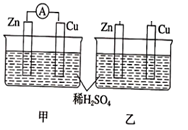
(1)下列叙述正确的是_______ (填字母)。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯溶液中H+浓度均减小 D.甲产生气泡的速率比乙慢
(2)甲装置中的能量转化形式:_______ 能转化为_______ 能,乙转置中的能量转化形式:_______ 能转化为_______ 能;
(3)在甲装置中,若把稀硫酸换成 CuSO4溶液,试写出铜电极的电极反应:_______ 。

(1)下列叙述正确的是
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯溶液中H+浓度均减小 D.甲产生气泡的速率比乙慢
(2)甲装置中的能量转化形式:
(3)在甲装置中,若把稀硫酸换成 CuSO4溶液,试写出铜电极的电极反应:
您最近一年使用:0次
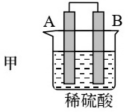
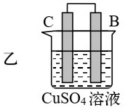
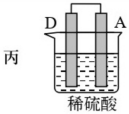
10 . 由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)装置乙溶液中C电极反应:_______ ;外电路中电子由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)装置乙溶液中C电极反应:
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次