湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
湖北
高一
期中
2021-04-27
275次
整体难度:
容易
考查范围:
常见无机物及其应用、化学反应原理、认识化学科学、化学实验基础
湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
湖北
高一
期中
2021-04-27
275次
整体难度:
容易
考查范围:
常见无机物及其应用、化学反应原理、认识化学科学、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 下列关于 的叙述正确的是
的叙述正确的是
 的叙述正确的是
的叙述正确的是A. 是无色、无臭、有毒的气体 是无色、无臭、有毒的气体 |
B. 与NaOH溶液反应生成 与NaOH溶液反应生成 ,说明 ,说明 有酸性氧化物的性质 有酸性氧化物的性质 |
C. 能使紫色的 能使紫色的 溶液褪色,说明 溶液褪色,说明 有漂白性 有漂白性 |
D. 有毒,不能用作食品添加剂 有毒,不能用作食品添加剂 |
您最近一年使用:0次
2021-04-26更新
|
200次组卷
|
3卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
单选题
|
容易(0.94)
解题方法
2. 下列事实与括号中浓硫酸的性质对应关系正确的是
| A.空气中敞口久置的浓硫酸质量增大(挥发性) |
| B.浓硫酸使蓝色胆矾变白(脱水性) |
| C.浓硫酸可用来干燥某些气体(吸水性) |
| D.用浓硫酸在纸上书写的字迹变黑(氧化性) |
您最近一年使用:0次
2021-04-26更新
|
396次组卷
|
2卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
单选题
|
适中(0.65)
3. 下列有关化学反应速率的说法正确的是
| A.对于放热反应,升高温度化学反应速率减小 |
| B.改变压强,化学反应速率必然改变 |
| C.用铁和稀硫酸反应制取氢气时,换成浓硫酸,产生氢气的速率加快 |
| D.Na、Mg、Al的金属性决定了它们与水反应的速率大小 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
4. 下列有关化学反应限度的说法正确的是
| A.可逆反应达到平衡状态时,各反应物、生成物的浓度相等 |
| B.在一定条件下,一个可逆反应达到的平衡状态就是该反应所能达到的最大限度 |
| C.化学反应在一定条件下建立平衡状态时,化学反应将会停止 |
D.1mol 和 和 在一定条件下可完全生成 在一定条件下可完全生成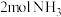 |
您最近一年使用:0次
2021-04-26更新
|
343次组卷
|
3卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
单选题
|
适中(0.65)
5. 下列有关化学反应能量变化的说法正确的是
| A.氢气燃烧,浓硫酸溶于水,都放出热量,这些变化都为放热反应 |
| B.化学反应既有物质变化,又有能量变化 |
| C.镁条在空气中燃烧是放热反应,反应过程中所释放的能量全部转化为热能 |
| D.吸热反应需要加热才能进行,放热反应都不需要加热就可以进行 |
您最近一年使用:0次
单选题
|
适中(0.65)
6. 下列关于原电池的叙述中,正确的是
| A.将铜片和锌片用导线连接插入酒精中,电流表指针发生偏转 |
| B.在铜—锌—稀硫酸原电池中,电子由锌通过导线流向铜,再由铜通过电解质溶液到达锌 |
| C.原电池中阳离子向正极移动 |
| D.原电池中的负极反应一定是电极材料失电子 |
您最近一年使用:0次
单选题
|
适中(0.65)
8. 下列关于氮的固定的叙述中,正确的是
| A.氮的固定中氮元素一定被氧化 |
| B.豆科植物的根瘤菌固氮属于自然固氮中的高能固氮 |
C.工业上将 转化为其他铵态化肥属于人工固氮 转化为其他铵态化肥属于人工固氮 |
D. 和 和 在放电条件下会生成 在放电条件下会生成 属于自然固氮 属于自然固氮 |
您最近一年使用:0次
单选题
|
较易(0.85)
10. 下列关于硅酸盐的叙述中,不正确的是
| A.硅酸盐是由硅、氧和金属组成的混合物 |
| B.硅酸盐结构较为复杂,大多不溶于水,化学性质很稳定 |
| C.硅氧四面体中,硅原子与氧原子都是以共价键结合 |
| D.水泥与玻璃的共同原料是石灰石,水泥与陶瓷的共同原料是黏土 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
11. 下列溶液或用品中:①澄清石灰水;②品红溶液;③酸性 溶液;④溴水;⑤湿润的蓝色石蕊试纸;⑥
溶液;④溴水;⑤湿润的蓝色石蕊试纸;⑥ 溶液;⑦
溶液;⑦ 溶液。不能区别
溶液。不能区别 和
和 气体的是
气体的是
 溶液;④溴水;⑤湿润的蓝色石蕊试纸;⑥
溶液;④溴水;⑤湿润的蓝色石蕊试纸;⑥ 溶液;⑦
溶液;⑦ 溶液。不能区别
溶液。不能区别 和
和 气体的是
气体的是| A.①⑦ | B.①⑤⑦ | C.①⑤ | D.②③④⑤⑥ |
您最近一年使用:0次
2021-04-26更新
|
269次组卷
|
2卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
单选题
|
适中(0.65)
解题方法
12. 铜和镁的合金8.8g完全溶于足量的硝酸后,再加入过量的 溶液,生成15.6g沉淀,则合金与硝酸反应时,放出的气体可能是
溶液,生成15.6g沉淀,则合金与硝酸反应时,放出的气体可能是
 溶液,生成15.6g沉淀,则合金与硝酸反应时,放出的气体可能是
溶液,生成15.6g沉淀,则合金与硝酸反应时,放出的气体可能是A. | B.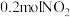 和 和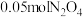 |
C.0. 和 和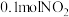 | D.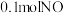 、 、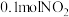 和 和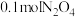 |
您最近一年使用:0次
单选题
|
适中(0.65)
13. 锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起,气体X和液体Y不可能是
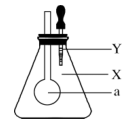

A.X是 ,Y是 ,Y是 溶液 溶液 |
B.X是 ,Y是饱和 ,Y是饱和 溶液 溶液 |
C.X是 ,Y是 ,Y是 溶液 溶液 |
D.X是 ,Y是石蕊稀溶液 ,Y是石蕊稀溶液 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
15. 一定温度下,在恒容的容器中充入 和
和 发生反应:
发生反应: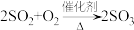 一段时间后,该反应达到化学平衡,下列能说明达到化学平衡状态的组合是
一段时间后,该反应达到化学平衡,下列能说明达到化学平衡状态的组合是
①
②
③单位时间内消耗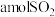 ,同时生成
,同时生成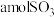
④ 、
、 和
和 的浓度之比为2∶1∶2
的浓度之比为2∶1∶2
⑤混合气体的总的物质的量不再改变
⑥混合气体的压强不再改变
⑦混合气体的密度不再改变
⑧混合气体的平均相对分子质量不再改变
 和
和 发生反应:
发生反应: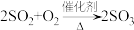 一段时间后,该反应达到化学平衡,下列能说明达到化学平衡状态的组合是
一段时间后,该反应达到化学平衡,下列能说明达到化学平衡状态的组合是①

②

③单位时间内消耗
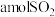 ,同时生成
,同时生成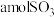
④
 、
、 和
和 的浓度之比为2∶1∶2
的浓度之比为2∶1∶2⑤混合气体的总的物质的量不再改变
⑥混合气体的压强不再改变
⑦混合气体的密度不再改变
⑧混合气体的平均相对分子质量不再改变
| A.①⑤⑥⑧ | B.①②③⑤ | C.⑤⑥⑦⑧ | D.④⑤⑥⑦ |
【知识点】 化学平衡状态的判断方法解读
您最近一年使用:0次
2021-04-26更新
|
452次组卷
|
2卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
16. 某厂漂白车间需要33.6L(标准状况下) ,某化学小组经计算后,取一定量的锌与
,某化学小组经计算后,取一定量的锌与 浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的
浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的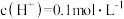 ,即将收集所得气体全部送至车间,不料经质检科检验后,发现产品存在严重的质量问题,气体随即被退回。
,即将收集所得气体全部送至车间,不料经质检科检验后,发现产品存在严重的质量问题,气体随即被退回。
(1)写出锌与浓硫酸反应的化学方程式:___________ 。
(2)下列叙述中正确的是___________ (填字母)。
A.气体A为 和
和 的混合物 B.气体A中
的混合物 B.气体A中 和
和 的体积比为4∶1
的体积比为4∶1
C.反应中共消耗Zn97.5g D.反应中共转移3mol电子
(3)为了验证所制气体的成分,该化学小组设计了如图所示的实验装置。

①连接好仪器,开始实验前,必须进行的一个操作是___________ 。
②A中加入的试剂是___________ , 溶液的作用是。
溶液的作用是。
③证明气体中混有某杂质气体的实验现象: C中:___________ ,D中:___________ 。
 ,某化学小组经计算后,取一定量的锌与
,某化学小组经计算后,取一定量的锌与 浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的
浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的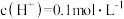 ,即将收集所得气体全部送至车间,不料经质检科检验后,发现产品存在严重的质量问题,气体随即被退回。
,即将收集所得气体全部送至车间,不料经质检科检验后,发现产品存在严重的质量问题,气体随即被退回。(1)写出锌与浓硫酸反应的化学方程式:
(2)下列叙述中正确的是
A.气体A为
 和
和 的混合物 B.气体A中
的混合物 B.气体A中 和
和 的体积比为4∶1
的体积比为4∶1C.反应中共消耗Zn97.5g D.反应中共转移3mol电子
(3)为了验证所制气体的成分,该化学小组设计了如图所示的实验装置。

①连接好仪器,开始实验前,必须进行的一个操作是
②A中加入的试剂是
 溶液的作用是。
溶液的作用是。③证明气体中混有某杂质气体的实验现象: C中:
【知识点】 浓硫酸的强氧化性解读 探究物质组成或测量物质的含量解读
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
17. 通过海水晾晒可得粗盐,粗盐中除含有 外,还含有
外,还含有 、
、 、
、 以及泥沙等杂质。制备精盐的各步操作流程如下:
以及泥沙等杂质。制备精盐的各步操作流程如下:

(1)在第⑦步蒸发过程中要用玻璃棒搅拌,目的是___________ 。
(2)为除去 、
、 、
、 ,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量)加入的顺序为
,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量)加入的顺序为___________ (填字母)。
A. B.
B. C.
C.
(3)第⑥步操作中发生反应的离子方程式为___________ 。
(4)在第③步操作中,选择的除杂试剂不能是KOH溶液,理由是___________ 。
(5)第⑤步操作中,需要的玻璃仪器有___________ 、___________ 、___________ 。
 外,还含有
外,还含有 、
、 、
、 以及泥沙等杂质。制备精盐的各步操作流程如下:
以及泥沙等杂质。制备精盐的各步操作流程如下:
(1)在第⑦步蒸发过程中要用玻璃棒搅拌,目的是
(2)为除去
 、
、 、
、 ,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量)加入的顺序为
,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量)加入的顺序为A.
 B.
B. C.
C.
(3)第⑥步操作中发生反应的离子方程式为
(4)在第③步操作中,选择的除杂试剂不能是KOH溶液,理由是
(5)第⑤步操作中,需要的玻璃仪器有
您最近一年使用:0次
2021-04-26更新
|
116次组卷
|
2卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
18. 分别按如图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中Ⓐ为电流表。请回答下列问题:
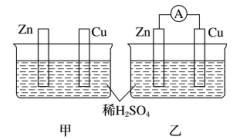
(1)以下叙述中,正确的是___________ (填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为___________ ;乙为___________ 。
(3)某同学依据氧化还原反应: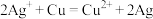 设计的原电池如图所示:
设计的原电池如图所示:
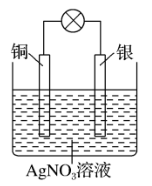
①负极的材料是___________ ,发生的电极反应为___________ ;
②外电路中的电子是从___________ 电极流向___________ 电极。(写出电极材料的名称)
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是___________ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的主要形式:甲为
(3)某同学依据氧化还原反应:
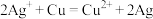 设计的原电池如图所示:
设计的原电池如图所示:
①负极的材料是
②外电路中的电子是从
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是
您最近一年使用:0次
2021-04-26更新
|
429次组卷
|
2卷引用:湖北省部分高中联考协作体2020-2021学年高一下学期期中考试化学试题
填空题
|
较易(0.85)
19. (1)在某一容积为2L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
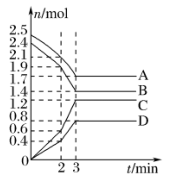
回答下列问题:
①该反应的化学方程式为___________ 。
②前2min用A的浓度变化表示的化学反应速率为___________ 。在2min时,图象发生改变的原因是___________ (填字母)。
A.增大压强 B.降低温度
C.加入催化剂 D.增加A的物质的量
(2)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大?___________ min(填“0~1”“1~2”“2~3”“3~4”或“4~5”),原因是___________ 。
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率:___________ (设溶液体积不变)。
(3)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是(填字母)_____ 。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液

回答下列问题:
①该反应的化学方程式为
②前2min用A的浓度变化表示的化学反应速率为
A.增大压强 B.降低温度
C.加入催化剂 D.增加A的物质的量
(2)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 100 | 240 | 464 | 576 | 620 |
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率:
(3)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是(填字母)
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
【知识点】 化学反应速率计算解读 影响化学反应速率的外因
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学反应原理、认识化学科学、化学实验基础
试卷题型(共 19题)
题型
数量
单选题
15
解答题
2
填空题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 二氧化硫的物理性质 酸性氧化物的通性 二氧化硫与其他强氧化剂的反应 | |
| 2 | 0.94 | 硫酸物理性质 浓硫酸的吸水性 浓硫酸的脱水性 | |
| 3 | 0.65 | 影响化学反应速率的内因 浓度对化学反应速率的影响 压强对化学反应速率的影响 温度对化学反应速率的影响 | |
| 4 | 0.85 | 可逆反应及反应限度 化学平衡建立的过程 化学平衡状态本质及特征 | |
| 5 | 0.65 | 吸热反应和放热反应 | |
| 6 | 0.65 | 原电池原理理解 通过实验探究原电池原理 原电池电子流向判断及应用 | |
| 7 | 0.65 | 二次电池 锰锌干电池 氢氧燃料电池 | |
| 8 | 0.65 | 自然界氮的固定 | |
| 9 | 0.65 | 硝酸 硝酸的强氧化性 | |
| 10 | 0.85 | 硅酸与硅酸盐 硅酸盐工业 | |
| 11 | 0.65 | 酸性氧化物的通性 二氧化硫的漂白性 二氧化硫的弱氧化性 二氧化硫与其他强氧化剂的反应 | |
| 12 | 0.65 | 氧化还原反应有关计算 有关酸性环境下硝酸根氧化性的有关计算 铜与强氧化性酸的反应 | |
| 13 | 0.65 | 氨的物理性质 氨水的性质 二氧化硫 硫化氢 | |
| 14 | 0.65 | 原电池概念及组成 原电池的结构 | |
| 15 | 0.65 | 化学平衡状态的判断方法 | |
| 二、解答题 | |||
| 16 | 0.65 | 浓硫酸的强氧化性 探究物质组成或测量物质的含量 | 实验探究题 |
| 17 | 0.65 | 离子反应在混合物分离、除杂中的应用 物质的分离、提纯 物质分离、提纯综合应用 | 实验探究题 |
| 三、填空题 | |||
| 18 | 0.65 | 原电池原理的应用 原电池原理理解 原电池正负极判断 | |
| 19 | 0.85 | 化学反应速率计算 影响化学反应速率的外因 | |