名校
解题方法
1 . 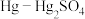 标准电极常用于测定其他电极的电势,测知
标准电极常用于测定其他电极的电势,测知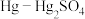 电极的电势高于
电极的电势高于 电极的电势。以下说法正确的是( )
电极的电势。以下说法正确的是( )

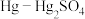 标准电极常用于测定其他电极的电势,测知
标准电极常用于测定其他电极的电势,测知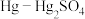 电极的电势高于
电极的电势高于 电极的电势。以下说法正确的是( )
电极的电势。以下说法正确的是( )
A. 溶液可用 溶液可用 代替 代替 |
B. 电极反应为 电极反应为 |
| C.微孔瓷片起到阻隔离子通过的作用 |
D.若把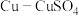 体系换作 体系换作 体系,电压表的示数变大 体系,电压表的示数变大 |
您最近一年使用:0次
2023-10-17更新
|
419次组卷
|
14卷引用:湖北省武汉市蔡甸区汉阳一中2020-2021学年高一下学期5月月考化学试题
湖北省武汉市蔡甸区汉阳一中2020-2021学年高一下学期5月月考化学试题河北省廊坊市香河县2020-2021学年高一下学期期末调研考试化学试题辽宁省2021年普通高中学业水平选择考适应性测试化学试题福建省莆田一中2021届高三模拟质量检测化学试题重庆市第一中学校 2021-2022学年高二上学期入学摸底考试化学试题江西省吉安市第一中学2021-2022学年度高二上学期开学考试化学试题(已下线)第12练 原电池原理及其应用-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)第六章 化学反应与能量 第35练 原电池 化学电源重庆市第一中学校2020-2021学年高二下学期期末考试化学试题(已下线)第3讲 原电池 化学电源山东师范大学附属中学2023-2024学年高二上学期10月月考化学试题福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题广东省深圳市高级中学2023-2024学年高二上学期期中考试化学试题
名校
2 . 化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
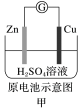


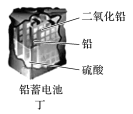




| A.甲:Zn2+向Cu电极方向移动,溶液中H+浓度减小 |
| B.乙:正极的电极反应式为Zn-2e-+2OH-=Zn(OH)2 |
| C.丙:锌筒作负极,发生氧化反应,锌筒会变薄 |
| D.丁:放电一段时间后,电解质溶液的浓度减小,两极质量增加 |
您最近一年使用:0次
名校
解题方法
3 . 原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是
| A.Al、Cu、稀H2SO4组成原电池,负极反应式为:Al-3e-=Al3+ |
B.Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO +2H2O +2H2O |
| C.由Al、Cu、浓硝酸组成原电池,负极反应式为:Al-3e-=Al3+ |
| D.由Fe、Cu、FeCl3溶液组成原电池,负极反应式:Fe-2e-=Fe2+ |
您最近一年使用:0次
名校
解题方法
4 . 微型银一锌电池可用作电子仪器的电源,其电极分别是Ag/Ag2O和Zn,电解质为KOH溶液,电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2,下列说法正确的是
| A.正极发生反应Ag2O+2H++2e-=2Ag+H2O |
| B.负极发生反应Zn+2OH--2e-=Zn(OH)2 |
| C.电池工作过程中,KOH溶液浓度减小 |
| D.电池工作过程中,电解液中OH-向正极迁移 |
您最近一年使用:0次
2022-09-06更新
|
154次组卷
|
2卷引用:湖北省恩施州高中教育联盟2020-2021学年高一下学期期末考试化学试题
名校
解题方法
5 . 如图为一原电池示意图,在原电池两极之间设有隔膜,Zn2+、SO 可以自由通过。则下列说法不正确的是
可以自由通过。则下列说法不正确的是

 可以自由通过。则下列说法不正确的是
可以自由通过。则下列说法不正确的是
| A.Zn2+通过隔膜从负极区向正极区移动 |
| B.电子由Cu极通过导线流向Zn极 |
| C.一段时间后,ZnSO4溶液浓度增大,CuSO4溶液浓度减小 |
| D.隔膜可以避免Zn极直接接触CuSO4溶液,提高了能量转换效率 |
您最近一年使用:0次
2022-01-11更新
|
564次组卷
|
4卷引用:湖北省部分省级示范高中2020-2021学年高一下学期期末测试化学试题
名校
解题方法
6 . 根据化学能转化电能的相关知识,回答下列问题:
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_______ ,发生_______ 反应,电解质溶液是_______ 。
(2)正极上出现的现象是___________________ 。
(3)若导线上转移电子1 mol,则生成银___________________ g。
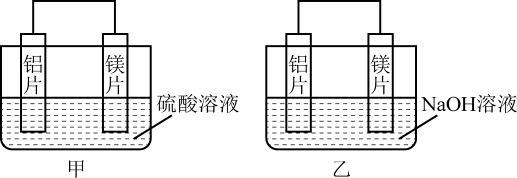
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
(4)写出甲中正极的电极反应式:___________________ 。
(5)乙中负极为___________________ ,总反应的离子方程式:___________________ 。
(6)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有___________________。
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子1 mol,则生成银
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。

(4)写出甲中正极的电极反应式:
(5)乙中负极为
(6)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有___________________。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析 |
您最近一年使用:0次
2022-01-07更新
|
92次组卷
|
3卷引用:湖北省黄石市有色一中2020-2021学年高一下学期期末考试化学试题
名校
解题方法
7 . 一种锂电池的工作原理如图所示,正极反应被可以在正极区和氧化罐间循环流通,氧化罐中加入的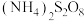 可以将Fe2+氧化、自身被还原为
可以将Fe2+氧化、自身被还原为 。下列关于该电池的说法正确的是
。下列关于该电池的说法正确的是
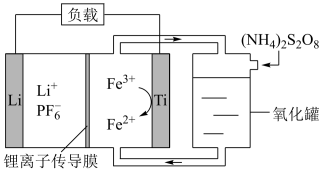
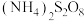 可以将Fe2+氧化、自身被还原为
可以将Fe2+氧化、自身被还原为 。下列关于该电池的说法正确的是
。下列关于该电池的说法正确的是
| A.电池放电时将电能转化为化学能 |
| B.放电时Li+由正极区移向负极区 |
C.放电时的负极反应为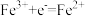 |
D.氧化罐中反应的离子方程式为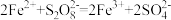 |
您最近一年使用:0次
2021-11-13更新
|
564次组卷
|
15卷引用:湖北省武汉市部分重点中学2020-2021学年高一下学期期中考试化学试题
湖北省武汉市部分重点中学2020-2021学年高一下学期期中考试化学试题湖北省巴东县第一高级中学2020-2021学年高一下学期第二次月考化学试题河北省廊坊市河北省三河市第一中学2020-2021学年高一下学期第二次阶段考化学试题吉林省松原市乾安七中2020-2021学年高一下学期第七次质量检测化学试题江苏省如皋市2021届高三上学期期末教学质量调研化学试题江苏省宜兴市张渚高级中学2020-2021学年高二下学期期中考试化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省盐城市上冈高级中学2021-2022学年高三上学期第一次学情检测(实验班)化学试题山东省枣庄滕州市2021-2022学年高三上学期期中考试化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第34练 原电池-2023年高考化学一轮复习小题多维练(全国通用)(已下线)考点18 原电池 化学电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
8 . 化学反应与生产研究息息相关,我们不仅关注能量变化,还需要关注化学反应的快慢和程度。请根据要求,回答下列问题:
(1)下面是四个化学反应理论上不可以用于设计原电池的化学反应是_______ (填字母,下同)
A.
B.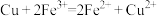
C.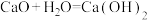
D.
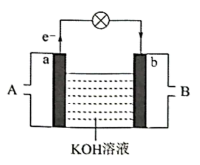
(2)将氢气与氧气的反应设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中_______ (填A或B)处电极入口通氧气,其电极反应式为_______ 。当消耗标准状况下氢气11.2L时,假设能量转化率为85%,则导线中转移电子的物质的量为_______  。
。
(3)某温度时,在2L容器中发生X、Y两种物质间的转化反应,X、Y物质的量随时间变化的曲线如图所示:

①该反应的化学方程式为_______ 。
②反应开始至2min时,Y的平均反应速率为_______ 。
③2min时,v正_______ (填“>”“<”或“=”)v逆。
(1)下面是四个化学反应理论上不可以用于设计原电池的化学反应是
A.

B.
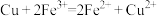
C.
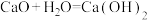
D.

(2)将氢气与氧气的反应设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中
 。
。
(3)某温度时,在2L容器中发生X、Y两种物质间的转化反应,X、Y物质的量随时间变化的曲线如图所示:

①该反应的化学方程式为
②反应开始至2min时,Y的平均反应速率为
③2min时,v正
您最近一年使用:0次
2021-07-05更新
|
921次组卷
|
4卷引用:湖北省黄冈市2020-2021学年高一下学期期末调研考试化学试题
解题方法
9 . 如图为发光二极管连接柠檬电池。下列说法不正确 的是
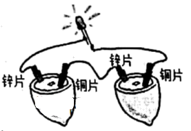

| A.该装置的能量转化形式主要为化学能→电能 |
| B.电子的流向:Zn→导线→Cu→柠檬液→Zn |
| C.锌片是负极,质量不断减小 |
| D.铜片上的电极反应为:2H++2e-=H2↑ |
您最近一年使用:0次
2021-06-28更新
|
527次组卷
|
5卷引用:湖北省黄石市有色一中2020-2021学年高一下学期期末考试化学试题
湖北省黄石市有色一中2020-2021学年高一下学期期末考试化学试题浙江省宁波市慈溪市2020-2021学年高一下学期期末考试化学试题天津市红桥区2021-2022学年高三上学期期中考试化学试题(已下线)2022年1月浙江省普通高中学业水平考试化学仿真模拟试卷A浙江省杭嘉湖金四县区2021-2022学年高一下学期学考模拟化学试题
名校
解题方法
10 . 某小组为研究原电池原理,设计如图装置。下列叙述正确的是
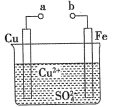

| A.a和b不连接时,铁片上会有H2产生 |
| B.a和b用导线连接时,铁片上发生的反应为Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b用导线连接时,电子由a流向b |
您最近一年使用:0次
2021-06-01更新
|
330次组卷
|
8卷引用:湖北省鄂东学校2020-2021学年高一下学期5月联考化学试题



