解题方法
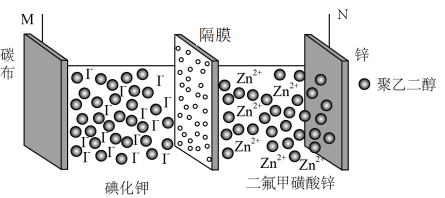
1 . 碘因来源丰富和具有较快的氧化还原动力性能使其作为电池的正极材料备受青睐。如图为聚乙二醇(PEG)水系电解液锌碘双离子二次电池的装置示意图。已知:PEG与 易发生络合反应,生成的PEG的碘化物不能穿过隔膜,下列说法不正确的是
易发生络合反应,生成的PEG的碘化物不能穿过隔膜,下列说法不正确的是
 易发生络合反应,生成的PEG的碘化物不能穿过隔膜,下列说法不正确的是
易发生络合反应,生成的PEG的碘化物不能穿过隔膜,下列说法不正确的是
A.PEG可以防止 穿梭到N电极区域 穿梭到N电极区域 |
| B.放电时,电子由N极经外电路流向M极 |
C.充电时,N电极反应式为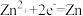 |
| D.隔膜上的孔隙越小,电池的性能越好 |
您最近一年使用:0次
解题方法
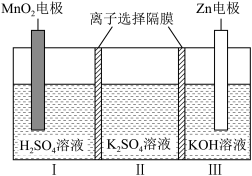
2 . 一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(已知:KOH溶液中,Zn2+以Zn(OH) 存在)。电池放电时,下列说法正确的是
存在)。电池放电时,下列说法正确的是
 存在)。电池放电时,下列说法正确的是
存在)。电池放电时,下列说法正确的是
| A.MnO2电极为负极 | B.I区的SO 通过隔膜向Ⅱ区迁移 通过隔膜向Ⅱ区迁移 |
| C.Ⅱ区的K+通过隔膜向Ⅲ区迁移 | D.Zn电极反应:Zn+2e-+4OH-=Zn(OH) |
您最近一年使用:0次
名校
解题方法
3 . 下列图示的装置不能形成原电池的是
A.稀硫酸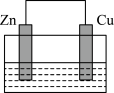 | B.硫酸铜溶液 |
C.稀硫酸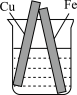 | D. 稀盐酸 稀盐酸 |
您最近一年使用:0次
2023-04-18更新
|
442次组卷
|
2卷引用:江苏省连云港高级中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
4 . 任何化学反应都伴随着能量的变化,通过化学反应,化学能可转化为热能、电能等不同形式的能量。
(1)H2可用于工业合成氨气,已知拆开1molH—H、1molN≡N分别需要吸收的能量为436kJ、946kJ,形成1molN—H会放出能量391kJ,则在反应N2+3H2 2NH3中,每生成2molNH3,
2NH3中,每生成2molNH3,_______ (填“吸收”或“放出”)热量_______ kJ。当在相同的条件下向容器中充入1molN2和3molH2时,它们反应对应的热量_______ (填“大于”“等于”或“小于”)你所计算出的值。
(2)用图甲、乙所示装置进行实验,请回答下列问题。
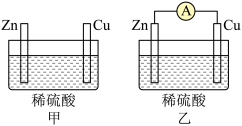
以下叙述中,正确的是_______ (填字母)。
a.甲中铜片是正极,乙中锌片是负极
b.两池中溶液的pH均增大
c.两池中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标准状况下的体积均为2.24L
(3)Mg、Al设计成如图所示原电池装置:
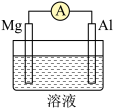
若溶液为氢氧化钠溶液,负极的电极反应为_______ 。
(4)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
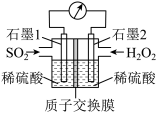
①石墨1为_______ (填“正极”或“负极”);正极的电极反应式为_______ 。
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为_______ 。
(1)H2可用于工业合成氨气,已知拆开1molH—H、1molN≡N分别需要吸收的能量为436kJ、946kJ,形成1molN—H会放出能量391kJ,则在反应N2+3H2
 2NH3中,每生成2molNH3,
2NH3中,每生成2molNH3,(2)用图甲、乙所示装置进行实验,请回答下列问题。

以下叙述中,正确的是
a.甲中铜片是正极,乙中锌片是负极
b.两池中溶液的pH均增大
c.两池中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标准状况下的体积均为2.24L
(3)Mg、Al设计成如图所示原电池装置:

若溶液为氢氧化钠溶液,负极的电极反应为
(4)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。

①石墨1为
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
您最近一年使用:0次
2023-04-12更新
|
668次组卷
|
2卷引用:广西百色高级中学田林分校2022-2023学年高一下学期3月月考化学试题
解题方法
5 . 下图是发表于《科学进展》的一种能够捕捉 的电化学装置。下列说法正确的是
的电化学装置。下列说法正确的是

 的电化学装置。下列说法正确的是
的电化学装置。下列说法正确的是
| A.该装置将电能转化为化学能 |
B.正极的电极反应为 |
C.每生成 的草酸铝,外电路中转移 的草酸铝,外电路中转移 电子 电子 |
| D.随着反应的进行,草酸盐的浓度减小 |
您最近一年使用:0次
名校
解题方法
6 . 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是
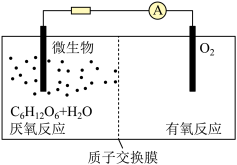

| A.正极反应中有H2O生成 |
| B.微生物参与的反应中无电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
D.电池总反应为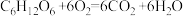 |
您最近一年使用:0次
解题方法
7 . 用a、b、c、d四种金属片进行如下实验,实验装置和现象如下表所示:
据此判断,这四种金属的活动性顺序为
| 装置 |  |  |  |
| 现象 | a电极附近产生大量气泡 | 电子由c电极经导线流向d电极 | 电解质溶液颜色变浅,b电极质量增加 |
| A.a>b>c>d | B.a>b>d>c | C.b>a,b>d>c | D.c>d>b>a |
您最近一年使用:0次
解题方法
8 . 某种培根型碱性氢氧燃料电池示意图如所示,下列有关该电池的说法不正确 的是
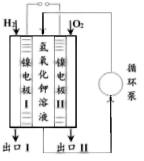

A.电池放电时, 向镍电极Ⅰ的方向迁移 向镍电极Ⅰ的方向迁移 |
B.正极电极反应为: |
| C.出口Ⅰ处有水生成 |
| D.循环泵可使电解质溶液不断浓缩、循环 |
您最近一年使用:0次
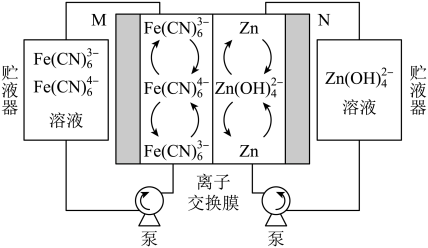
9 . 碱性锌铁液流电池具有电压高、成本低的优点。该电池的总反应为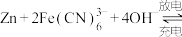
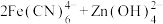 ,下列叙述不正确的是
,下列叙述不正确的是
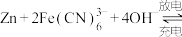
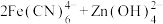 ,下列叙述不正确的是
,下列叙述不正确的是
A.放电时,M极电极反应式为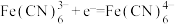 |
B.充电时,右侧贮液器中 浓度降低 浓度降低 |
C.若离子交换膜只有 通过, 通过,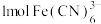 反应时,有 反应时,有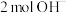 通过离子交换膜 通过离子交换膜 |
D.电池工作时,当电路中转移 个电子,理论上消耗锌16.25 g 个电子,理论上消耗锌16.25 g |
您最近一年使用:0次
2023-03-28更新
|
211次组卷
|
2卷引用:湖南省名校联盟2022-2023学年高三下学期第二次联考化学试题
名校
解题方法
10 . 银锌电池广泛用作各种电子仪器的电源,其电极分别为 、
、 ,电解质溶液为
,电解质溶液为 溶液,总反应为
溶液,总反应为 。下列说法中错误的是
。下列说法中错误的是
 、
、 ,电解质溶液为
,电解质溶液为 溶液,总反应为
溶液,总反应为 。下列说法中错误的是
。下列说法中错误的是A.原电池放电时,负极上发生反应的物质是 |
B.溶液中 向正极移动, 向正极移动, 、 、 向负极移动 向负极移动 |
C.工作时,电子由 电极沿导线流向 电极沿导线流向 电极 电极 |
D.负极上发生的反应是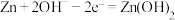 |
您最近一年使用:0次



