1 . 下图是飞船和空间站中利用Sabatier反应再生氧气的大体流程。
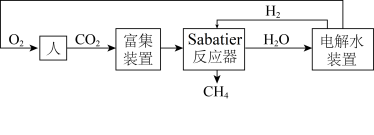
(1)已知:2H2(g)+O2(g) 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1
CH4(g)+2O2(g) CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
则Sabatier反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=___________ 。
(2)二氧化碳的富集装置如图所示。
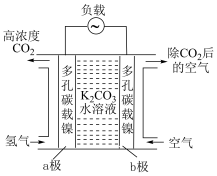
①该富集法采用___________ 原理(填“原电池”或“电解池”)。当a极上消耗1molH2,并保持电解液溶质不变时,b极上除去的CO2在标准状况下的体积为___________ 。
②工作一段时间后,K2CO3溶液的pH___________ (填“变大”“变小”或“不变”)。
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是___________ 。
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是___________ 。
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=___________ (用P0表示)。已知Kp是以分压表示的平衡常数,分压=总压×物质的量分数。
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为___________ (填化学式)。

(1)已知:2H2(g)+O2(g)
 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1CH4(g)+2O2(g)
 CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1则Sabatier反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=(2)二氧化碳的富集装置如图所示。

①该富集法采用
②工作一段时间后,K2CO3溶液的pH
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为
| 离子种类 | H+ | OH- |  SO SO | Cl- |  CO CO | K+ | Na+ |
| 摩尔电导率×104(S·m2·mol-1) | 349.82 | 198.0 | 79.8 | 76.34 | 72.0 | 73.52 | 50.11 |
您最近一年使用:0次
名校
解题方法
2 . 中国科学技术大学科研人员开发了一种高性能的水系锰基锌电池。该装置获得电能的同时可以制得 ,其工作原理如图所示,下列说法正确的是
,其工作原理如图所示,下列说法正确的是

 ,其工作原理如图所示,下列说法正确的是
,其工作原理如图所示,下列说法正确的是
| A.电池放电时,正极区溶液的pH降低 |
| B.a膜为阳离子交换膜,b膜为阴离子交换膜 |
C.X溶液中的溶质只能为 ,Y溶液中溶质只能为KOH ,Y溶液中溶质只能为KOH |
| D.放电时,消耗1mol Zn时,正极区电解质溶液增重87g |
您最近一年使用:0次
2022-12-27更新
|
1062次组卷
|
5卷引用:山东省潍坊市2022年12月高三优生学习质量检测化学试题
解题方法
3 . 目前,锂硫电池是最接近实用的大容量储能电池。一种锂硫电池的工作原理如图所示:
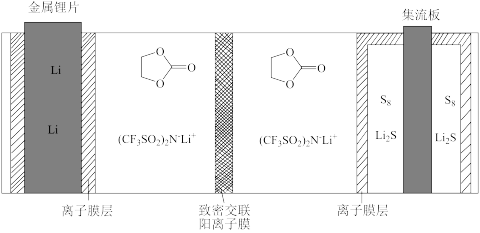
下列说法中正确的是

下列说法中正确的是
| A.放电时,锂电极的电势高 |
| B.电解质溶液可以用无机物水溶液代替 |
C.放电时, 由右室通过致密交联阳离子膜移到左室 由右室通过致密交联阳离子膜移到左室 |
D.放电时,正极反应式为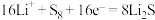 |
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)下列反应是氧化还原反应且是吸热反应的是____ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为____ ,当线路中转移0.2mol电子时,则被腐蚀铜的质量为____ g。
(3)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为____ ,正极附近溶液的碱性____ (填“增强”“减弱”“不变”)。
(4)实验小组对可逆反应aX(g)+bY(g) pZ(g)进行探究。回答下列问题:
pZ(g)进行探究。回答下列问题:
T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
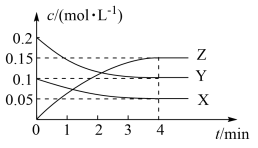
①0~4min内的反应速率v(Y)=____ 。
②为提高此反应的速率,下列措施可行的是____ (填字母代号)。
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达最大限度时Y的体积分数为____ 。
④下列描述能表示该反应达平衡状态的是____ 。
A.容器内的混合气体的平均相对分子质量不再改变
B.容器内压强不再发生变化
C.2v(X)=v(Y)
D.X的体积分数不再改变
(1)下列反应是氧化还原反应且是吸热反应的是
| A.稀醋酸与烧碱溶液反应 | B.灼热的炭与CO2的反应 |
| C.铁片与稀盐酸的反应 | D.Ba(OH)2•8H2O与NH4Cl的反应 |
(3)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为(4)实验小组对可逆反应aX(g)+bY(g)
 pZ(g)进行探究。回答下列问题:
pZ(g)进行探究。回答下列问题:T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。

①0~4min内的反应速率v(Y)=
②为提高此反应的速率,下列措施可行的是
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达最大限度时Y的体积分数为
④下列描述能表示该反应达平衡状态的是
A.容器内的混合气体的平均相对分子质量不再改变
B.容器内压强不再发生变化
C.2v(X)=v(Y)
D.X的体积分数不再改变
您最近一年使用:0次
名校
解题方法
5 . 有机物电极材料具有来源丰富、可降解等优点,一种负极材料为固态聚酰亚胺-水系二次电池的结构如图所示。下列说法正确的是
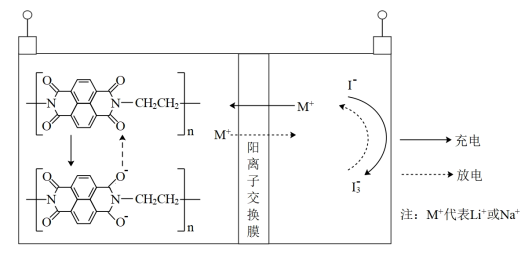

| A.充电时有机电极发生了氧化反应 |
B.充电时每转移 ,右室离子数目减少 ,右室离子数目减少 |
C.放电时负极电极反应为: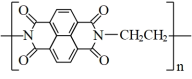 -2e-= -2e-=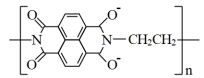 |
D.将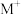 由 由 换成 换成 ,电池的比能量会下降 ,电池的比能量会下降 |
您最近一年使用:0次
2022-04-14更新
|
2562次组卷
|
18卷引用:广东省佛山市普通高中2022届高三教学质量检测(二)化学试题
广东省佛山市普通高中2022届高三教学质量检测(二)化学试题广东省佛山市2022届高三下学期4月第二次教学质量监测(二模)化学试题(已下线)必刷卷04-2022年高考化学考前信息必刷卷(全国乙卷)福建省龙岩第一中学2022届高三毕业班模拟训练(二)化学试题(已下线)押江苏卷第12题 电化学及其应用 -备战2022年高考化学临考题号押题(江苏卷)(已下线)【直抵名校】04-备战2022年高考化学名校进阶模拟卷(通用版)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题湖南省岳阳县第一中学2022届高三下学期5月月考化学试题湖南省湘东九校2021-2022学年高二下学期期末联考化学试题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)化学(辽宁A卷)-学易金卷:2023年高考第一次模拟考试卷湖南省株洲市九方中学2022-2023学年高三上学期第四次月考化学试题福建省厦门第一中学2022-2023学年高三上学期11月期中考试化学试题辽宁省葫芦岛市第一高级中学2022-2023学年高三上学期期末线上教学阶段检测化学试题江苏省常州市第一中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市第二中学2023届高三第七次月考化学试题(已下线)T10-电化学原理山东省滕州市2023-2024学年高三上学期期中考试化学试题
6 . 一种全有机质子二次电池放电原理如图所示,电极材料中的P、PO、PR均为有机高分子化合物。下列说法正确的是


| A.放电时,电极M发生氧化反应 |
| B.放电时,H+移向电极N |
| C.充电一段时间后,电解液的pH未变 |
| D.充电时,阳极反应为P-2e-=PO+2H+ |
您最近一年使用:0次
2022-03-12更新
|
858次组卷
|
3卷引用:山东省烟台市、德州市2021-2022学年下学期高三一模化学试题
山东省烟台市、德州市2021-2022学年下学期高三一模化学试题(已下线)卷03 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)江西省鹰潭市、宜春市三校2021-2022学年高二下学期第二次月考化学试题
7 . 我国科学家正在研究一种可充电Na—Zn双离子电池体系(如图)。下列说法不正确 的是

| A.闭合K1时,装置中的化学能转化为电能 |
| B.闭合K2充电时,a须为电源的负极 |
| C.闭合K1,当外电路流过xmol电子时,负极区减少2xmolNa+ |
D.电池,总反应式可表示为:xZn+2Na0.6-xMnO2+4xOH-+2xNa+ 2Na0.6MnO2+x[Zn(OH)4]2- 2Na0.6MnO2+x[Zn(OH)4]2- |
您最近一年使用:0次
解题方法
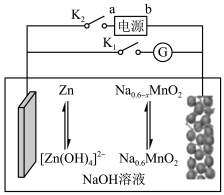
8 . 利用生物燃料电池原理研究室温下氨的合成,电池工作时 在电极与酶之间传递电子,示意图如下所示。下列说法
在电极与酶之间传递电子,示意图如下所示。下列说法不正确 的是

 在电极与酶之间传递电子,示意图如下所示。下列说法
在电极与酶之间传递电子,示意图如下所示。下列说法
A.正极电极反应式为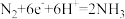 |
B.负极区,在氢化酶作用下发生反应 |
| C.电池工作时质子通过交换膜由负极区向正极区移动 |
| D.相比现有工业合成氨,该方法条件温和,同时还可提供电能 |
您最近一年使用:0次
2022-01-21更新
|
217次组卷
|
2卷引用:浙江省湖州市2021-2022学年高二上学期期末考试化学试题
名校
9 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 一段时间后,取铁电极区少量溶液于试管中,滴加铁氰化钾溶液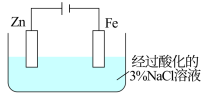 | 未出现特征蓝色的沉淀 | 锌、铁与酸化的氯化钠溶液构成原电池后,锌能够有效保护铁制品 |
| B | 向2支盛有5 mL0.1 mol·L-1H2SO4溶液的试管中分别加入5mL0.1 mol·L-1 Na2S2O3溶液,分别放入20 °C,40 °C的水浴中,并开始计时 | 40°C下出现浑浊的时间短 | 温度越高反应速率越快 |
| C | 向10 ml. 0.2 mol·L-1 NaOH 溶液中滴加2滴0.1 mol· L-1 MgCl2溶液,产生白 色沉淀后,再滴加2滴0.1 mol·L-1FeCl3溶液 | 生成红褐色沉淀 | 证明在相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 在相同条件下,用pH计分别测定0.1 mol·L-1FeCl3溶液和0.01 mol·L-1FeCl3溶液的pH | 0.1 mol·L-1FeCl3溶液的pH为1.16,0.01 mol·L-1 FeCl3溶液的pH为1.76 | 增大c(FeCl3),抑制FeCl3水解,也说明加水稀释后水解平衡右移,促进FeCl3水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-15更新
|
160次组卷
|
2卷引用:湖南省大联考2021-2022学年高二上学期期末考试化学试题
2021·云南·一模
名校
解题方法
10 . 我国电动汽车产业发展迅猛,多种车型采用三元锂电池,其正极材料可表示为Li1-aNixCoyMnzO2其中Ni、Co、Mn的化合价分别为+2、+3、+4,且x+y+z=1,电池总反应为Li1-aNixCoyMnzO2+LiaC6 LiNixCoyMnzO2+6C(石墨),其电池工作原理如图所示,两板之间有一个允许特定离子X通过的隔膜。下列说法错误的是
LiNixCoyMnzO2+6C(石墨),其电池工作原理如图所示,两板之间有一个允许特定离子X通过的隔膜。下列说法错误的是

 LiNixCoyMnzO2+6C(石墨),其电池工作原理如图所示,两板之间有一个允许特定离子X通过的隔膜。下列说法错误的是
LiNixCoyMnzO2+6C(石墨),其电池工作原理如图所示,两板之间有一个允许特定离子X通过的隔膜。下列说法错误的是
| A.允许离子X通过的隔膜属于阳离子交换膜 |
| B.充电时,外电路中流过0.2mol电子,A极质量减少1.4g |
| C.在Li1-aNixCoyMnzO2材料中,若x:y:z=2:3:5,则a=0.3 |
| D.放电时,正极反应式为Li1-aNixCoyMnzO2+aLi++ae-=LiNxCoyMnzO2 |
您最近一年使用:0次
2022-01-03更新
|
1640次组卷
|
3卷引用:专项11 电化学基础-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)
(已下线)专项11 电化学基础-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)云南省2021-2022学年高三上学期“3+3+3”高考备考诊断性联考(一)理科综合化学试题四川省广元中学2022-2023学年高二下学期5月期中考试化学试题



