名校
解题方法
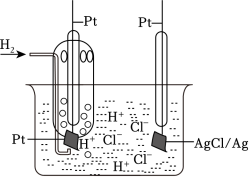
1 . 某充电电池如图所示,其反应原理为H2+2AgCl(s) 2Ag(s)+2HCl。下列说法正确的是
2Ag(s)+2HCl。下列说法正确的是
 2Ag(s)+2HCl。下列说法正确的是
2Ag(s)+2HCl。下列说法正确的是
| A.放电时,右边电极电势高 |
| B.放电时,溶液中H+向左边电极移动 |
| C.充电时,右边电极上发生的电极反应式:Ag+e﹣+Cl﹣=AgCl |
| D.充电时,当左边电极生成1molH2时,电解质溶液减轻2g |
您最近半年使用:0次
2 . 亚硫酸氢钠在染料、造纸制革、化学合成等工业中可用作还原剂。
(一)制备NaHSO3(装置如图所示)。
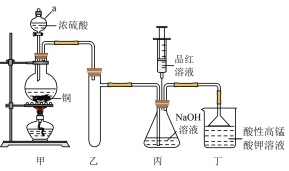
(1)装置丁的作用有①___________ ;②___________ ;③吸收尾气,防止环境污染。
(2)将丙中针筒内品红溶液推进锥形瓶中,若发现___________ ,则说明NaOH已完全转化为NaHSO3。
(二)小组同学欲探究NaHSO3与 的反应,经查阅资料后提出假设,并进行实验验证。
的反应,经查阅资料后提出假设,并进行实验验证。
已知:氯化亚铜(CuCl)是不溶于水的白色沉淀
假设1: 与
与 仅发生双水解反应
仅发生双水解反应
假设2: 可以还原
可以还原
设计实验如下:
①向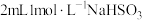 溶液中加入
溶液中加入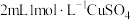 溶液,得到绿色溶液,放置一段时间无明显变化。
溶液,得到绿色溶液,放置一段时间无明显变化。
②向①所得绿色溶液中加入适量NaCl固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
(3)实验证实假设___________ 合理,实验①发生的离子方程式为___________ 。
(4)甲、乙同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差 [其中
[其中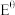 (标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
(标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
①根据上述实验结论,对比甲、乙两实验,写出乙同学实验现象为___________ (写出两条即可)。
②根据相关资料,解释产生上述现象的原因为___________ 。
(一)制备NaHSO3(装置如图所示)。

(1)装置丁的作用有①
(2)将丙中针筒内品红溶液推进锥形瓶中,若发现
(二)小组同学欲探究NaHSO3与
 的反应,经查阅资料后提出假设,并进行实验验证。
的反应,经查阅资料后提出假设,并进行实验验证。已知:氯化亚铜(CuCl)是不溶于水的白色沉淀
假设1:
 与
与 仅发生双水解反应
仅发生双水解反应假设2:
 可以还原
可以还原
设计实验如下:
①向
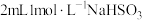 溶液中加入
溶液中加入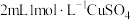 溶液,得到绿色溶液,放置一段时间无明显变化。
溶液,得到绿色溶液,放置一段时间无明显变化。②向①所得绿色溶液中加入适量NaCl固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
(3)实验证实假设
(4)甲、乙同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差
 [其中
[其中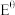 (标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
(标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:| 编号 | 甲 | 乙 |
| 实验 |  | 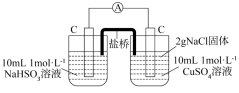 |
②根据相关资料,解释产生上述现象的原因为
您最近半年使用:0次
3 . 高电压水系锌﹣有机混合液流电池的装置如图所示。下列说法错误的是


| A.充电时,中性电解质NaCl的浓度增大 |
B.放电时,负极反应式为 |
| C.充电时,1molFQH2转化为FQ转移2mol电子 |
| D.放电时,正极区溶液的pH减小 |
您最近半年使用:0次
4 . 下图是飞船和空间站中利用Sabatier反应再生氧气的大体流程。
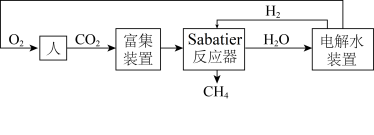
(1)已知:2H2(g)+O2(g) 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1
CH4(g)+2O2(g) CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
则Sabatier反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=___________ 。
(2)二氧化碳的富集装置如图所示。
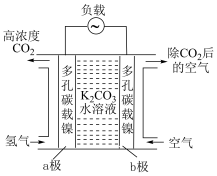
①该富集法采用___________ 原理(填“原电池”或“电解池”)。当a极上消耗1molH2,并保持电解液溶质不变时,b极上除去的CO2在标准状况下的体积为___________ 。
②工作一段时间后,K2CO3溶液的pH___________ (填“变大”“变小”或“不变”)。
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是___________ 。
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是___________ 。
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=___________ (用P0表示)。已知Kp是以分压表示的平衡常数,分压=总压×物质的量分数。
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为___________ (填化学式)。

(1)已知:2H2(g)+O2(g)
 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1CH4(g)+2O2(g)
 CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1则Sabatier反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=(2)二氧化碳的富集装置如图所示。

①该富集法采用
②工作一段时间后,K2CO3溶液的pH
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为
| 离子种类 | H+ | OH- |  SO SO | Cl- |  CO CO | K+ | Na+ |
| 摩尔电导率×104(S·m2·mol-1) | 349.82 | 198.0 | 79.8 | 76.34 | 72.0 | 73.52 | 50.11 |
您最近半年使用:0次
解题方法
5 . 2016年7月美国康奈尔大学的研究人员瓦迪·阿尔·萨达特和林登·阿彻在发表于《科学进展》(ScienceAdvances)上的一篇论文中,描述了一种能够捕捉二氧化碳的电化学电池的设计方案。其简易结构如下图。下列说法错误的是
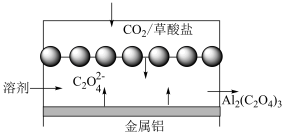

| A.金属铝作为还原剂参与负极的氧化反应 |
B.该装置除了吸收 之外还可得到化工产品 之外还可得到化工产品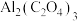 |
C.该装置每消耗27kg的金属铝,可以吸收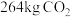 |
D.该装置的正极反应方程式为: |
您最近半年使用:0次
解题方法
6 . 如图1所示为1970年实现了商品化的一次性锂电池工作原理示意图,该锂锰电池的体积小,性能优良,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2(晶胞结构如图2)晶格中,生成LiMnO2。
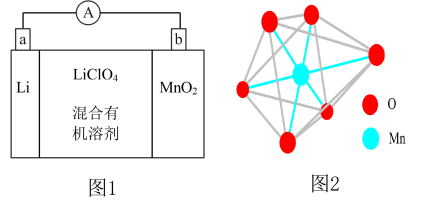
下列关于该锂电池的相关说法正确的是

下列关于该锂电池的相关说法正确的是
| A.可以用水代替有机溶剂 |
| B.b电极的反应为:MnO2+Li++e-=LiMnO2 |
| C.图2所示MnO2晶胞中氧原子的配位数为6 |
| D.外电路中电子由a极流向b极,再由b极经溶有LiClO4的混合有机溶剂回流到a极 |
您最近半年使用:0次
名校
解题方法
7 . 镁—空气电池的工作原理如图所示,电池反应方程式为:2Mg+O2+2H2O=2Mg(OH)2。下列有关该电池的说法正确的是
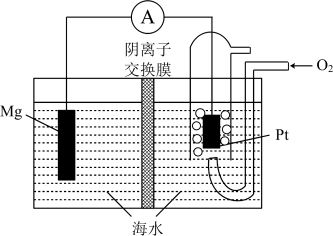

| A.氧气在Pt电极表面得到电子,故Pt电极为负极 |
| B.负极的电极反应为Mg-2e-=Mg2+ |
| C.电池工作时,溶液中的Na+由负极移向正极 |
| D.当电路中转移0.04mol电子时,参加反应的O2体积为224mL(标准状况下) |
您最近半年使用:0次
名校
解题方法
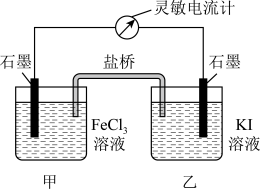
8 . 控制合适的条件,将反应2Fe3++2I- 2Fe2++I2设计成如图所示原电池,下列判断不正确的是
2Fe2++I2设计成如图所示原电池,下列判断不正确的是
 2Fe2++I2设计成如图所示原电池,下列判断不正确的是
2Fe2++I2设计成如图所示原电池,下列判断不正确的是
| A.反应开始时,电流方向是从甲池石墨棒流向乙池石墨棒 |
| B.反应开始时,甲中石墨电极上Fe3+被还原 |
| C.盐桥中的阳离子向甲池移动 |
| D.放电时,乙中石墨电极为正极 |
您最近半年使用:0次
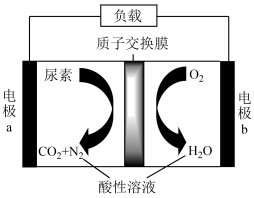
9 . 为保护环境,降低城市水体污染,科学家利用城市废水中的尿素,设计尿素 燃料电池,电池结构如图所示。下列说法不正确的是
燃料电池,电池结构如图所示。下列说法不正确的是
 燃料电池,电池结构如图所示。下列说法不正确的是
燃料电池,电池结构如图所示。下列说法不正确的是
A.电流从电极 通过外电路流向电极 通过外电路流向电极 |
B.电池工作时,正极区 减小 减小 |
C.理论上每除去 ,电路中通过 ,电路中通过 电子 电子 |
| D.利用此法,也可除去废水中的甲醇等有机物 |
您最近半年使用:0次
名校
解题方法
10 . 某铁—空气电池放电时,其原理如图所示。电池总反应为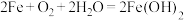 。下列说法不正确的是
。下列说法不正确的是

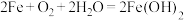 。下列说法不正确的是
。下列说法不正确的是
| A.a极发生氧化反应 | B. 极为电池正极,发生氧化反应 极为电池正极,发生氧化反应 |
C.电子从 电极经负载流向 电极经负载流向 电极 电极 | D.该装置将化学能转化为电能 |
您最近半年使用:0次



