名校
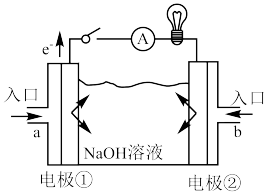
1 . 一种航天器能量储存系统的工作原理示意图如图,其中装置Y为碱性燃料电池。下列说法正确的是
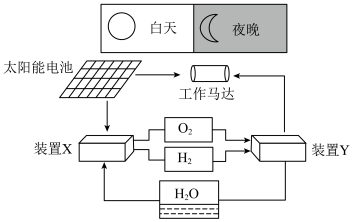
| A.太阳能电池的主要材料为高纯SiO2 |
| B.该系统中只存在太阳能、机械能和化学能三者之间的转化 |
C.装置Y的负极上的电极反应式为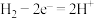 |
| D.装置X能实现电池的燃料和氧化剂再生 |
您最近一年使用:0次
7日内更新
|
68次组卷
|
2卷引用:河北省保定市部分示范性高中2023-2024学年高一下学期5月期中考试化学试题
解题方法
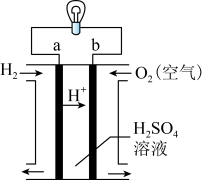
2 . 氢氧燃料电池是一种常见化学电源,其工作示意图如图。___________ (用a或b填写),其电极反应为___________ 。
(2)关于该电池,下列说法正确的是___________。
(3)若用 作燃料,以KOH溶液为电解质溶液,则
作燃料,以KOH溶液为电解质溶液,则 通入电池的
通入电池的___________ (填“正极”或“负极”),该电极反应方程式为___________ 。
(2)关于该电池,下列说法正确的是___________。
A. 由正极流向负极 由正极流向负极 |
B. 溶液的作用是传导电子 溶液的作用是传导电子 |
| C.该电池工作一段时间后,电解质溶液的酸性减弱 |
D.标准状况下a电极若每消耗 ,外电路转移电子数为 ,外电路转移电子数为 |
(3)若用
 作燃料,以KOH溶液为电解质溶液,则
作燃料,以KOH溶液为电解质溶液,则 通入电池的
通入电池的
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式正确的是
A.氢氧燃料电池的负极反应式: |
B.稀硫酸与硫代硫酸钠溶液混合: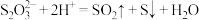 |
C.惰性电极电解 水溶液: 水溶液: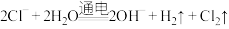 |
D.用碳酸钠溶液处理水垢中的硫酸钙: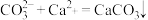 |
您最近一年使用:0次
4 . 电化学在生产、生活中有广泛的应用。下列说法正确的是
| A.铁腐蚀消耗氧气和水,食品包装袋的双吸剂可用铁粉为主要成分制作 |
B.航天器所用的氢氧燃料电池中,通入 的电极为电池的负极 的电极为电池的负极 |
C.铁钉镀铜使用硫酸铜溶液做电镀液、铜做阴极、铁做阳极,能维持电镀液 浓度不变 浓度不变 |
| D.铜的电解精炼时,粗铜中含有的锌、金、银等金属在阳极沉降下来形成阳极泥 |
您最近一年使用:0次
名校
5 . 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:___________ ,Y的转化率为___________ 。
(2)该反应的化学方程式为___________ 。
(3)下列能表示该反应达平衡状态的是___________(填选项字母)。
(4)10s后保持其他条件不变,判断改变下列条件后反应速率的变化情况:
A.继续通入一定量的X:___________ (填“增大”、“减小”或“不变”,下同)。
B.继续通入一定量的He:___________ 。
(5)下列图像或实验属于放热反应的是___________ (填序号)。___________ (填物质名称),负极的电极反应式为___________ 。

(2)该反应的化学方程式为
(3)下列能表示该反应达平衡状态的是___________(填选项字母)。
| A.容器内气体质量不再发生变化 |
| B.容器内气体压强不再发生变化 |
| C.X的体积分数不再改变 |
| D.容器内混合气体的密度不再发生变化 |
(4)10s后保持其他条件不变,判断改变下列条件后反应速率的变化情况:
A.继续通入一定量的X:
B.继续通入一定量的He:
(5)下列图像或实验属于放热反应的是

您最近一年使用:0次
名校
解题方法
6 . 下列电池工作时,属于二次电池的是
|
|
|
|
| A.锌锰电池 | B.氢氧燃料电池 | C.铅蓄电池 | D.锌银纽扣电池 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 按要求回答问题。
(1)制作印刷电路板的过程中常用FeCl3溶液与铜反应2Fe3++Cu=2Fe2++Cu2+,把该反应设计成原电池,可用___________ 作正极材料,正极反应的电极方程式为___________ 。
(2)氢氧燃料电池的构造如图所示,由此判断OH-向___________ (填“正”或“负”)极定向移动,Y极的电极反应式为___________ 。 Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量
Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量___________ (填“增大”或“减小”)。放电过程中,外电路中转移2.5 mol e-,消耗硫酸___________ mol。
(4)某电解池装置如图所示,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则___________ 。
②Y电极上的电极反应式为___________ ,检验该电极反应产物的方法及现象是___________ 。
(1)制作印刷电路板的过程中常用FeCl3溶液与铜反应2Fe3++Cu=2Fe2++Cu2+,把该反应设计成原电池,可用
(2)氢氧燃料电池的构造如图所示,由此判断OH-向

 Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量
Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量(4)某电解池装置如图所示,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
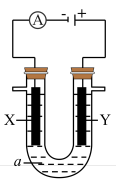
②Y电极上的电极反应式为
您最近一年使用:0次
2024-05-06更新
|
209次组卷
|
2卷引用:江苏省扬州市邗江中学2023-2024学年高一下学期三月检测化学试题
名校
8 . 元素周期律是自然科学的基本规律,也是无机化学的基础.下图为现代元素周期表的一部分,请回答下列问题:
(1)⑤和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;
(2)③、④、⑥、⑧的简单离子半径由大到小依次为___________ (用离子符号表示);
(3)由②的最低负价氢化物与最高正价氧化物的水化物反应所生成的物质中,所含化学键类型有:___________ 、___________ ;
(4)元素①②③④形成的简单气态氢化物的稳定性由弱到强的顺序排列为:___________ (用化学式表示)。
(5)某盐由③⑤⑦三种元素组成,向其水溶液中通入少量二氧化碳气体,出现白色胶状沉淀,写出该反应的离子方程式__________________________________ ;
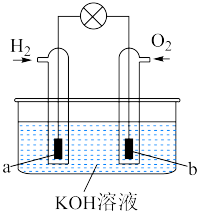
(6)氢气和③的单质可以作为燃料电池的两个电极反应气体,其装置如图所示_____ 极(填“正”或“负”),该电极上发生________ 反应(填“氧化”或“还原”);b极发生的电极反应方程式是__________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(1)⑤和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
(2)③、④、⑥、⑧的简单离子半径由大到小依次为
(3)由②的最低负价氢化物与最高正价氧化物的水化物反应所生成的物质中,所含化学键类型有:
(4)元素①②③④形成的简单气态氢化物的稳定性由弱到强的顺序排列为:
(5)某盐由③⑤⑦三种元素组成,向其水溶液中通入少量二氧化碳气体,出现白色胶状沉淀,写出该反应的离子方程式
(6)氢气和③的单质可以作为燃料电池的两个电极反应气体,其装置如图所示
您最近一年使用:0次
名校
9 . 积极发展清洁能源,推动经济社会绿色低碳转型,已经成为国际社会应对全球气候变化的普遍共识。
(1)甲醇 是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是
是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是____________ 转化为___________ ;其燃烧反应中反应物的总能量_____________ (填“大于”“小于”或“等于”)生成物的总能量。
(2)氢能是最理想的清洁能源。某氢能源公交车使用的燃料电池结构示意图(质子交换膜传导 )如图。
)如图。__________ 反应, 由
由_______ (填“M”或“N”,下同)极移向_________ 极。
②该电池工作时,M极的电极反应式为________________________________ 。
③与传统的发动机供能相比,氢能源供能的优点是_____________________ (任写一点)。
④每转移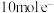 ,消耗氢气的质量为
,消耗氢气的质量为___________  。
。
(1)甲醇
 是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是
是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是(2)氢能是最理想的清洁能源。某氢能源公交车使用的燃料电池结构示意图(质子交换膜传导
 )如图。
)如图。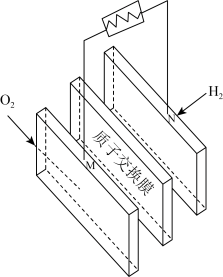
 由
由②该电池工作时,M极的电极反应式为
③与传统的发动机供能相比,氢能源供能的优点是
④每转移
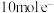 ,消耗氢气的质量为
,消耗氢气的质量为 。
。
您最近一年使用:0次
名校
解题方法
10 . 郑州宇通客车公司已经成功将氨氧燃料电池应用于新能源公交汽车中,氢氧燃料电池的反应原理如图。下列说法不正确的是
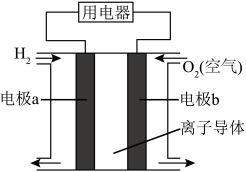
| A.该电池工作时化学能转化为电能 |
| B.该电池工作时阴离子向a极移动 |
| C.外电路中电子由电极a通过导线流向电极b |
D.若离子导体选择稀硫酸溶液,则电池正极反应方程式为 |
您最近一年使用:0次