解题方法
1 . 氧、硫及其化合物应用广泛。 可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中
可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中 在液态
在液态 中被
中被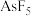 氧化成
氧化成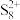 ,反应方程式为
,反应方程式为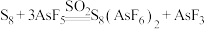 。氧能形成
。氧能形成 、
、 、
、 、
、 、
、 等重要氧化物。
等重要氧化物。 是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(
是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物( )等方法来制取。
)等方法来制取。 在
在 催化作用下与
催化作用下与 反应生成
反应生成 。下列关于化学反应的表示或说法正确的是
。下列关于化学反应的表示或说法正确的是
 可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中
可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中 在液态
在液态 中被
中被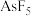 氧化成
氧化成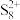 ,反应方程式为
,反应方程式为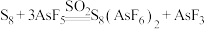 。氧能形成
。氧能形成 、
、 、
、 、
、 、
、 等重要氧化物。
等重要氧化物。 是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(
是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物( )等方法来制取。
)等方法来制取。 在
在 催化作用下与
催化作用下与 反应生成
反应生成 。下列关于化学反应的表示或说法正确的是
。下列关于化学反应的表示或说法正确的是A.碱性氢氧燃料电池的正极反应: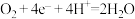 |
B. 与 与 反应: 反应: |
C. 与 与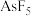 反应中,n(氧化剂):n(还原剂)=3:1 反应中,n(氧化剂):n(还原剂)=3:1 |
D.温度越高, 越大,硫酸钙制取 越大,硫酸钙制取 的反应正向进行程度越大 的反应正向进行程度越大 |
您最近半年使用:0次
名校
解题方法
2 . 下列电池工作时,属于二次电池的是
|
|
|
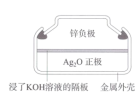
|
| A.锌锰电池 | B.氢氧燃料电池 | C.铅蓄电池 | D.锌银纽扣电池 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 下列说法正确的是
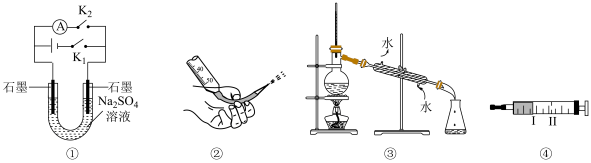
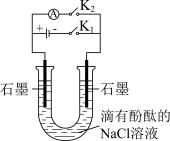
A.图①闭合 一段时间,再打开 一段时间,再打开 闭合 闭合 可制得简易燃料电池,左侧石墨为电池正极 可制得简易燃料电池,左侧石墨为电池正极 |
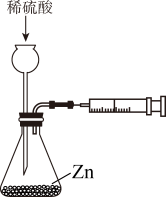
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡 溶液滴定管尖嘴内的气泡 |
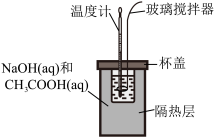
| C.图③用于分离沸点相差很小的液体混合物 |
D.图④研究压强对 平衡的影响,将活塞从Ⅰ拉到Ⅱ,气体压强减小,平衡逆向移动,颜色加深 平衡的影响,将活塞从Ⅰ拉到Ⅱ,气体压强减小,平衡逆向移动,颜色加深 |
您最近半年使用:0次
4 . 下列有关电极反应的书写中,错误的是
A.氯碱工业电解装置中,阳极的电极反应: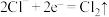 |
B.粗铜精炼时,阴极的电极反应: |
C.钢铁发生电化学腐蚀时,负极的电极反应: |
D.碱性氢氧燃料电池,正极的电极反应: |
您最近半年使用:0次
5 . 2023年,我国科技事业收获丰硕成果。下列与科技成就相关的描述正确的是
A.打造北斗卫星系统——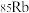 与星载铷钟所用 与星载铷钟所用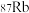 互为同位素 互为同位素 |
B.实施 海底封存—— 海底封存—— 液化时,其共价键被破坏 液化时,其共价键被破坏 |
| C.开启航运氢能时代——氢氧燃料电池工作时可将热能转化为电能 |
| D.突破量子通信技术——作为传输介质的光纤,其主要成分为晶体硅 |
您最近半年使用:0次
6 . 按要求回答问题。
(1)制作印刷电路板的过程中常用FeCl3溶液与铜反应2Fe3++Cu=2Fe2++Cu2+,把该反应设计成原电池,可用___________ 作正极材料,正极反应的电极方程式为___________ 。
(2)氢氧燃料电池的构造如图所示,由此判断OH-向___________ (填“正”或“负”)极定向移动,Y极的电极反应式为___________ 。 Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量
Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量___________ (填“增大”或“减小”)。放电过程中,外电路中转移2.5 mol e-,消耗硫酸___________ mol。
(4)某电解池装置如图所示,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则___________ 。
②Y电极上的电极反应式为___________ ,检验该电极反应产物的方法及现象是___________ 。
(1)制作印刷电路板的过程中常用FeCl3溶液与铜反应2Fe3++Cu=2Fe2++Cu2+,把该反应设计成原电池,可用
(2)氢氧燃料电池的构造如图所示,由此判断OH-向

 Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量
Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量(4)某电解池装置如图所示,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
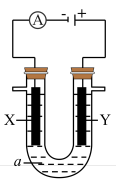
②Y电极上的电极反应式为
您最近半年使用:0次
2024-05-06更新
|
166次组卷
|
2卷引用:江苏省扬州市邗江中学2023-2024学年高一下学期三月检测化学试题
解题方法
7 . 使用下列装置进行实验,能达到实验目的的是
| A | B | C | D |
| |
|
|
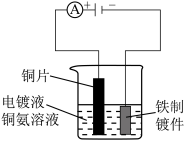
| 测定化学反应速率 | 测定中和反应反应热 | 制作简单氢氧燃料电池 | 在铁质镀件表面镀铜 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 科技创新是新质生产力的核心要素。下列说法错误的是
| A.制造C919飞机的材料——氮化硅陶瓷属于新型无机非金属材料 |
| B.开启航运氢能时代——氢氧燃料电池放电时可将热能转化为电能 |
C.打造北斗卫星系统——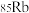 与星载铷钟所用87Rb的物理性质不同 与星载铷钟所用87Rb的物理性质不同 |
| D.突破量子通信技术——作为传输介质的光纤其主要成分为二氧化硅 |
您最近半年使用:0次
解题方法
9 . 回答下列问题。
(1)如图为氢氧燃料电池的构造示意图。________ 口通入;电池工作时, 向
向________ 极移动。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质可以传导 ,则电池工作时负极电极反应式为
,则电池工作时负极电极反应式为________ 。
(2)银锌电池总反应为: 。则负极电极反应式:
。则负极电极反应式:________ 。正极电极反应式:________ 。
(3)铅酸蓄电池反应为 。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。
。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。
①铅酸蓄电池的负极材料________ (填“Pb”或“PbO2”)极。
②放电时负极电极反应式为:________ 。充电时的阳极反应式:________________ 。
(1)如图为氢氧燃料电池的构造示意图。
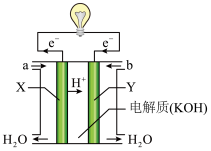
 向
向②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质可以传导
 ,则电池工作时负极电极反应式为
,则电池工作时负极电极反应式为(2)银锌电池总反应为:
 。则负极电极反应式:
。则负极电极反应式:(3)铅酸蓄电池反应为
 。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。
。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。①铅酸蓄电池的负极材料
②放电时负极电极反应式为:
您最近半年使用:0次
解题方法
10 . 回答下列问题:
(1)一定温度下,向1 L恒容密闭容器中加入1 mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2的物质的量随时间的变化如图所示。
H2(g)+I2(g),H2的物质的量随时间的变化如图所示。___________ 。
②该温度下,H2(g)+I2(g) ⇌2HI(g)的平衡常数K=___________ 。
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡___________ 移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的___________ (填字母序号),产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(3)以H2为燃料,KOH溶液为电解质溶液可制得氢氧燃料电池。该电池负极反应式为___________ 。已知2H2(g)+O2(g)=2H2O(l) ΔH=-572 kJ·mol-1.若该氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,则该电池的能量转化率为___________ 。
(1)一定温度下,向1 L恒容密闭容器中加入1 mol HI(g),发生反应2HI(g)
 H2(g)+I2(g),H2的物质的量随时间的变化如图所示。
H2(g)+I2(g),H2的物质的量随时间的变化如图所示。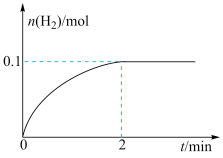
②该温度下,H2(g)+I2(g) ⇌2HI(g)的平衡常数K=
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(3)以H2为燃料,KOH溶液为电解质溶液可制得氢氧燃料电池。该电池负极反应式为
您最近半年使用:0次