名校
1 . Ⅰ.700℃时,若向2L恒容的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。

(1)0~10min 内的 CO2平均反应速率v( CO2)=___________
(2)图中A点v正___________ v逆(填“>”“<”或“=”)。
(3)下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与N2的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时消耗2a mol NO
D.N2的质量分数在混合气体中保持不变
E.混合气体的密度不随时间的变化而变化
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(4)该电池的负极反应式为___________ 。
(5)电池工作一段时间后电解质溶液的
___________ (填“增大”“减小”或“不变”)。
 C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
(1)0~10min 内的 CO2平均反应速率v( CO2)=
(2)图中A点v正
(3)下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与N2的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时消耗2a mol NO
D.N2的质量分数在混合气体中保持不变
E.混合气体的密度不随时间的变化而变化
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(4)该电池的负极反应式为
(5)电池工作一段时间后电解质溶液的

您最近一年使用:0次
名校
解题方法
2 . 化学与生活密切相关。下列叙述正确的是
| A.医用酒精中乙醇的质量分数为75% |
| B.二氧化硅是一种良好的半导体材料 |
| C.棉花、麻和蚕丝均为碳水化合物 |
| D.氢能客车中使用的电池是将化学能转化为电能 |
您最近一年使用:0次
名校
3 . 一种氢氧燃料电池以 为燃料,
为燃料, 为氧化剂,电解质溶液是质量分数为30%的KOH溶液,下列叙述正确的是
为氧化剂,电解质溶液是质量分数为30%的KOH溶液,下列叙述正确的是
 为燃料,
为燃料, 为氧化剂,电解质溶液是质量分数为30%的KOH溶液,下列叙述正确的是
为氧化剂,电解质溶液是质量分数为30%的KOH溶液,下列叙述正确的是A. 在电池负极发生还原反应 在电池负极发生还原反应 |
| B.工作一段时间后,正极区域溶液pH增大 |
| C.使用一段时间后KOH溶液质量分数仍为30% |
| D.若反应过程中有0.4 mol电子发生转移,则反应中消耗的气体体积为6.72 L |
您最近一年使用:0次
2022-07-20更新
|
314次组卷
|
2卷引用:天津市第一中学2021-2022学年高一下学期期末质量调查化学试题
4 . 一种氢氧燃料电池以 为燃料,
为燃料, 为氧化剂,电解质溶液是质量分数为30%的
为氧化剂,电解质溶液是质量分数为30%的 溶液,下列叙述正确的是
溶液,下列叙述正确的是
 为燃料,
为燃料, 为氧化剂,电解质溶液是质量分数为30%的
为氧化剂,电解质溶液是质量分数为30%的 溶液,下列叙述正确的是
溶液,下列叙述正确的是A. 在电池负极发生还原反应 在电池负极发生还原反应 |
B.使用一段时间后 溶液质量分数仍为30% 溶液质量分数仍为30% |
| C.电池的能量转化率可达100% |
D.通入 的一极做电池的正极 的一极做电池的正极 |
您最近一年使用:0次
名校
5 . 铜基催化剂催化甲醇水蒸气重整制氢是液体燃料制氢的重要方向,主要包含甲醇水蒸气重整反应、甲醇分解反应和水气变换反应,具体反应方程式如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)则
___________  。
。
(2)有利于提高甲醇平衡转化率的是___________ (填标号)。
A.增加 的用量 B.恒温恒压条件下通入Ar
的用量 B.恒温恒压条件下通入Ar
C.升高温度 D.选择更高效的催化剂 E.及时分离出
(3)一定条件下,向压强为 的恒压密闭容器中通入
的恒压密闭容器中通入 、
、 物质的量比为
物质的量比为 的混合气体,发生上述反应,达到平衡时,容器中
的混合气体,发生上述反应,达到平衡时,容器中 、
、 ,此时
,此时 的产率为
的产率为___________ ,反应Ⅱ的以分压表示的化学平衡常数 为
为___________ (用含 的代数式表示)。
的代数式表示)。
(4)液相空速表示进料速度的快慢。不同温度下,平衡时甲醇转化率和CO浓度随甲醇液相空速的变化如图所示。随温度升高,CO浓度变化的原因是___________ ,制氢产物可以用于车载燃料电池,CO含量太高会对电池产生巨大危害。甲醇水蒸气重整制氢的适宜条件是___________ ℃,___________  。
。

(5)在允许 自由迁移的固体电解质氢氧燃料电池中,
自由迁移的固体电解质氢氧燃料电池中, 放电的电极反应式为
放电的电极反应式为___________ 。
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)则

 。
。(2)有利于提高甲醇平衡转化率的是
A.增加
 的用量 B.恒温恒压条件下通入Ar
的用量 B.恒温恒压条件下通入ArC.升高温度 D.选择更高效的催化剂 E.及时分离出

(3)一定条件下,向压强为
 的恒压密闭容器中通入
的恒压密闭容器中通入 、
、 物质的量比为
物质的量比为 的混合气体,发生上述反应,达到平衡时,容器中
的混合气体,发生上述反应,达到平衡时,容器中 、
、 ,此时
,此时 的产率为
的产率为 为
为 的代数式表示)。
的代数式表示)。(4)液相空速表示进料速度的快慢。不同温度下,平衡时甲醇转化率和CO浓度随甲醇液相空速的变化如图所示。随温度升高,CO浓度变化的原因是
 。
。
(5)在允许
 自由迁移的固体电解质氢氧燃料电池中,
自由迁移的固体电解质氢氧燃料电池中, 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
2024-02-22更新
|
191次组卷
|
2卷引用:山东省济南市名校联盟2023-2024学年高三下学期开学考试化学试题
解题方法
6 . 氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上,并同时制得 和
和 溶液。相关物料的传输与转化关系如图所示:
溶液。相关物料的传输与转化关系如图所示:
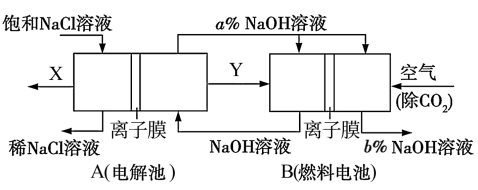
请回答下列问题:
(1)A池总反应的离子反应方程式为___________ 。燃料电池B中正极上发生的电极反应式为___________ 。
(2)装置中的离子膜是阳离子交换膜,当阴极产生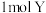 时,通过离子交换膜的
时,通过离子交换膜的 有
有___________  。
。
(3)装置图中氢氧化钠溶液质量分数的大小:
___________ 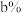 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
 和
和 溶液。相关物料的传输与转化关系如图所示:
溶液。相关物料的传输与转化关系如图所示:
请回答下列问题:
(1)A池总反应的离子反应方程式为
(2)装置中的离子膜是阳离子交换膜,当阴极产生
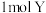 时,通过离子交换膜的
时,通过离子交换膜的 有
有 。
。(3)装置图中氢氧化钠溶液质量分数的大小:

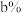 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
您最近一年使用:0次
名校
7 . 如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
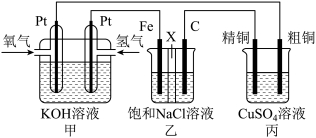
根据要求回答相关问题:
(1)通入氧气的电极为___________ (填“正极”或“负极”),负极的电极反应式为___________ 。
(2)铁电极为___________ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为___________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将___________ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为___________ ;丙装置中阴极析出铜的质量为___________ 。
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的___________ 极;该发生器中反应的总离子方程式为___________

(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
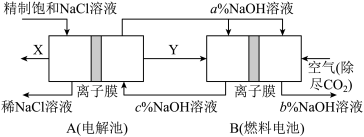
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为___________ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的

(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
名校
解题方法
8 . 氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,离子膜均为阳离子交换膜。下列说法错误的是
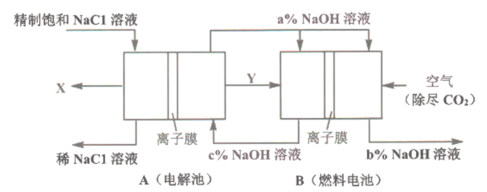

A.图中X是 ,Y是 ,Y是 |
| B.燃料电池中阳离子的移动方向:从左向右 |
| C.图中氢氧化钠溶液质量分数:b%>a%>c% |
D.电解池中每产生1mol ,理论上燃料电池中消耗 ,理论上燃料电池中消耗 的物质的量为1mol 的物质的量为1mol |
您最近一年使用:0次
2021-07-16更新
|
223次组卷
|
3卷引用:河南省开封市2020-2021学年高二下学期期末考试化学试题
名校
解题方法
9 . 如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
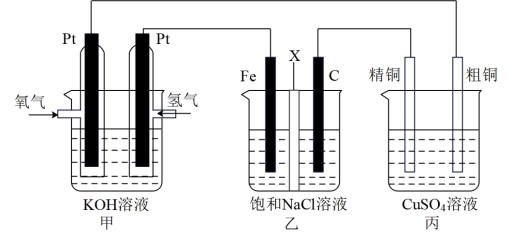
根据要求回答相关问题:
(1)通入氧气的电极为_______ (填“正极”或“负极”),
(2)铁电极为_______ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为_______ ;丙装置中阴极析出铜的质量为_______ 。
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的_______ 极;该发生器中反应的总离子方程式为_______
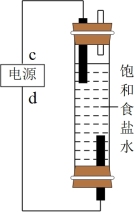
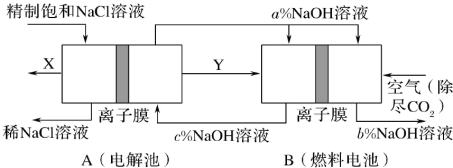
(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的

(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为

您最近一年使用:0次
解题方法
10 . 废旧碱性锌锰电池经以下工艺处理后,可实现钾、锌、锰等元素的有效回收。回答下列问题:
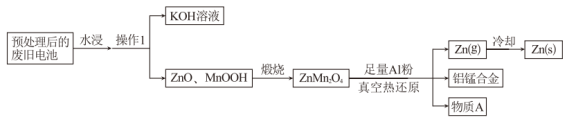
(1)“操作1”的名称为___________ 。
(2) 中
中 元素的化合价为
元素的化合价为___________ 。
(3)“煅烧”得到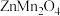 的化学方程式为
的化学方程式为___________ 。
(4)物质 的主要成分为
的主要成分为___________ (填化学式)。
(5)预处理后的废旧电池质量为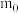 ,其中
,其中 元素的质量分数为
元素的质量分数为 ,回收得到
,回收得到 的质量为
的质量为 ,则
,则 元素的回收率为
元素的回收率为___________ (回收率 )。
)。
(6)氢氧燃料电池选用 溶液作为电解质溶液,负极的电极反应式为
溶液作为电解质溶液,负极的电极反应式为___________ 。

(1)“操作1”的名称为
(2)
 中
中 元素的化合价为
元素的化合价为(3)“煅烧”得到
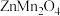 的化学方程式为
的化学方程式为(4)物质
 的主要成分为
的主要成分为(5)预处理后的废旧电池质量为
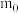 ,其中
,其中 元素的质量分数为
元素的质量分数为 ,回收得到
,回收得到 的质量为
的质量为 ,则
,则 元素的回收率为
元素的回收率为 )。
)。(6)氢氧燃料电池选用
 溶液作为电解质溶液,负极的电极反应式为
溶液作为电解质溶液,负极的电极反应式为
您最近一年使用:0次



