1 . 科学家设计了一种将苯酚(C6H5OH)氧化为CO2和H2O的原电池-电解池组合装置如图所示,已知羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。下列说法错误的是
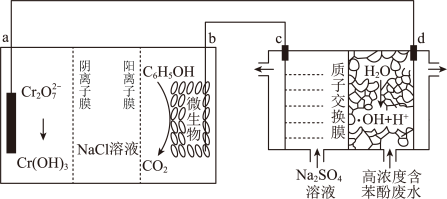

| A.高温下不利于该电池的使用 |
| B.电池工作一段时间后, NaCl溶液浓度将降低 |
| C.d电极的电极反应为:H2O-e-=·OH+H+ |
| D.相同时间内,c、d两极产生气体的体积比(相同条件下)为3:7 |
您最近一年使用:0次
名校
解题方法
2 . 某小组设计实验探究氯气的性质,装置如图所示:
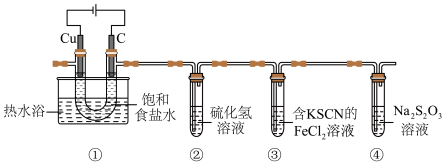
实验中观察到③中溶液先变红色,后褪色。
资料显示:④中反应为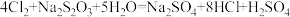
下到叙述错误的是

实验中观察到③中溶液先变红色,后褪色。
资料显示:④中反应为
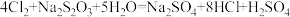
下到叙述错误的是
A.铜极附近逸出气泡,其溶液 升高 升高 |
| B.②中溶液变浑浊,可推知氯的非金属性比硫的强 |
C.取③中溶液,滴加 溶液可判断 溶液可判断 是否被氧化 是否被氧化 |
D.用硝酸酸化的 溶液可验证④中是否生成了 溶液可验证④中是否生成了 |
您最近一年使用:0次
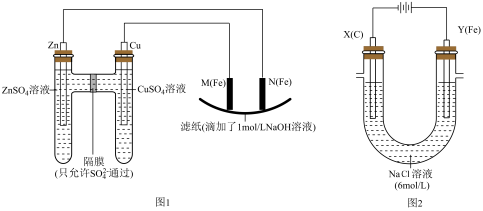
3 . 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用如图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,能替代Cu做电极的是_________ (填字母序号).
(2)M极发生反应的电极反应式为_________ ;
(3)实验过程中,SO
_________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有_________ ,写出产生此现象的反应方程式:_________ ;
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH_________ (填“增大”、“减小”或“不变”);
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O 和 4OH--4e-═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少_________ g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料, 电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为_________ 。

请回答:
Ⅰ.用如图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,能替代Cu做电极的是
| A.铝 | B.石墨 | C.镁 | D.铂 |
(3)实验过程中,SO

Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O 和 4OH--4e-═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(6)在碱性锌电池中,用高铁酸钾作为正极材料, 电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为
您最近一年使用:0次
2014高三·全国·专题练习
名校
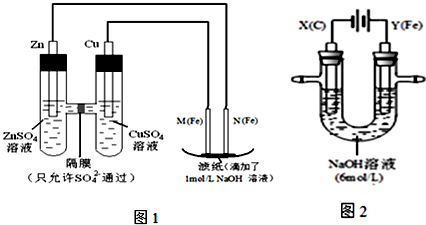
4 . 某课外小组分别用下图所示装置对原电池和电解原理进行实验探究.
请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是______ (填字母序号).
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为_____________ .
(3)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________ .
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”).
(5)电解过程中,Y极发生的电极反应为_____________ 和4OH- - 4e-= 2H2O + O2↑
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g.
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为__________ .

请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为
您最近一年使用:0次
2017-06-17更新
|
606次组卷
|
7卷引用:2014届高考化学二轮专题复习 电化学练习卷
(已下线)2014届高考化学二轮专题复习 电化学练习卷(已下线)2014高考名师推荐化学电解规律及电化学计算北京市2017届高三高考押题卷化学试题河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题2020届高考化学二轮复习大题精准训练 ——原电池、电解池填空题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题
名校
5 . 羟基自由基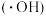 具有很强的氧化性,能将苯酚氧化为
具有很强的氧化性,能将苯酚氧化为 和
和 。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是
。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是
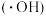 具有很强的氧化性,能将苯酚氧化为
具有很强的氧化性,能将苯酚氧化为 和
和 。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是
。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是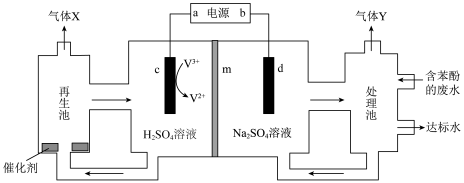
A.d电极的电极反应式: |
B.再生池中发生的反应: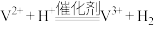 |
C.a为电源负极,m为阴离子交换膜, 能增强导电性 能增强导电性 |
D.气体X与Y在相同条件下的体积比为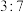 |
您最近一年使用:0次
7日内更新
|
540次组卷
|
5卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
6 . NO是人体不可缺少的“健康信使”,在心脑血管疾病的治疗中起到重要作用。但NO也是一种有毒的物质,如果在空气中含量过高,存在一定的危害。研究NO的无害化处理对治理大气污染、建设生态文明具有重要意义。请按要求回答下列问题:
(1)汽车发动机工作时会引发N2(g)+O2(g) 2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
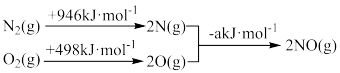
则断开1molNO中化学键所需要的能量为______ 。
(2)已知2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0.
N2(g)+2CO2(g) ΔH<0.
①在密闭容器中充入一定量CO和NO,发生反应,图甲为平衡时NO的体积分数与温度、压强的关系。
温度:T1______ T2(填“<”或“>”);若反应在D点达到平衡,此时对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的______ 点。
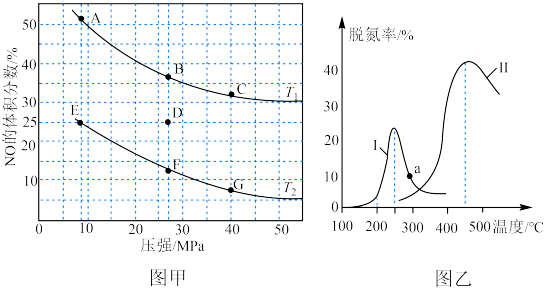
②探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如上图乙所示。曲线上a点的脱氮率______ (填“是>”、“<”或“=”)对应温度下的平衡脱氮率。催化剂Ⅱ条件下,450℃后,脱氮率随温度升高而下降的原因可能是______ ;
(3)T3K时,在刚性密闭容器中充入物质的量之比为2∶2∶1的CO、NO和N2的混合气体,起始气体总压强为P0kPa,达平衡时气体总压强为0.9P0kPa.则CO的平衡转化率为______ ,用气体分压表示KP=______ (用含有P0的代数式表示)。
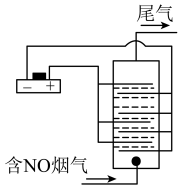
(4)以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为______ 。
(1)汽车发动机工作时会引发N2(g)+O2(g)
 2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
则断开1molNO中化学键所需要的能量为
(2)已知2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0.
N2(g)+2CO2(g) ΔH<0.①在密闭容器中充入一定量CO和NO,发生反应,图甲为平衡时NO的体积分数与温度、压强的关系。
温度:T1

②探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如上图乙所示。曲线上a点的脱氮率
(3)T3K时,在刚性密闭容器中充入物质的量之比为2∶2∶1的CO、NO和N2的混合气体,起始气体总压强为P0kPa,达平衡时气体总压强为0.9P0kPa.则CO的平衡转化率为
(4)以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为
您最近一年使用:0次
名校
7 .  具有强氧化性,工业上制备它的一种原理如图所示,其中右侧电解室内存在
具有强氧化性,工业上制备它的一种原理如图所示,其中右侧电解室内存在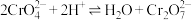 。下列说法正确的是
。下列说法正确的是

 具有强氧化性,工业上制备它的一种原理如图所示,其中右侧电解室内存在
具有强氧化性,工业上制备它的一种原理如图所示,其中右侧电解室内存在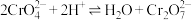 。下列说法正确的是
。下列说法正确的是
| A.电源的电极电势:a>b |
B.石墨电极上的电极反应式为 |
C.当电路中有 电子转移时,透过膜X的离子为 电子转移时,透过膜X的离子为 |
| D.铁电极上发生氧化反应 |
您最近一年使用:0次
8 . 利用某一工业钴渣(主要成分为 ,含少量
,含少量 、
、 、MgO、CuO)制备金属钴的流程如图所示:
、MgO、CuO)制备金属钴的流程如图所示:
①沉淀1为黄钠铁矾,化学式为: 。
。
②当某离子浓度 时认为沉淀完全,
时认为沉淀完全, ,
, ,
, ,
, ,
,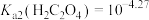
③氧化性:
(1)“浸出”过程中 元发生反应的离子方程式为
元发生反应的离子方程式为_______ ,用盐酸代替硫酸的缺点是_______ 。
(2)“浸出液”中加入 的作用是
的作用是_______ ,试剂a为_______ 。
(3)有机萃取剂用HR表示,发生萃取的反应可表示为 ,为回收
,为回收 ,可向有机相中加入一定浓度的
,可向有机相中加入一定浓度的 ,将其反萃取到水相,其原理是
,将其反萃取到水相,其原理是_______ 。
(4)沉淀2为 ,当
,当 恰好沉淀完全时,溶液中HF浓度为
恰好沉淀完全时,溶液中HF浓度为 ,则此时溶液的pH=
,则此时溶液的pH=_______ 。用 溶液沉钴,其水溶液中存在反应
溶液沉钴,其水溶液中存在反应 ,其平衡常数为K,则K=
,其平衡常数为K,则K=_______ 。
(5)已知氧化性: 。工业上采用惰性电极电解
。工业上采用惰性电极电解 溶液制取钴,不用
溶液制取钴,不用 溶液代替
溶液代替 溶液的原因是
溶液的原因是_______ 。
 ,含少量
,含少量 、
、 、MgO、CuO)制备金属钴的流程如图所示:
、MgO、CuO)制备金属钴的流程如图所示: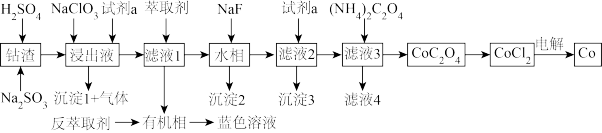
①沉淀1为黄钠铁矾,化学式为:
 。
。②当某离子浓度
 时认为沉淀完全,
时认为沉淀完全, ,
, ,
, ,
, ,
,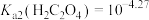
③氧化性:

(1)“浸出”过程中
 元发生反应的离子方程式为
元发生反应的离子方程式为(2)“浸出液”中加入
 的作用是
的作用是(3)有机萃取剂用HR表示,发生萃取的反应可表示为
 ,为回收
,为回收 ,可向有机相中加入一定浓度的
,可向有机相中加入一定浓度的 ,将其反萃取到水相,其原理是
,将其反萃取到水相,其原理是(4)沉淀2为
 ,当
,当 恰好沉淀完全时,溶液中HF浓度为
恰好沉淀完全时,溶液中HF浓度为 ,则此时溶液的pH=
,则此时溶液的pH= 溶液沉钴,其水溶液中存在反应
溶液沉钴,其水溶液中存在反应 ,其平衡常数为K,则K=
,其平衡常数为K,则K=(5)已知氧化性:
 。工业上采用惰性电极电解
。工业上采用惰性电极电解 溶液制取钴,不用
溶液制取钴,不用 溶液代替
溶液代替 溶液的原因是
溶液的原因是
您最近一年使用:0次
解题方法
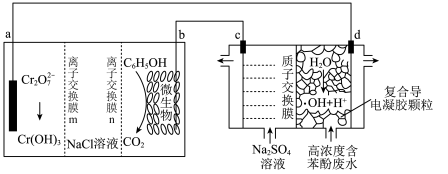
9 . 羟基自由基( )具有极强的氧化性,一种能将苯酚氧化为
)具有极强的氧化性,一种能将苯酚氧化为 和
和 的组合装置如图所示。下列说法错误的是
的组合装置如图所示。下列说法错误的是
 )具有极强的氧化性,一种能将苯酚氧化为
)具有极强的氧化性,一种能将苯酚氧化为 和
和 的组合装置如图所示。下列说法错误的是
的组合装置如图所示。下列说法错误的是
| A.离子交换膜n为阴离子交换膜 |
B.a极的电极反应式为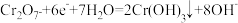 |
C.b、c两极产生气体的体积比为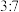 (标准状况) (标准状况) |
D.电池工作时,d极室溶液 逐渐增大 逐渐增大 |
您最近一年使用:0次
名校
10 . 三氧化二锑,又称锑白,在工业上作阻燃剂、填充剂等,用途广泛。一种利用辉锑矿粉(含 及少量
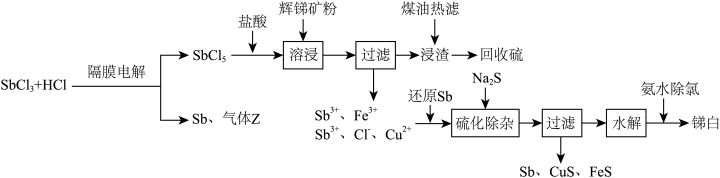
及少量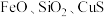 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
已知:①常温下,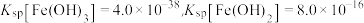 ,
, 。
。
②锑的常见价态为+3、+5价,其中 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。
(1)锑元素的原子序数为51,位于元素周期表第___________ 周期第___________ 族。
(2)溶浸时发生的主要反应的离子方程式为___________ 。
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是___________ 。
(4) 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:___________ ,锑白洗涤后便可干燥保存,检验洗净的试剂为___________ 。
(5)隔膜电解时,气体Z的分子式为___________ ;为平衡两极电荷,应使用___________ 交换膜(填“阴离子”“阳离子”或“质子”),理由是___________ 。
 及少量
及少量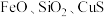 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
已知:①常温下,
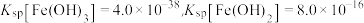 ,
, 。
。②锑的常见价态为+3、+5价,其中
 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。(1)锑元素的原子序数为51,位于元素周期表第
(2)溶浸时发生的主要反应的离子方程式为
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是
(4)
 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:(5)隔膜电解时,气体Z的分子式为
您最近一年使用:0次
2023-02-03更新
|
422次组卷
|
2卷引用:江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题



