解题方法
1 . 某锂离子电池的总反应为:FeS+2Li=Fe+Li2S。某小组以该电池为电源电解处理含Ba(OH)2废水和含Ni2+、Cl-的酸性废水,并分别获得BaCl2溶液和单质镍。电解处理的工作原理如图所示[LiPF6·SO(CH3)2为锂离子电池的电解质]。下列说法错误的是
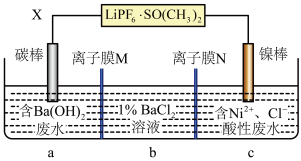
| A.X极相连的锂离子电池电极反应式为FeS+2Li++2e-=Fe+Li2S |
| B.当电路中转移1mole-时,b室离子数增加2NA个 |
| C.离子膜M为阳离子交换膜,离子膜N为阴离子交换膜 |
| D.若去掉离子膜M,将ab两室合并,则X极会产生有毒气体 |
您最近一年使用:0次
解题方法
2 . 如下所示装置,通电后石墨电极Ⅱ上有O2生成,Fe2O3逐渐溶解,下列判断正确的是
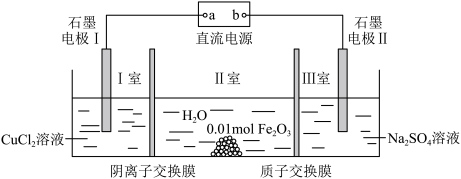
| A.b是电源的负极 |
| B.当通过质子交换膜的H+为0.12mol时,Ⅱ室内溶液质量增加超过3.32g |
| C.电解一段时间后,I室溶液的pH降低 |
| D.电解一段时间后,欲使CuCl2溶液恢复到原来浓度,需补充一定量的金属铜和氯气 |
您最近一年使用:0次
名校
解题方法
3 . 电解原理在化学工业中有着广泛的应用。如图所示装置,C、D、E、F、X、Y都是惰性电极,A、B为外接直流电源的两极。将直流电源接通后,E极附近呈红色。请回答:

(1)外接直流电源B为___________ 极。
(2)乙中F电极的电极反应式为______________________
(3)甲中开始电解时的化学反应方程式为___________ ;通电一段时间后,向甲所得溶液中加入0.1
 粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为
粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为___________ ,若将甲中产生的气体收集,共收集到标准状况下气体___________ L。
(4)现用丙装置给铜件镀银,G为___________ (填“镀件”或“镀层),当乙中溶液的 是13时(此时乙溶液体积为1000
是13时(此时乙溶液体积为1000 ),丙中镀件上析出银的质量为
),丙中镀件上析出银的质量为___________ 。

(1)外接直流电源B为
(2)乙中F电极的电极反应式为
(3)甲中开始电解时的化学反应方程式为

 粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为
粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为(4)现用丙装置给铜件镀银,G为
 是13时(此时乙溶液体积为1000
是13时(此时乙溶液体积为1000 ),丙中镀件上析出银的质量为
),丙中镀件上析出银的质量为
您最近一年使用:0次
解题方法
4 . 二氧化碳的综合利用是当下研究的重要课题。从高炉气回收 制取储氢物质
制取储氢物质 的综合利用示意图如图所示。已知该温度下,
的综合利用示意图如图所示。已知该温度下,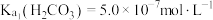 ,
, 。下列说法错误的是
。下列说法错误的是

 制取储氢物质
制取储氢物质 的综合利用示意图如图所示。已知该温度下,
的综合利用示意图如图所示。已知该温度下,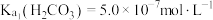 ,
, 。下列说法错误的是
。下列说法错误的是
| A.玻碳电极上发生氧化反应 |
| B.溶液中质子向铂电极方向移动 |
C.该温度下,当吸收池中溶液的 时,此时该溶液中 时,此时该溶液中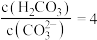 |
D.阴极反应为 、 、 |
您最近一年使用:0次
名校
5 . 设计如图装置回收金属钴,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。保持细菌所在环境pH稳定,借助细菌降解乙酸盐生成CO2,同时将废旧锂离子电池的正极材料LiCoO2(s)转化为 中。已知电极材料均为石墨材质,下列说法错误的是
中。已知电极材料均为石墨材质,下列说法错误的是

 中。已知电极材料均为石墨材质,下列说法错误的是
中。已知电极材料均为石墨材质,下列说法错误的是
| A.左侧装置为电解池,右侧装置为原电池 |
| B.装置工作时,左侧装置中H+从左室经阳膜移向甲室 |
C.左侧装置a电极反应式为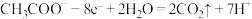 |
D.右侧装置d电极反应式为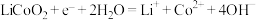 |
您最近一年使用:0次
2024-02-24更新
|
208次组卷
|
2卷引用:安徽省滁州中学2023-2024学年高二上学期期末测试化学试卷
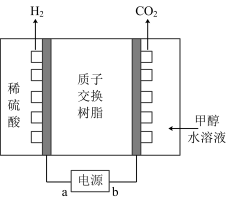
6 . 甲醇电解法制 比电解水法制
比电解水法制 的氢原子的利用率更高、电解电压更低,其工作原理如图所示。下列说法错误的是
的氢原子的利用率更高、电解电压更低,其工作原理如图所示。下列说法错误的是
 比电解水法制
比电解水法制 的氢原子的利用率更高、电解电压更低,其工作原理如图所示。下列说法错误的是
的氢原子的利用率更高、电解电压更低,其工作原理如图所示。下列说法错误的是
A.质子交换树脂只允许 通过 通过 |
| B.a极是电源的负极,它与电解池的阴极相连 |
C.每产生22.4L ,外电路中要通过6 ,外电路中要通过6 电子 电子 |
| D.参与反应的甲醇与生成的氢气的质量之比为16∶3 |
您最近一年使用:0次
名校
7 . 如图所示,回答下列问题:

(1)此装置的名称是___________ 。
(2)氯化钠溶液中离子有___________ ,其中,定向移动至阴极附近的离子有___________ 。
(3)阳极附近的产物是___________ ,检验该物质的方法是___________ 。
(4)电解饱和食盐水的化学方程式___________ ,工业上,利用电解饱和食盐水可制得多种产品,如有___________ 。(如举两例)

(1)此装置的名称是
(2)氯化钠溶液中离子有
(3)阳极附近的产物是
(4)电解饱和食盐水的化学方程式
您最近一年使用:0次
名校
8 . 下列叙述不正确的是
| A.电解稀硫酸溶液,实质上是电解水,故溶液的pH不变 |
| B.原电池的正极和电解池的阴极所发生的反应都是还原反应 |
| C.电解精炼铜时粗铜作阳极、精铜作阴极、溶液中含有铜离子 |
| D.在铁制品上镀锌的方案设计是锌作阳极、镀件作阴极、溶液中含有锌离子 |
您最近一年使用:0次
名校
9 . 双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内层为水层,装置工作时水层中的H2O解离成H+和OH-,分别向两侧发生迁移。CO2电化学还原法制备甲醇的电解原理如图所示。该装置工作时,下列说法正确的是
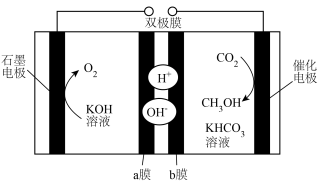

| A.催化电极上发生氧化反应 |
| B.石墨电极区溶液pH不变 |
| C.H+穿过b膜进入右室溶液 |
D.电解一段时间后,右室HCO 的物质的量减少 的物质的量减少 |
您最近一年使用:0次
2023-08-15更新
|
564次组卷
|
3卷引用:安徽省合肥市第一中学2023-2024学年高二上学期期末考试化学试题
安徽省合肥市第一中学2023-2024学年高二上学期期末考试化学试题河北省保定市定州中学2023届高三下学期模拟考试化学试题(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
10 . 电化学原理在现代工业中应用广泛,回答下列问题:
(1)氯碱工业上利用电解精制饱和食盐水的方法制取氯气、氯气、烧碱和氯的含氧酸盐等一系列化工产品,如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
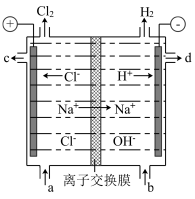
①离子交换膜的作用为___________ 、___________ 。
②氯氧化钠溶液从图中___________ (填“a”“b”“c”或“d”)处收集。
(2) 可作超级电容器材料。用惰性电极电解
可作超级电容器材料。用惰性电极电解 溶液制得
溶液制得 ,其阳极的电极反应式为
,其阳极的电极反应式为___________ 。
(3)金属镍有广泛的用途,粗镍中含有少量的Fe、Zn、Cu、Pt等杂质,故可用电解法制备高纯度的镍。(金属活动性: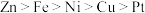 )
)
①电解过程中,阳极杂质的电极反应式为___________ 。
②电解过程中,阳极减少的质量与阴极增加的质量___________ (填“相等”或“不相等”),电解结束后,Pt以___________ 形式存在。
(4)图甲是一种将废水中的氯乙烯(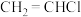 )进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
)进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
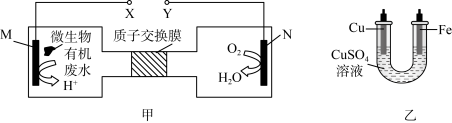
①M为___________ (填“正极”“负极”“阴极”或“阳极”),镀铜时,___________ (填“X”或“Y”)与铁电极相连,工作过程中,N极区域溶液中pH将___________ (填“增大”“减小”或“不变”)。
②若M极消耗0.1mol氯乙烯,则铁电极增重___________ g,硫酸铜溶液的浓度将___________ (填“增大”“减小”或“不变”)。
(1)氯碱工业上利用电解精制饱和食盐水的方法制取氯气、氯气、烧碱和氯的含氧酸盐等一系列化工产品,如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

①离子交换膜的作用为
②氯氧化钠溶液从图中
(2)
 可作超级电容器材料。用惰性电极电解
可作超级电容器材料。用惰性电极电解 溶液制得
溶液制得 ,其阳极的电极反应式为
,其阳极的电极反应式为(3)金属镍有广泛的用途,粗镍中含有少量的Fe、Zn、Cu、Pt等杂质,故可用电解法制备高纯度的镍。(金属活动性:
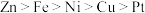 )
)①电解过程中,阳极杂质的电极反应式为
②电解过程中,阳极减少的质量与阴极增加的质量
(4)图甲是一种将废水中的氯乙烯(
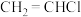 )进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
)进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
①M为
②若M极消耗0.1mol氯乙烯,则铁电极增重
您最近一年使用:0次
2023-08-08更新
|
382次组卷
|
2卷引用:安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题



