名校
解题方法
1 . 处理工业酸性废水中 的电解池工作原理如图所示,电解总反应为
的电解池工作原理如图所示,电解总反应为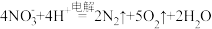 。下列说法正确的是
。下列说法正确的是

 的电解池工作原理如图所示,电解总反应为
的电解池工作原理如图所示,电解总反应为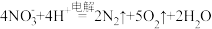 。下列说法正确的是
。下列说法正确的是
| A.X电极上发生还原反应 |
| B.电解池工作时,电路中每通过2mol电子,生成15.68L气体 |
| C.电解池工作时,H+从质子交换膜右侧向左侧移动 |
D.Y电极上发生的电极反应为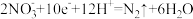 |
您最近一年使用:0次
名校
解题方法
2 . 有关电解池的应用,下列叙述错误的是
| A.使用阳离子交换膜工业电解饱和食盐水时,阴极区获得烧碱溶液和氧气 |
B.电解精炼铜时外电路通过 ,阳极质量减少64g ,阳极质量减少64g |
| C.以硫酸铜溶液为电镀液,在铁件上镀铜的过程中,硫酸铜溶液的浓度保持不变 |
D.工业上用石墨电极电解熔融 冶炼铝时,阳极因被氧气氧化需定期更换 冶炼铝时,阳极因被氧气氧化需定期更换 |
您最近一年使用:0次
名校
解题方法
3 . 利用如图所示装置模拟电解在工业生产的应用,下列说法正确的是
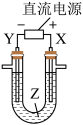

A.若要在铁片上镀铜,Z为 溶液 溶液 |
| B.若要在铁片上镀铜,X、Y分别为纯铜和铁片 |
C.若Z是饱和 溶液,电解一段时间后,Y电极析出少量的 溶液,电解一段时间后,Y电极析出少量的 |
D.若Z是饱和 溶液,X电极首先发生的电极反应式是: 溶液,X电极首先发生的电极反应式是: |
您最近一年使用:0次
名校
4 . 硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解槽中水溶液的主要成分及反应过程如图所示。下列说法正确的是


| A.惰性电极2为阴极 |
B.反应前后 保持不变 保持不变 |
C.外电路通过1 mol电子,可得到1 mol |
| D.该合成方法中的能量转换形式是化学能全部转化为电能 |
您最近一年使用:0次
2024-02-11更新
|
91次组卷
|
2卷引用:天津市南开区2023-2024学年高二上学期期末测试化学试题
5 . 氯气是一种重要的工业原料,在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新工艺方案,如图所示。下列说法不正确的是
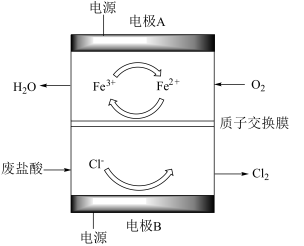

| A.电极B与外接电源的正极相连 |
B.负极区仅发生反应: |
C.电解时,总的电解方程式可以写为 |
D.电路中转移 时,理论上需消耗氧气 时,理论上需消耗氧气 (标准状况) (标准状况) |
您最近一年使用:0次
6 . Ⅰ.次磷酸 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。
(1) 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:___________ 。
(2)用电渗析法制备 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
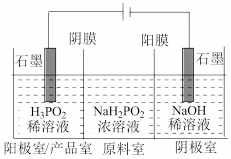
①写出阴极的电极反应:___________ 。
② 的移动方向是:
的移动方向是: 移向
移向___________ (填“阴极室”或“原料室”)。
③阳极室得到 ,
, 的浓度逐渐增大。
的浓度逐渐增大。
a.结合电极反应说明其原因是___________ 。
b.该方法得到的产品 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是___________ 。
Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时, 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,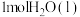 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(4)氢氧燃料电池中氢气在___________ (填“正”或“负”)极发生反应。
(5)在允许 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,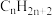 放电的电极反应式为
放电的电极反应式为___________ 。
(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→___________ (用b~j等代号表示)。

 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。(1)
 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:(2)用电渗析法制备
 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
①写出阴极的电极反应:
②
 的移动方向是:
的移动方向是: 移向
移向③阳极室得到
 ,
, 的浓度逐渐增大。
的浓度逐渐增大。a.结合电极反应说明其原因是
b.该方法得到的产品
 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时,
 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,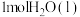 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(4)氢氧燃料电池中氢气在
(5)在允许
 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,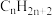 放电的电极反应式为
放电的电极反应式为(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→

您最近一年使用:0次
解题方法
7 . 如图是模拟铁制品镀铜工艺的装置,下列说法不正确 的是


| A.a电极为铜 | B.b电极上发生还原反应 |
C.电解质溶液可以是 溶液 溶液 | D.电镀过程中,溶液中 浓度不断减小 浓度不断减小 |
您最近一年使用:0次
名校
解题方法
8 . 电化学在现代生活、生产和科学技术的发展中发挥着越来越重要的作用。
(1)Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4。
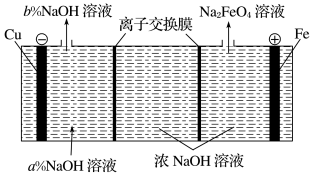
①阳极的电极反应式为_______ 。
②右侧的离子交换膜为_______ (填“阴”或“阳”)离子交换膜,阴极区a%_______ b%(填“>”“═”或“<”)。
③阴极产生的气体为_______ 。
(2)SO2和NOx是主要大气污染物,如图是同时吸收SO2和NOx的示意图。
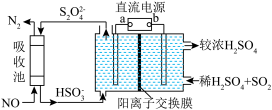
①b是直流电源的_______ 。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为_______ 。
③当NOx均为NO时,吸收池中发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(3)某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl。

①当电路中转移amole-时,交换膜左侧溶液中约减少_______ mol离子。交换膜右侧溶液中c(HCl)________ (填“>”“<”或“═”)1mol•L-1(忽略溶液体积变化)。
②若质子交换膜换成阴离子交换膜,其他不变。若有11.2L氯气(标准状况)参与反应,则必有_______ mol离子通过交换膜向_______ 侧迁移。(填“左”、“右”)
(1)Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4。

①阳极的电极反应式为
②右侧的离子交换膜为
③阴极产生的气体为
(2)SO2和NOx是主要大气污染物,如图是同时吸收SO2和NOx的示意图。

①b是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③当NOx均为NO时,吸收池中发生反应的氧化剂与还原剂的物质的量之比为
(3)某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl。

①当电路中转移amole-时,交换膜左侧溶液中约减少
②若质子交换膜换成阴离子交换膜,其他不变。若有11.2L氯气(标准状况)参与反应,则必有
您最近一年使用:0次
名校
解题方法
9 . 我国提出争取在2030年前实现碳达峰、2060年实现碳中和,这对于改善环境、实现绿色发展至关重要。在铜基配合物的催化作用下,利用电化学原理可将CO2还原为碳基燃料(包括烷烃和羧酸等),其装置原理如图所示。下列叙述不正确的是


| A.该装置工作时,H+穿过质子交换膜从左向右移动 |
| B.图中石墨烯为阴极,电极反应式为CO2+2H++2e-═HCOOH |
| C.每转移2mol电子,阴极室电解质溶液质量增加44g |
| D.该装置工作过程中,图中Pt电极附近溶液的pH减小 |
您最近一年使用:0次
名校
解题方法
10 . 钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法不正确的是
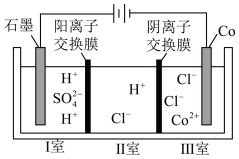

| A.工作时,Ⅰ室和Ⅱ室溶液的pH均增大 |
B.电解总反应:2Co2++2H2O 2Co+O2↑+4H+ 2Co+O2↑+4H+ |
| C.移除两交换膜后,石墨电极上发生的反应会发生变化 |
| D.生成2molCo,Ⅰ室溶液质量理论上减少36g |
您最近一年使用:0次



