解题方法
1 . 如图是原电池电解池的组合装置图。
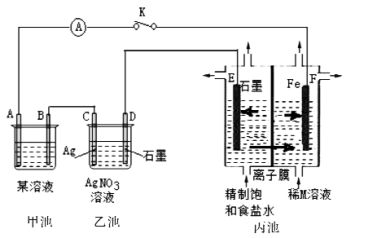
请回答:
(1)若甲池某溶液为稀H2SO4,闭合K时,电流表指针发生偏转,电极材料A为Fe,B为碳棒。则:
①甲池为______ (填“原电池”或“电解池”);B电极上发生的现象为______ 。
②乙池中的银电极上的电极反应式为______ 。
③丙池中E电极为______ (填“正极”、“负极”、“阴极”或“阳极”);闭合K一段时间后,稀M溶液的浓度会增加,则M溶液中的溶质是______ (填化学式);丙池中的离子膜为______ (填“阳离子交换膜”或“阴离子交换膜”)
(2)若将甲池的某溶液改为FeCl3,电极材料A为Cu、B为碳棒,则甲池的总反应的离子方程式为______ 。
(3)若甲池为氢氧燃料电池,某溶液为KOH溶液,A极通入氢气。则:
①A电极的反应方程式为______ 。
②若线路中转移0.02mol电子,乙池中D极质量变化______ g。
③二氧化氯(ClO2)为黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出也能用丙池装置制取二氧化氯。写出生成二氧化氯的电极反应式为______ 。

请回答:
(1)若甲池某溶液为稀H2SO4,闭合K时,电流表指针发生偏转,电极材料A为Fe,B为碳棒。则:
①甲池为
②乙池中的银电极上的电极反应式为
③丙池中E电极为
(2)若将甲池的某溶液改为FeCl3,电极材料A为Cu、B为碳棒,则甲池的总反应的离子方程式为
(3)若甲池为氢氧燃料电池,某溶液为KOH溶液,A极通入氢气。则:
①A电极的反应方程式为
②若线路中转移0.02mol电子,乙池中D极质量变化
③二氧化氯(ClO2)为黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出也能用丙池装置制取二氧化氯。写出生成二氧化氯的电极反应式为
您最近一年使用:0次
2021-01-28更新
|
297次组卷
|
2卷引用:安徽省滁州市定远县育才学校2021-2022学年高二(普通班)下学期开学摸底考试化学试题
名校
2 . 甲、乙两池电极材料都是铁棒与碳棒(如图)。请回答下列问题:
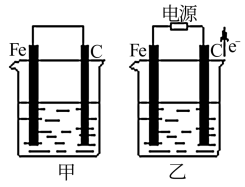
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的_______ 棒;乙池中的_______ 棒。
②在甲池中碳棒这极的电极反应是_______ ,在乙池中阳极的电极反应是_______ 。
(2)若两池中均盛放饱和NaCl溶液。
①乙池中铁棒是_______ 极,写出乙池中总反应的离子方程式:_______ 。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去。这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸。该反应的化学方程式为_______ 。
(3)如下图为相互串联的甲、乙两个电解池(电极都是惰性电极),请回答:
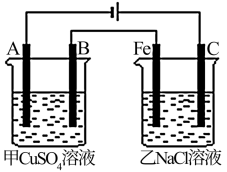
①写出甲电解池中的电解反应方程式:_______ 。
②若甲槽阴极增重19.2g,则乙槽阳极放出气体在标准状况下的体积为_______ ;若乙槽剩余液体为400 mL,则电解后得到碱液的物质的量浓度为_______ 。

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的
②在甲池中碳棒这极的电极反应是
(2)若两池中均盛放饱和NaCl溶液。
①乙池中铁棒是
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去。这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸。该反应的化学方程式为
(3)如下图为相互串联的甲、乙两个电解池(电极都是惰性电极),请回答:

①写出甲电解池中的电解反应方程式:
②若甲槽阴极增重19.2g,则乙槽阳极放出气体在标准状况下的体积为
您最近一年使用:0次
3 . 下图为某实验小组设计的利用氢氧燃料电池电解饱和食盐水的装置示意图。已知甲、乙、丙均为气体。回答下列问题:
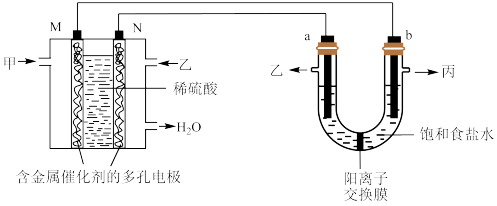
(1)甲为_________________ (写化学式),该电极反应式为______________________________________________________ 。
(2)电解饱和食盐水的离子方程式为________________________________________ 。
(3)装置工作时,若生成2mol丙,则燃料电池中消耗乙为______ L(标准状况下)。
(4)假定装入的饱和食盐水为50mL(电解前后溶液体积变化可忽略),当测得的气体丙为5.6mL(标准状况下,忽略气体的溶解)时,则所得溶液中c(NaOH)=__________ 。

(1)甲为
(2)电解饱和食盐水的离子方程式为
(3)装置工作时,若生成2mol丙,则燃料电池中消耗乙为
(4)假定装入的饱和食盐水为50mL(电解前后溶液体积变化可忽略),当测得的气体丙为5.6mL(标准状况下,忽略气体的溶解)时,则所得溶液中c(NaOH)=
您最近一年使用:0次
解题方法
4 . I.氮和氮的化合物在国防、工农业生产和生活中都有极其广泛的用途。请回答下列问题:
(1)亚硝酰氯(结构式为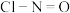 )是有机合成中的重要试剂,它可由
)是有机合成中的重要试剂,它可由 和
和 在常温常压条件下反应制得,反应方程式为:
在常温常压条件下反应制得,反应方程式为: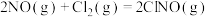 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:
则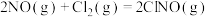

________  。
。
(2)在一个恒容密闭容器中充入 和
和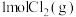 发生(1)中的反应,在温度分别为
发生(1)中的反应,在温度分别为 ℃、
℃、 ℃时测得
℃时测得 的物质的量(单位:mol)与时间的关系如下表所示:
的物质的量(单位:mol)与时间的关系如下表所示:
①
________  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
②温度为 时,起始时容器内的压强为
时,起始时容器内的压强为 ,则该反应的平衡常数
,则该反应的平衡常数
________ (用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)(化为最简式)。
物质的量分数)(化为最简式)。
(3)近年来,地下水中的氮污染已成为世界性的环境问题。在金属 、
、 和依(
和依( )的催化作用下,
)的催化作用下, 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),其工作原理如图所示。
),其工作原理如图所示。
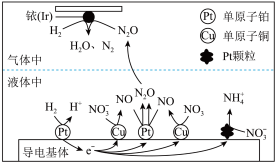
① 表面发生反应的化学方程式为:
表面发生反应的化学方程式为:________ 。
②若导电基体上的 颗粒增多,造成的后果是
颗粒增多,造成的后果是________ 。
Ⅱ.利用电化学原理,将 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
制成燃料电池,模拟工业电解法精炼银,装置如下图所示。

(4)①甲池工作时, 转变成绿色硝化剂
转变成绿色硝化剂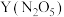 ,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为
,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为________ 。
②若用10A的电流电解50min后,乙中阴极得到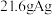 ,则该电解池的电解效率为
,则该电解池的电解效率为________ %。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为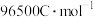 )
)
(1)亚硝酰氯(结构式为
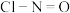 )是有机合成中的重要试剂,它可由
)是有机合成中的重要试剂,它可由 和
和 在常温常压条件下反应制得,反应方程式为:
在常温常压条件下反应制得,反应方程式为: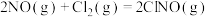 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:| 化学键 |  |  | 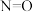 |  |
键能 | 243 | 200 | 607 | 630 |
则
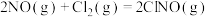

 。
。(2)在一个恒容密闭容器中充入
 和
和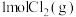 发生(1)中的反应,在温度分别为
发生(1)中的反应,在温度分别为 ℃、
℃、 ℃时测得
℃时测得 的物质的量(单位:mol)与时间的关系如下表所示:
的物质的量(单位:mol)与时间的关系如下表所示:t/min 温度  | 0 | 5 | 8 | 13 |
 | 2 | 1.5 | 1.3 | 1.0 |
 | 2 | 1.15 | 1.0 | 1.0 |
①

 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。②温度为
 时,起始时容器内的压强为
时,起始时容器内的压强为 ,则该反应的平衡常数
,则该反应的平衡常数
 总压
总压 物质的量分数)(化为最简式)。
物质的量分数)(化为最简式)。(3)近年来,地下水中的氮污染已成为世界性的环境问题。在金属
 、
、 和依(
和依( )的催化作用下,
)的催化作用下, 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),其工作原理如图所示。
),其工作原理如图所示。
①
 表面发生反应的化学方程式为:
表面发生反应的化学方程式为:②若导电基体上的
 颗粒增多,造成的后果是
颗粒增多,造成的后果是Ⅱ.利用电化学原理,将
 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
(4)①甲池工作时,
 转变成绿色硝化剂
转变成绿色硝化剂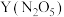 ,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为
,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为②若用10A的电流电解50min后,乙中阴极得到
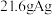 ,则该电解池的电解效率为
,则该电解池的电解效率为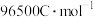 )
)
您最近一年使用:0次
名校
解题方法
5 . 如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:
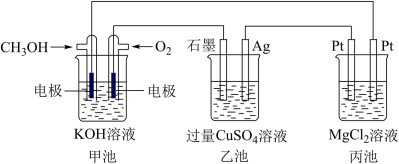
(1)甲池燃料电池的负极反应为__ 。
(2)写出乙池中电解总反应的化学方程式:__ 。
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生__ g沉淀,此时乙池中溶液的体积为400mL,该溶液的pH=__ 。
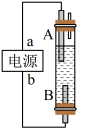
(4)某同学利用甲醇燃料电池设计电解法制取消毒液或Fe(OH)2 的实验装置(如图)。若用于制消毒液,a为电池的__ 极,电解质溶液最好用__ 。若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用__ 作电极。

(1)甲池燃料电池的负极反应为
(2)写出乙池中电解总反应的化学方程式:
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生
(4)某同学利用甲醇燃料电池设计电解法制取消毒液或Fe(OH)2 的实验装置(如图)。若用于制消毒液,a为电池的

您最近一年使用:0次
2020-01-18更新
|
219次组卷
|
10卷引用:安徽省亳州市涡阳县育翠高级中学2019-2020高二上学期第二次月考化学试题
安徽省亳州市涡阳县育翠高级中学2019-2020高二上学期第二次月考化学试题湖北省黄冈市2017-2018学年高二上学期期末考试化学试题四川省宜宾市第四中学2018-2019学年高二上学期期末模拟理科综合化学试题【全国百强校】四川省棠湖中学2018-2019学年高二下学期开学考试化学试题四川省武胜县烈面中学校2018届高三9月入学考试化学试题江西省南昌市第十中学2019-2020学年高二上学期期末考试化学试题(已下线)【南昌新东方】2019 南昌市三校(一中、十中、铁一中)高二上 期末(已下线)第四章 化学反应与电能(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)江西省南昌市八一中学、洪都中学等七校2020-2021学年高二上学期期末联考化学试题江西省宜春市万载中学2021-2022学年高二上学期第三次月考化学试题
解题方法
6 . 如图所示,X是一种生活中常见的金属元素,A、B、C、D为石墨电极,E、F分别为短周期相邻两种活泼金属中的一种,且E能与NaOH溶液反应。按图示接通线路,反应一段 时间(实验中所有溶液均足量)。
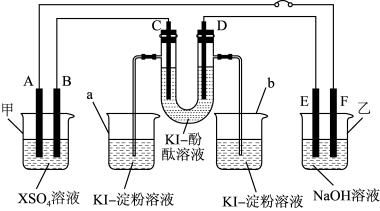
(1)甲池是___ (填“原电池”或“电解池”,下同)装置;乙池是___ 装置。
(2)D极为___ (填“阴极”或“阳极”)。
(3)烧杯中溶液会变蓝的是____ (填“a”或“b”);C极上的电极反应式为___________________________ 。
(4)F极上的电极反应式为:_________________________________________________ 。
(5)当电路中通过0.02mol电子时,B电极上沉积0.64g金属X,则X为___ (填元素符号),甲池中反应的化学方程式为______________________________________________________ 。

(1)甲池是
(2)D极为
(3)烧杯中溶液会变蓝的是
(4)F极上的电极反应式为:
(5)当电路中通过0.02mol电子时,B电极上沉积0.64g金属X,则X为
您最近一年使用:0次
2020-01-01更新
|
112次组卷
|
2卷引用:安徽省枞阳县浮山中学2019-2020学年高二上学期期中考试化学试题
名校
7 . 某课外活动小组用如图所示装置进行实验,请回答下列问题:
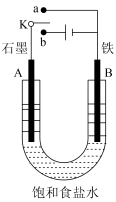
(1)若开始实验时开关K与a连接,则B极的电极反应式为_________ 。
(2)若开始实验时开关K与b连接,则下列说法正确的是_____ (填序号)。
①溶液中Na+向A极移动
②从A极逸出的气体能使湿润的淀粉KI试纸变蓝
③反应一段时间后向电解液中加适量盐酸可使其恢复到电解前的浓度
(3)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
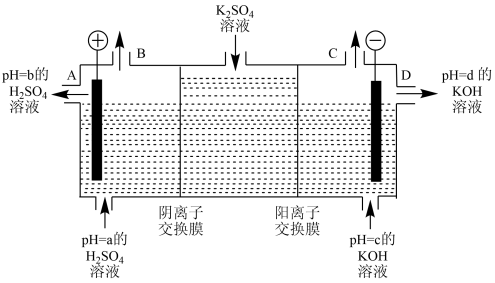
①该电解槽的阳极反应式为_________ ,通过阴离子交换膜的离子数____ (填“>”“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为____ ;
③电解一段时间后,B口与C口产生气体的质量比为___ 。

(1)若开始实验时开关K与a连接,则B极的电极反应式为
(2)若开始实验时开关K与b连接,则下列说法正确的是
①溶液中Na+向A极移动
②从A极逸出的气体能使湿润的淀粉KI试纸变蓝
③反应一段时间后向电解液中加适量盐酸可使其恢复到电解前的浓度
(3)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。

①该电解槽的阳极反应式为
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为
③电解一段时间后,B口与C口产生气体的质量比为
您最近一年使用:0次
2019-11-18更新
|
178次组卷
|
3卷引用:安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题
名校
解题方法
8 . (1)某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞 (如图1)。
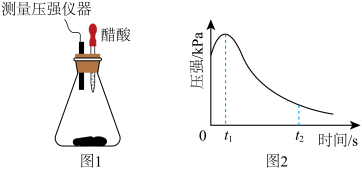
从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了____________ 腐蚀,此时,碳粉表面发生的电极反应式是____________ 。
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确 的是______ 。
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)电动车采用了一种高效耐用的新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①该电池放电时负极电极反应式为_________ ;
②充电时阳极电极反应式为_______ 。
(4)下列描述中,符合生产实际的是( )
A. 电解食盐水制得金属钠 B. 电解熔融氯化铝制取金属铝,用石墨作阳极
C. 一氧化碳高温还原铁矿石制得铁 D.电解熔融氧化镁制取金属镁,用铁作阳极
(5)金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A.阴极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt

从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)电动车采用了一种高效耐用的新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①该电池放电时负极电极反应式为
②充电时阳极电极反应式为
(4)下列描述中,符合生产实际的是
A. 电解食盐水制得金属钠 B. 电解熔融氯化铝制取金属铝,用石墨作阳极
C. 一氧化碳高温还原铁矿石制得铁 D.电解熔融氧化镁制取金属镁,用铁作阳极
(5)金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阴极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
您最近一年使用:0次
2019-11-14更新
|
243次组卷
|
2卷引用:安徽省蚌埠市第二中学2019-2020学年高二上学期期中考试化学试题
名校
解题方法
9 . 以食盐为原料进行生产并综合利用的某些过程如图。

(1) 除去粗盐中的微溶物质CaSO4通常用Na2CO3处理,请用平衡移动原理解释说明:_____________ 。
(2) 人们习惯上把电解饱和食盐水的工业叫做氯碱工业.图1表示电解饱和NaCl 溶液的装置,X、Y是石墨棒。实验开始后,检验Y 电极反应产物的方法是_________________ 。

(3) 若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的气体,其化学式是__________ 。
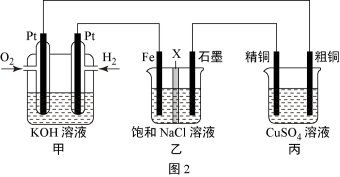
(4) 某同学设计一个燃料电池(如图2所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。根据要求回答相关问题:
①通入氢气电极的反应式为__________________ 。
②反应一段时间后,在乙装置中滴入酚酞溶液,______________ (填“铁”或“石墨”)极区的溶液先变红。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将___________ (填“增大”“减小”或“不变”)。
④若在标准状况下有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为_________ L。

(1) 除去粗盐中的微溶物质CaSO4通常用Na2CO3处理,请用平衡移动原理解释说明:
(2) 人们习惯上把电解饱和食盐水的工业叫做氯碱工业.图1表示电解饱和NaCl 溶液的装置,X、Y是石墨棒。实验开始后,检验Y 电极反应产物的方法是


(3) 若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的气体,其化学式是
(4) 某同学设计一个燃料电池(如图2所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。根据要求回答相关问题:
①通入氢气电极的反应式为
②反应一段时间后,在乙装置中滴入酚酞溶液,
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将
④若在标准状况下有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为
您最近一年使用:0次
11-12高二上·浙江绍兴·期中
名校
解题方法
10 . 如右图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为_____ 极,A极的电极反应式为_______________ 。若所盛溶液为KCl溶液:则B极的电极反应式为________________ , K+移向___ 极(填A、B)
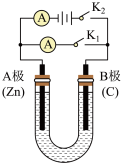
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:①A电极附近可观察到的现象是_________________________ 。
②B电极上的电极反应式为________________ ,总反应化学方程式是_______________________________________ 。
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为_________ 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的___________ 。
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是_______ ,电极反应式是____________________ ,反应一段时间后电解质溶液中Cu2+浓度______ (填“增大”、“减小”、“不变”)。
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为

(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:①A电极附近可观察到的现象是
②B电极上的电极反应式为
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是
您最近一年使用:0次
2016-12-09更新
|
525次组卷
|
4卷引用:安徽省阜阳市临泉县第一中学2016-2017学年高二下学期学科竞赛化学试题
安徽省阜阳市临泉县第一中学2016-2017学年高二下学期学科竞赛化学试题(已下线)2011-2012学年浙江省诸暨中学高二上学期期中考试化学(理)试卷湖北省宜昌市部分示范高中教学协作体2016-2017学年高二下学期期中考试化学试题湖北省宜昌市示范高中协作体2016-2017学年高二下学期期中考试化学试题



