名校
1 . 采用电化学方法使Fe2+与H2O2反应,可生成非常活泼的·OH(羟基自由基)中间体用于降解废水中的有机污染物,原理如下图所示。下列说法不正确 的是
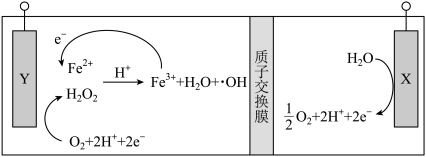

| A.采用电化学方法时将电能转化为化学能 |
| B.可将X电极上产生的O2收集起来,输送到Y电极继续使用 |
| C.根据装置推测,Y电极是阳极,·OH在该电极侧产生 |
| D.起始时,在Y电极附近加入适量Fe2+或Fe3+,均能让装置正常工作 |
您最近一年使用:0次
2021-11-10更新
|
369次组卷
|
6卷引用:专题4.2.2 电解原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)
(已下线)专题4.2.2 电解原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)山东省实验中学2021-2022学年高二上学期期中化学试题河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题山东省新泰市第一中学2022-2023学年高二上学期期中考试化学试题山东省济南第十一中学2022-2023学年高二上学期期中考试化学试题山东省泰安新泰市第一中学(实验部)2023-2024学年高二上学期第一次质量检测化学试题
解题方法
2 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池为_______ (填“原电池”或“电解池”),A电极的电极反应式为_______ 。
(2)丙池中E电极为_______ (填“正极”、“负极”、“阴极”或“阳极”),丙池总反应的离子方程式为_______ 。
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的物质的量为_______ mol
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______(填选项字母)。
(5)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
此装置中爱迪生蓄电池的正极是_______ (填“a”或“b”),该电池工作一段时间后必须充电,充电时阴极的电极反应式为_______ 。


(1)甲池为
(2)丙池中E电极为
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的物质的量为
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______(填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
 Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。此装置中爱迪生蓄电池的正极是

您最近一年使用:0次
解题方法
3 . 某油脂厂废弃的油脂加氢所用催化剂主要含金属Ni、Al、Fe及他们的氧化物,还有少量其他不溶性物质。采用如图工艺流程回收其中的镍来制备硫酸镍晶体(NiSO4·7H2O):
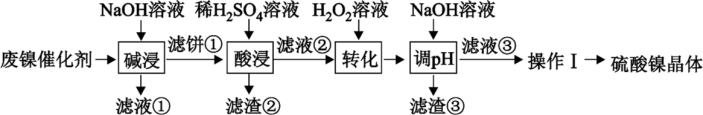
溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
(1)废弃催化剂上的油脂在_______ 过程中被处理
(2)滤液①中含有的无机阴离子除OH-离子外还有_______ 。
(3)“转化”过程的离子方程式_______ ;“转化”过程宜控制较低温度的原因是_______ 。
(4)加NaOH溶液“调pH”应控制的pH范围是_______ 。
(5)操作I为_______ 、_______ 、过滤、洗涤、干燥,得到产品。
(6)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。某手机镍氢电池总反应为NiOOH+MH M+Ni(OH)2(M为储氢金属或合金),则放电时,正极反应式为
M+Ni(OH)2(M为储氢金属或合金),则放电时,正极反应式为_______ 。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH | 6.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(2)滤液①中含有的无机阴离子除OH-离子外还有
(3)“转化”过程的离子方程式
(4)加NaOH溶液“调pH”应控制的pH范围是
(5)操作I为
(6)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
 M+Ni(OH)2(M为储氢金属或合金),则放电时,正极反应式为
M+Ni(OH)2(M为储氢金属或合金),则放电时,正极反应式为
您最近一年使用:0次
2021·全国·模拟预测
名校
解题方法
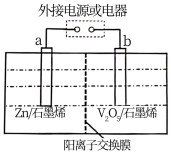
4 . 一种锌钒电池的工作原理如图所示,电解质为ZnSO4溶液,电池反应式为:Zn+ V2O5 ZnV2O5。下列说法错误的是
ZnV2O5。下列说法错误的是
 ZnV2O5。下列说法错误的是
ZnV2O5。下列说法错误的是
| A.放电时,b电极的反应式:Zn2++V2O5 + 2e-=ZnV2O5 |
| B.放电时,Zn2+从a电极区向b电极区迁移 |
| C.充电时,b电极与电源负极相连 |
| D.充电时,若转移0.4 mol 电子,理论上a电极增重13 g |
您最近一年使用:0次
2021-09-30更新
|
825次组卷
|
6卷引用:高中化学《新教材变化解读与考法剖析》第四章 化学反应与电能(人教版2019选择性必修1)
(已下线)高中化学《新教材变化解读与考法剖析》第四章 化学反应与电能(人教版2019选择性必修1)(已下线)第7周 周测卷-备战2022年高考化学周测与晚练(新高考专用)黑龙江省哈尔滨市第三中学2021-2022学年高二上学期10月阶段性测试化学试题福建省永安市第三中学高中校2021-2022学年高二上学期10月月考化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】13广东省佛山市南海区2022届高三上学期8月摸底测试化学试题
2021高三·全国·专题练习
名校
解题方法
5 . 肼(N2H4)-空气碱性燃料电池放电效率高,以该电池为电源模拟工业制烧碱,装置如图所示:
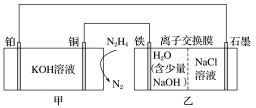
回答下列问题:
(1)乙装置的能量转化形式主要是_______ 。
(2)乙装置中离子交换膜的类型是_______ (填字母)。
A.质子交换膜 B.阳离子交换膜 C.阴离子交换膜
(3)铂电极的名称是_______ (填“正极”“负极”“阴极”或“阳极”)。
(4)写出铜电极的电极反应式:_______ 。
(5)电解过程中,石墨电极附近溶液的pH减小,其原因是___ (用化学用语和必要的文字说明)。
(6)若铂电极上有4.48LO2(标准状况)发生反应,装置的电流效率为80%,理论上制备纯度为96%的烧碱_______ g(结果保留1位小数)。

回答下列问题:
(1)乙装置的能量转化形式主要是
(2)乙装置中离子交换膜的类型是
A.质子交换膜 B.阳离子交换膜 C.阴离子交换膜
(3)铂电极的名称是
(4)写出铜电极的电极反应式:
(5)电解过程中,石墨电极附近溶液的pH减小,其原因是
(6)若铂电极上有4.48LO2(标准状况)发生反应,装置的电流效率为80%,理论上制备纯度为96%的烧碱
您最近一年使用:0次
2021-09-23更新
|
238次组卷
|
3卷引用:专题六 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)
(已下线)专题六 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)河南省南阳市一中2021-2022学年高二上学期第一次月考化学试题山西省怀仁市第一中学2021-2022学年高二上学期期中理科综合化学试题
2021高三·全国·专题练习
6 . 金属及其化合物在生产生活中具有广泛的应用。
(1)我国科学家设计的铝离子电池装置如图所示。已知电池总反应为nAl+4nAlCl +3(AlCl4)nMoSe2=4nAl2Cl
+3(AlCl4)nMoSe2=4nAl2Cl +3MoSe2。
+3MoSe2。
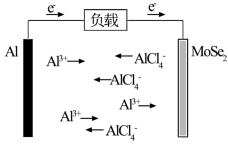
①负极材料为___ (填“A1”或“MoSe2”)。
②电池工作时能量形式由___ 转化为___ 。
③理论上生成2molAl2Cl 时,外电路转移电子的物质的量为
时,外电路转移电子的物质的量为__ mol。
(2)锂—硫电池是重要的新型储能可逆电池,其构造如图所示。
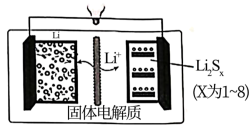
电池充电时,与电源负极所连电极发生的电极反应为___ ,在电池放电时,电池右边电极依次发生Li2S8→Li2S6→Li2S4→Li2S2→Li2S系列转化。若放电前,图右边电极中Li2Sx只有Li2S8,放电后生成产物Li2S、Li2S2物质的量之比为6:1,则1molLi2S8反应得到的电子数为__ 。
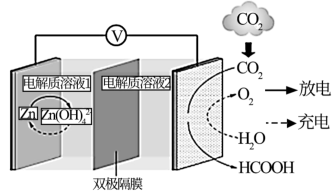
(3)一种新型Zn—CO2水介质电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸(HCOOH)。充电时电池总反应为__ ;放电时1molCO2转化为HCOOH,转移的电子数为__ mol。
(1)我国科学家设计的铝离子电池装置如图所示。已知电池总反应为nAl+4nAlCl
 +3(AlCl4)nMoSe2=4nAl2Cl
+3(AlCl4)nMoSe2=4nAl2Cl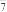 +3MoSe2。
+3MoSe2。
①负极材料为
②电池工作时能量形式由
③理论上生成2molAl2Cl
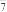 时,外电路转移电子的物质的量为
时,外电路转移电子的物质的量为(2)锂—硫电池是重要的新型储能可逆电池,其构造如图所示。

电池充电时,与电源负极所连电极发生的电极反应为

(3)一种新型Zn—CO2水介质电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸(HCOOH)。充电时电池总反应为
您最近一年使用:0次
名校
7 . 铅蓄电池是重要的二次电池。已知:铅蓄电池总的化学方程式为: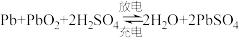 ,回答下列问题:
,回答下列问题:
(1)铅蓄电池负极板上覆盖的物质是__________ (填名称),充电时,PbSO4在__________ (填“阳极”、“阴极”或“两个电极”)上__________ (填“生成或除去”)。
(2)铅蓄电池在充电时正极接电源的__________ (正极/负极),充电时该极的电极反应式为__________ 。
(3)用铅蓄电池作为电源,电解饱和食盐水,电极均为惰性电极,电解饱和食盐水总反应的化学方程式为__________ 。当铅蓄电池负极生成2molPbSO4时,_________ (阴极/阳极)产生________ molH2。
(4)电解饱和食盐水工业生产中,采用了__________ (阴/阳)离子交换膜,这样做的原因有__________ 。
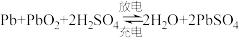 ,回答下列问题:
,回答下列问题:(1)铅蓄电池负极板上覆盖的物质是
(2)铅蓄电池在充电时正极接电源的
(3)用铅蓄电池作为电源,电解饱和食盐水,电极均为惰性电极,电解饱和食盐水总反应的化学方程式为
(4)电解饱和食盐水工业生产中,采用了
您最近一年使用:0次
名校
解题方法
8 . 我国某企业已研发出新一代LiFePO4“刀片电池”,具有高安全、长寿命等特点。LiFePO4电池的结构如图所示。反应可表示为6C + LiFePO4 LixC6 + Li1-x FePO4。下列说法错误的是
LixC6 + Li1-x FePO4。下列说法错误的是
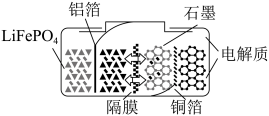
 LixC6 + Li1-x FePO4。下列说法错误的是
LixC6 + Li1-x FePO4。下列说法错误的是
| A.放电时,电流方向为:正极→导线→负载→导线→负极→电解质→正极 |
| B.放电时,负极的电极反应式:LixC6-xe-=xLi++6C |
| C.充电时,LiFePO4 转化为Li1-xFePO4的过程中铁元素的价态保持不变 |
| D.充电时,部分锂离子从LiFePO4中脱出,向石墨电极迁移生成LixC6 |
您最近一年使用:0次
名校
解题方法
9 . 如图所示,U形管内盛有100 mL的溶液,按要求回答下列问题:
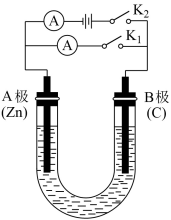
(1)断开K2,闭合K1,若所盛溶液为CuSO4溶液,则A极为___________ 极,B极的电极反应式为___________ 。若所盛溶液为KCl溶液,则B极的电极反应式为___________ 。
(2)断开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可以观察到的现象是___________ 。
②B电极上的电极反应式为___________ ,总反应的化学方程式是___________ 。
③反应一段时间后断开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2 mL,将溶液充分混合,溶液的pH约为___________ 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的___________ 。

(1)断开K2,闭合K1,若所盛溶液为CuSO4溶液,则A极为
(2)断开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可以观察到的现象是
②B电极上的电极反应式为
③反应一段时间后断开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2 mL,将溶液充分混合,溶液的pH约为
您最近一年使用:0次
2021高三·全国·专题练习
名校
解题方法
10 . 如图A为碱性硼化钒(VB2)—空气电池示意图,两极用离子交换膜隔开,VB2放电时生成两种氧化物。若用该电池为电源,用惰性电极电解硫酸铜溶液,实验装置如图B所示。则下列说法错误的是
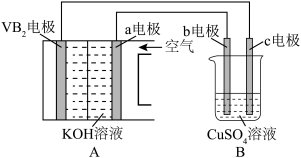

| A.碱性硼化钒(VB2)—空气电池中使用阴离子交换膜 |
| B.外电路中电子由VB2电极流向c电极 |
| C.电解过程中,b电极表面产生的气体可以收集后充入A池中的电极循环利用 |
| D.VB2电极发生的电极反应为2VB2-22e-+11H2O=V2O5+2B2O3+22H+ |
您最近一年使用:0次
2021-09-06更新
|
292次组卷
|
4卷引用:专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第四章第三节 电解池(第1课时 电解原理)(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题黑龙江省齐齐哈尔中学2022-2023学年高三上学期11月期中考试化学试题



