1 . 减少 的排放、捕集并利用
的排放、捕集并利用 是我国能源领域的一个重要战略方向。
是我国能源领域的一个重要战略方向。
在 加氢合成甲醇的体系中,同时存在以下反应:
加氢合成甲醇的体系中,同时存在以下反应:
反应i:
 kJ/mol
kJ/mol
反应ii:
 kJ/mol
kJ/mol
(1)反应iii: 的
的
___________ 。
(2)在 加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。
加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。
(3)某温度下,向容积恒为1 L的密闭容器中通入1 mol 和5 mol
和5 mol  ,10 min后体系达到平衡,此时
,10 min后体系达到平衡,此时 的转化率为20%。
的转化率为20%。 的选择性为50%。[已知:
的选择性为50%。[已知: 的选择性:
的选择性: ]
]
①反应i的平衡常数
___________ (写出计算式即可)。
②反应ii的净速率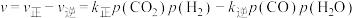 ,其中
,其中 、
、 分别为正、逆反应的速率常数,p为气体的分压。降低温度时,
分别为正、逆反应的速率常数,p为气体的分压。降低温度时,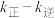
___________ (填“增大”“减小”或“不变”)。
③其他条件相同时,反应温度对 的平衡转化率和
的平衡转化率和 的选择性的影响如图甲所示,温度高于260°C时,
的选择性的影响如图甲所示,温度高于260°C时, 的平衡转化率变化的原因是
的平衡转化率变化的原因是___________ 。 的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:
的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:___________ 。
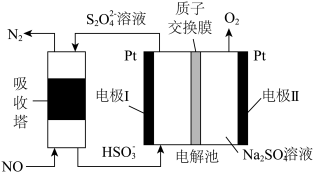
(4)利用如图所示原理去除NO:___________ ,每产生224 mL  (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为___________ mol。
 的排放、捕集并利用
的排放、捕集并利用 是我国能源领域的一个重要战略方向。
是我国能源领域的一个重要战略方向。在
 加氢合成甲醇的体系中,同时存在以下反应:
加氢合成甲醇的体系中,同时存在以下反应:反应i:

 kJ/mol
kJ/mol反应ii:

 kJ/mol
kJ/mol(1)反应iii:
 的
的
(2)在
 加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。
加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。| A.若在绝热恒容容器,反应i的平衡常数K保持不变,说明反应i、ii都已达平衡 |
| B.若气体的平均相对分子质量不变,说明反应i、花都已达平衡 |
| C.体系达平衡后,若压缩体积,反应i平衡正向移动,反应i平衡不移动 |
| D.选用合适的催化剂可以提高甲醇在单位时间内的产量 |
(3)某温度下,向容积恒为1 L的密闭容器中通入1 mol
 和5 mol
和5 mol  ,10 min后体系达到平衡,此时
,10 min后体系达到平衡,此时 的转化率为20%。
的转化率为20%。 的选择性为50%。[已知:
的选择性为50%。[已知: 的选择性:
的选择性: ]
]①反应i的平衡常数

②反应ii的净速率
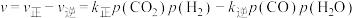 ,其中
,其中 、
、 分别为正、逆反应的速率常数,p为气体的分压。降低温度时,
分别为正、逆反应的速率常数,p为气体的分压。降低温度时,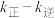
③其他条件相同时,反应温度对
 的平衡转化率和
的平衡转化率和 的选择性的影响如图甲所示,温度高于260°C时,
的选择性的影响如图甲所示,温度高于260°C时, 的平衡转化率变化的原因是
的平衡转化率变化的原因是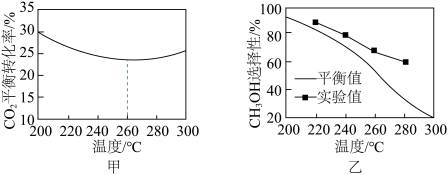
 的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:
的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:(4)利用如图所示原理去除NO:
 (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 我国科研团队研发了一种新型可充放电的生物质电池,其工作原理如图所示,下列说法不正确的是
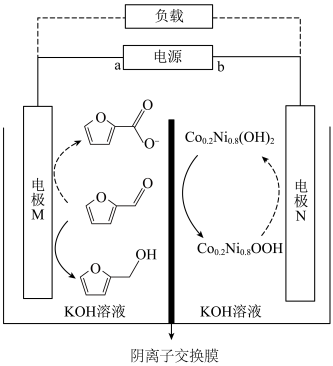
| A.充电时,a为电源的负极 |
| B.放电时,M极附近电解质溶液pH不变 |
| C.放电时,若外电路转移1mol电子,理论上N极增重1g |
D.充电时,M电极反应为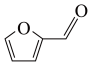 +2e—+2H2O= +2e—+2H2O=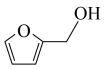 +2OH— +2OH— |
您最近一年使用:0次
2024-06-01更新
|
105次组卷
|
2卷引用:云南省曲靖市2023-2024学年高三下学期第二次教学质量监测理科综合试题卷-高中化学
名校
3 . 我国科研人员设计将甲烷和二氧化碳电化学耦合制备甲酸(如图,硫酸钠溶液为电解液)。下列说法错误的是

| A.载有催化剂的多孔电极有利于吸附气体发生反应 |
| B.隔膜宜选用质子交换膜 |
C.阴极的电极反应式为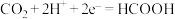 |
D.转移 电子时,最多生成 电子时,最多生成 |
您最近一年使用:0次
名校
解题方法
4 . 对氨基苯酚可用作农药、医药、染料等精细化学品的中间体,利用Al-PbO2电池(其装置如图甲所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图乙所示。已知电池工作过程中R区的K2SO4溶液浓度增大,下列说法正确的是
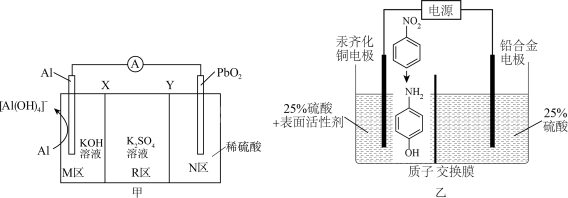
| A.X为阴离子交换膜 |
| B.铅合金电极应与Al电极相连 |
C.汞齐化铜电极上的反应式为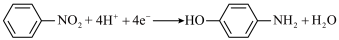 |
D.PbO2电极上的反应式为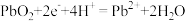 |
您最近一年使用:0次
2024-05-12更新
|
116次组卷
|
2卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三下学期适应性月考(九)理综试卷-高中化学
5 . 合物是化工、能源、环保等领域的研究热点。回答下列问题:
(1)如图所示为利用 和空气中的
和空气中的 以
以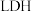 超薄纳米为催化剂在光催化作用下合成氨的原理。
超薄纳米为催化剂在光催化作用下合成氨的原理。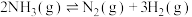

Ⅱ.
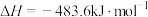
则上述合成氨的热化学方程式为___________ 。
(2)合成尿素 的反应为
的反应为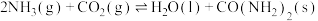
 。向恒容密闭容器中按物质的量之比
。向恒容密闭容器中按物质的量之比 充入
充入 和
和 ,使反应进行,保持温度不变,测得
,使反应进行,保持温度不变,测得 的转化率随时间的变化情况如图所示。
的转化率随时间的变化情况如图所示。 的浓度变化表示反应速率,则
的浓度变化表示反应速率,则 点的逆反应速率
点的逆反应速率___________ B点的正反应速率(填“>”“<”或“=”)。
②下列叙述中不能说明该反应达到平衡状态的是___________ (填序号)。
A.体系压强不再变化
B.气体平均摩尔质量不再变化
C. 的消耗速率和
的消耗速率和 的消耗速率之比为
的消耗速率之比为
D.固体质量不再发生变化
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量 。实验发现,
。实验发现, 易发生二聚反应
易发生二聚反应 并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为
并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为 和
和 时NO的转化率随时间变化的结果如图所示。
时NO的转化率随时间变化的结果如图所示。 时,达到平衡时体系的总压强为
时,达到平衡时体系的总压强为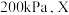 点
点 的物质的量分数为
的物质的量分数为___________ (保留三位有效数字), 点对应的平衡常数
点对应的平衡常数
___________  (用分压表示,保留小数点后三位);提高NO平衡转化率的条件为
(用分压表示,保留小数点后三位);提高NO平衡转化率的条件为___________ (任写两点)。
②如图所示,利用电解原理,可将废气中的 转化为
转化为 ,阳极的电极反应式为
,阳极的电极反应式为___________ ,通入 的目的是
的目的是___________ 。
(1)如图所示为利用
 和空气中的
和空气中的 以
以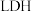 超薄纳米为催化剂在光催化作用下合成氨的原理。
超薄纳米为催化剂在光催化作用下合成氨的原理。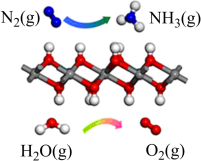
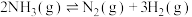

Ⅱ.

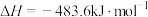
则上述合成氨的热化学方程式为
(2)合成尿素
 的反应为
的反应为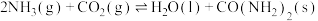
 。向恒容密闭容器中按物质的量之比
。向恒容密闭容器中按物质的量之比 充入
充入 和
和 ,使反应进行,保持温度不变,测得
,使反应进行,保持温度不变,测得 的转化率随时间的变化情况如图所示。
的转化率随时间的变化情况如图所示。
 的浓度变化表示反应速率,则
的浓度变化表示反应速率,则 点的逆反应速率
点的逆反应速率②下列叙述中不能说明该反应达到平衡状态的是
A.体系压强不再变化
B.气体平均摩尔质量不再变化
C.
 的消耗速率和
的消耗速率和 的消耗速率之比为
的消耗速率之比为
D.固体质量不再发生变化
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量
 。实验发现,
。实验发现, 易发生二聚反应
易发生二聚反应 并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为
并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为 和
和 时NO的转化率随时间变化的结果如图所示。
时NO的转化率随时间变化的结果如图所示。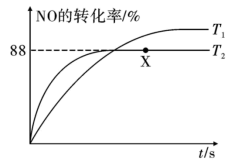
 时,达到平衡时体系的总压强为
时,达到平衡时体系的总压强为 点
点 的物质的量分数为
的物质的量分数为 点对应的平衡常数
点对应的平衡常数
 (用分压表示,保留小数点后三位);提高NO平衡转化率的条件为
(用分压表示,保留小数点后三位);提高NO平衡转化率的条件为②如图所示,利用电解原理,可将废气中的
 转化为
转化为 ,阳极的电极反应式为
,阳极的电极反应式为 的目的是
的目的是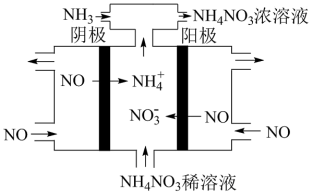
您最近一年使用:0次
名校
6 . 试运用化学原理知识解答下列问题。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的平衡时百分含量和温度的关系如图所示。根据图示回答下列问题:
2SO3(g),混合体系中SO3的平衡时百分含量和温度的关系如图所示。根据图示回答下列问题: 2SO3(g)的△H
2SO3(g)的△H___________ 0(填“>”或“<”)。
②温度为T1、T2,反应的平衡常数分别为K1、K2,则K1___________ K2(填“>”“<”或“=”)。
③若反应进行到状态D时,v正___________ v逆(填“>”“<”或“=”)。
(2)在一定温度下的某可变容器中保持恒压条件下发生2SO2(g)+O2(g) 2SO3(g),当反应达到后,若向平衡体系中通入氦气,平衡
2SO3(g),当反应达到后,若向平衡体系中通入氦气,平衡___________ 移动(填“向左”“向右”或“不”)。
(3)含镉(Cd2+)废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。用CaCO3处理Cd2+的离子方程式是___________ 。工业常选用CaCO3而不用Na2CO3的主要原因是___________ 。[已知:常温下,Ksp(CdCO3)=5.6×10-12、Ksp(CaCO3)=2.8×10-9]
(4)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗。___________ 离子交换膜(填“阴”或“阳”)。
②反应的总化学方程式为___________ ,电解一段时间后,右侧溶液质量___________ (填“增加”或“减少)。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)
 2SO3(g),混合体系中SO3的平衡时百分含量和温度的关系如图所示。根据图示回答下列问题:
2SO3(g),混合体系中SO3的平衡时百分含量和温度的关系如图所示。根据图示回答下列问题:
 2SO3(g)的△H
2SO3(g)的△H②温度为T1、T2,反应的平衡常数分别为K1、K2,则K1
③若反应进行到状态D时,v正
(2)在一定温度下的某可变容器中保持恒压条件下发生2SO2(g)+O2(g)
 2SO3(g),当反应达到后,若向平衡体系中通入氦气,平衡
2SO3(g),当反应达到后,若向平衡体系中通入氦气,平衡(3)含镉(Cd2+)废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。用CaCO3处理Cd2+的离子方程式是
(4)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗。

②反应的总化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 某电化学锂富集装置如图,工作步骤如下:Ⅰ.向MnO2所在腔室通入海水,启动电源乙,使海水中 进入MnO2结构形成
进入MnO2结构形成 ;Ⅱ.关闭电源乙和海水通道,启动电源甲,同时向电极a上通入O2.下列说法错误的是
;Ⅱ.关闭电源乙和海水通道,启动电源甲,同时向电极a上通入O2.下列说法错误的是
 进入MnO2结构形成
进入MnO2结构形成 ;Ⅱ.关闭电源乙和海水通道,启动电源甲,同时向电极a上通入O2.下列说法错误的是
;Ⅱ.关闭电源乙和海水通道,启动电源甲,同时向电极a上通入O2.下列说法错误的是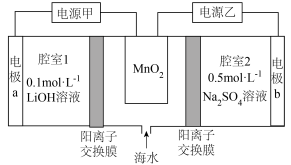
| A.电极b与电源乙的正极相连 |
B.步骤Ⅰ时,腔室2中的 进入MnO2所在腔室 进入MnO2所在腔室 |
C.步骤Ⅱ时,阳极的电极反应式为 |
| D.在电极a上每消耗5.6 L O2(换算成标准状况),腔室1质量增加7 g |
您最近一年使用:0次
2024-04-02更新
|
1191次组卷
|
9卷引用:2024届云南省大理州民族中学高三下学期5月月考理综试卷-高中化学
2024届云南省大理州民族中学高三下学期5月月考理综试卷-高中化学2024届东北三省三校高三下学期第二次联合模拟考试理综重组卷-高中化学东北三省2024届高三下学期三校二模联考化学试题黑龙江省哈尔滨市三校联考2024届高三二模化学试题江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 东北三省2024届高三下学期三校二模联考化学试题(已下线)题型8 反应热 电化学的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届江西省吉安市第一中学高三下学期一模化学试题(已下线)压轴题06?电化学原理综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
8 . 可充电水系电池因其安全性高、成本低而成为大规模能源存储的潜在系统。我国某高校研究人员报告了一种两性羟基乙酸铝( )为电解质的水系电池,其电解质具有
)为电解质的水系电池,其电解质具有 和
和 双极电离能力,可促进蒽醌(AQ)电极和氢氧化镍(
双极电离能力,可促进蒽醌(AQ)电极和氢氧化镍( )电极的氧化还原反应,工作原理如图所示,下列说法正确的是
)电极的氧化还原反应,工作原理如图所示,下列说法正确的是

A. 的 的 |
B.充电时,阴极的电极反应式为: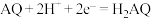 |
| C.放电时,正极与负极的电势差逐渐增大 |
| D.放电时,正极与负极的质量差逐渐减小 |
您最近一年使用:0次
名校
9 .  是生产金属钛及其化合物的重要中间体。工业上以高钛渣(主要成分是
是生产金属钛及其化合物的重要中间体。工业上以高钛渣(主要成分是 )为原料生产
)为原料生产 的反应原理为
的反应原理为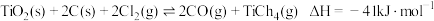 。回答下列问题:
。回答下列问题:
(1)已知:
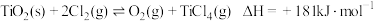 、
、 的燃烧热为
的燃烧热为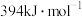 ,则表示CO燃烧热的热化学方程式为
,则表示CO燃烧热的热化学方程式为(2)
 时,将足量的
时,将足量的 和C加入一恒容密闭容器中,并通入一定量的
和C加入一恒容密闭容器中,并通入一定量的 和
和 的混合气体,
的混合气体, 不参与化学反应。容器中只发生反应:
不参与化学反应。容器中只发生反应: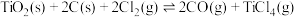 ,测得容器中的总压强(p总压)与
,测得容器中的总压强(p总压)与 的转化率(
的转化率( )随时间的变化关系如图所示:
)随时间的变化关系如图所示: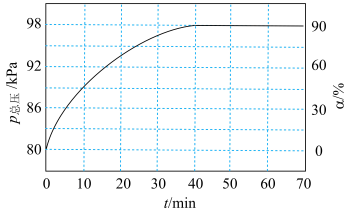
保持温度和起始总压相同,若向恒容密闭容器中通入的 不含
不含 ,与含
,与含 相比,
相比, 的平衡转化率将
的平衡转化率将
(3)利用
 制得
制得 ,焙烧
,焙烧 可得纳米
可得纳米 。书写
。书写 水解制备
水解制备 反应的化学方程式:
反应的化学方程式:(4)电解法生产钛的原理如图所示,电解过程中,被还原的Ca进一步还原
 得到钛。其中,直流电源a为
得到钛。其中,直流电源a为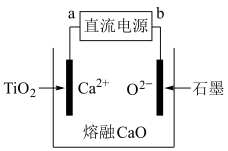
您最近一年使用:0次
解题方法
10 . 完成下列问题。
(1)用 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如图所示,电极材料为石墨。
,其原理如图所示,电极材料为石墨。
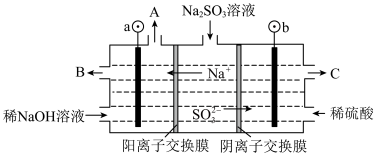
①图中b极要连接电源的______ (填“正”或“负”)极,B物质是________ 。
② 放电的电极反应式为:
放电的电极反应式为:________ 。
(2)已知 ,利用该反应设计电池的装置如图所示,此方法既能有效清除废气中的氮氧化物,减轻环境污染,又能充分利用化学能。
,利用该反应设计电池的装置如图所示,此方法既能有效清除废气中的氮氧化物,减轻环境污染,又能充分利用化学能。
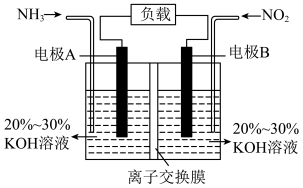
为使电池持续放电,离子交换膜需选用______ (填“阳”或“阴”)离子交换膜;电极A的电极反应式为_______ ;当有 (已折算成标准状况下的体积)
(已折算成标准状况下的体积) 被处理时,转移的电子数为
被处理时,转移的电子数为_______ 。
(1)用
 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如图所示,电极材料为石墨。
,其原理如图所示,电极材料为石墨。
①图中b极要连接电源的
②
 放电的电极反应式为:
放电的电极反应式为:(2)已知
 ,利用该反应设计电池的装置如图所示,此方法既能有效清除废气中的氮氧化物,减轻环境污染,又能充分利用化学能。
,利用该反应设计电池的装置如图所示,此方法既能有效清除废气中的氮氧化物,减轻环境污染,又能充分利用化学能。
为使电池持续放电,离子交换膜需选用
 (已折算成标准状况下的体积)
(已折算成标准状况下的体积) 被处理时,转移的电子数为
被处理时,转移的电子数为
您最近一年使用:0次



