名校
解题方法
1 . 硼化物在生产、生活和科研中应用广泛。回答下列问题:
(1)立方氮化硼硬度大,熔点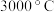 ,其晶体类型为
,其晶体类型为___________ 。
制备氮化硼( )的一种方法为
)的一种方法为 。
。 的空间构型为
的空间构型为___________ ,形成 时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式可能为
时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式可能为___________ (填标号)。 的球棍模型如图1所示。其中B原子的杂化方式有
的球棍模型如图1所示。其中B原子的杂化方式有___________ ,该阴离子中所存在的化学键类型有___________ (填标号)。
(3) 与B组成的金属硼化物结构如图2所示,硼原子全部组成
与B组成的金属硼化物结构如图2所示,硼原子全部组成 正八面体,各个顶点通过
正八面体,各个顶点通过 键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为
键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为___________ ,晶体中 原子的配位数为
原子的配位数为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为 ,已知
,已知 八面体中
八面体中 键的键长为
键的键长为 ,晶胞参数为
,晶胞参数为 ,
, 为阿伏加德罗常数的值,则N点原子的分数坐标为
为阿伏加德罗常数的值,则N点原子的分数坐标为___________ ,该金属硼化物的密度为___________  (列出计算式即可)。
(列出计算式即可)。
(1)立方氮化硼硬度大,熔点
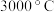 ,其晶体类型为
,其晶体类型为制备氮化硼(
 )的一种方法为
)的一种方法为 。
。 的空间构型为
的空间构型为 时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式可能为
时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式可能为A. 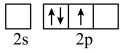 B.
B. 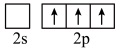 C.
C. 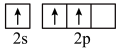 D.
D.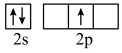
 的球棍模型如图1所示。其中B原子的杂化方式有
的球棍模型如图1所示。其中B原子的杂化方式有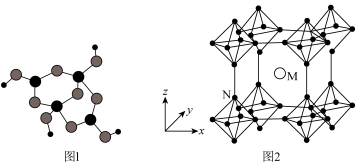
(3)
 与B组成的金属硼化物结构如图2所示,硼原子全部组成
与B组成的金属硼化物结构如图2所示,硼原子全部组成 正八面体,各个顶点通过
正八面体,各个顶点通过 键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为
键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为 原子的配位数为
原子的配位数为 ,已知
,已知 八面体中
八面体中 键的键长为
键的键长为 ,晶胞参数为
,晶胞参数为 ,
, 为阿伏加德罗常数的值,则N点原子的分数坐标为
为阿伏加德罗常数的值,则N点原子的分数坐标为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
名校
解题方法
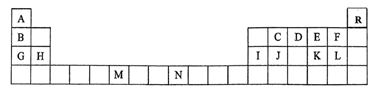
2 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式___________ 。
(2)D的气态氢化物的VSEPR模型为___________ ,其中心原子的杂化类型为___________ 。
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:___________ (用元素符号作答)。
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
(5)要证明太阳上是否含有R元素,可采用的方法是___________ 。
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有___________ (填元素符号)。
(7)C元素是形成有机物的主要元素,下列分子中含有sp和 杂化方式的是
杂化方式的是___________ (填字母)。
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式
(2)D的气态氢化物的VSEPR模型为
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
A. | B. | C. | D.苯 |
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有
(7)C元素是形成有机物的主要元素,下列分子中含有sp和
 杂化方式的是
杂化方式的是a.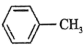 b.
b. c.
c. d.
d.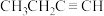
您最近一年使用:0次



