解题方法
1 . 实验室利用下图装置用乙醇和浓硫酸在 反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
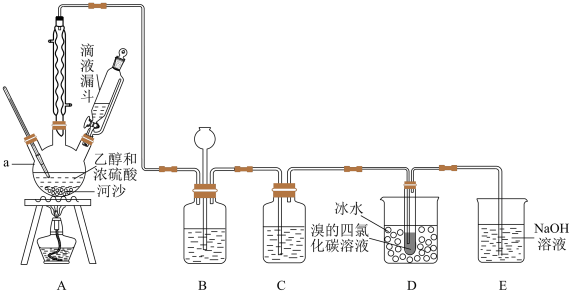
(1)在装置A中,生成的气体除乙烯外还有乙醚、 、
、 等,则生成乙烯的化学方程式为
等,则生成乙烯的化学方程式为___________ ,仪器a的名称为___________ 。
(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为___________ 。
(3)装置C可除去 、
、 ,所盛放的溶液为
,所盛放的溶液为___________ 。
(4)装置D中进行的主要反应的化学方程式为___________ ,可观察到的实验现象是___________ 。把试管置于盛有冰水的小烧杯中的目的是___________ 。
 反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
(1)在装置A中,生成的气体除乙烯外还有乙醚、
 、
、 等,则生成乙烯的化学方程式为
等,则生成乙烯的化学方程式为(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为
(3)装置C可除去
 、
、 ,所盛放的溶液为
,所盛放的溶液为(4)装置D中进行的主要反应的化学方程式为
您最近一年使用:0次
2023-07-29更新
|
179次组卷
|
2卷引用:山东省青岛莱西市2022-2023学年高二下学期7月期末考试化学试题
2 . 常见的有机反应装置示意图如下所示:
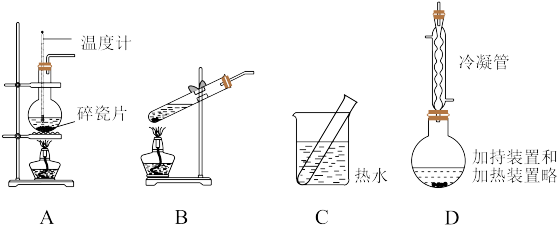
(1)实验室用乙醇制取乙烯,可选择上述装置_______ (填序号)。实验过程中,加热须注意的操作是_______ 。
(2)实验室制取乙酸乙酯,可选择上述装置_______ (填序号)。实验前,添加试剂的顺序依次是_______ 。对获得的粗产品进行纯化时,可向酯层中依次加入 溶液、饱和NaCl溶液、饱和
溶液、饱和NaCl溶液、饱和 溶液、无水硫酸镁,最后蒸馏。其中加入
溶液、无水硫酸镁,最后蒸馏。其中加入 溶液的目的是
溶液的目的是_______ 。
(3)实验室中用乙醛和银氨溶液做银镜反应实验,可选择上述装置_______ (填序号)。
①洗涤试管。在试管里先注入少量NaOH溶液,振荡,煮沸,其目的是_______ ;
②配制银氨溶液。在洁净的试管中,加入1 mL 20%的 溶液,边振荡边滴加2%的氨水,直至
溶液,边振荡边滴加2%的氨水,直至_______ ,写出填空内容对应的离子方程式_______ 。

(1)实验室用乙醇制取乙烯,可选择上述装置
(2)实验室制取乙酸乙酯,可选择上述装置
 溶液、饱和NaCl溶液、饱和
溶液、饱和NaCl溶液、饱和 溶液、无水硫酸镁,最后蒸馏。其中加入
溶液、无水硫酸镁,最后蒸馏。其中加入 溶液的目的是
溶液的目的是(3)实验室中用乙醛和银氨溶液做银镜反应实验,可选择上述装置
①洗涤试管。在试管里先注入少量NaOH溶液,振荡,煮沸,其目的是
②配制银氨溶液。在洁净的试管中,加入1 mL 20%的
 溶液,边振荡边滴加2%的氨水,直至
溶液,边振荡边滴加2%的氨水,直至
您最近一年使用:0次
3 . 用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):
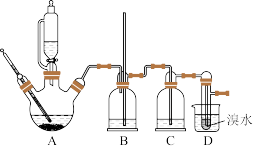
有关数据列表如下:
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是_______(填字母代号)。
(2)装置B的作用是_______ 。
(3)在装置C中应加入_______(填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
(4)若产物中有少量未反应的Br2,最好用_______(填字母代号)洗涤除去。
(5)若产物中有少量副产物乙醚,可用_______ 的方法除去。
(6)为了检验1,2-二溴乙烷中的溴元素,取出少量产品,下列几项实验步骤正确的操作顺序是_______(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH水溶液;⑤冷却

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/(g·cm-3) | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 131 | 34.6 |
| 熔点/℃ | -114 | 10 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是_______(填字母代号)。
| A.引发反应 | B.加快反应速率 | C.防止乙醇挥发 | D.减少副产物乙醚生成 |
(3)在装置C中应加入_______(填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
| A.水 | B.浓硫酸 | C.氢氧化钠溶液 | D.饱和碳酸氢钠溶液 |
| A.水 | B.氢氧化钠溶液 | C.碘化钠溶液 | D.乙醇 |
(6)为了检验1,2-二溴乙烷中的溴元素,取出少量产品,下列几项实验步骤正确的操作顺序是_______(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH水溶液;⑤冷却
| A.④①⑤③② | B.④③①⑤② | C.④③②①⑤ | D.④②①③⑤ |
您最近一年使用:0次
4 . 实验室制取乙烯的装置如图Ⅰ所示。根据实验及有关操作回答下列问题。
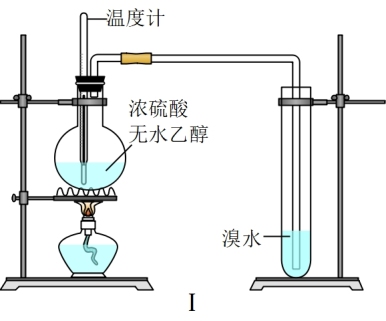
(1)甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:___ 。
(2)乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:
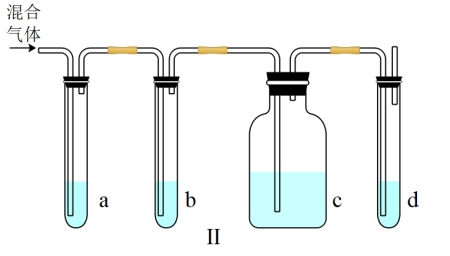
①Ⅱ装置abcd中可盛放的试剂的顺序依次是____ (填序号)。
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是____ 。
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。
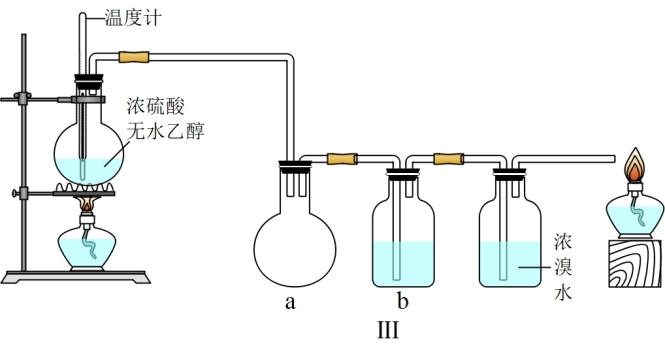
①图Ⅲ中装置a的作用是____ 。
②为除去混合气中的SO2和CO2,装置b中应该盛放的试剂是____ 。
③浓溴水的作用是____ 。
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是____ 。

(1)甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:
(2)乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:

①Ⅱ装置abcd中可盛放的试剂的顺序依次是
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。

①图Ⅲ中装置a的作用是
②为除去混合气中的SO2和CO2,装置b中应该盛放的试剂是
③浓溴水的作用是
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是
您最近一年使用:0次
解题方法
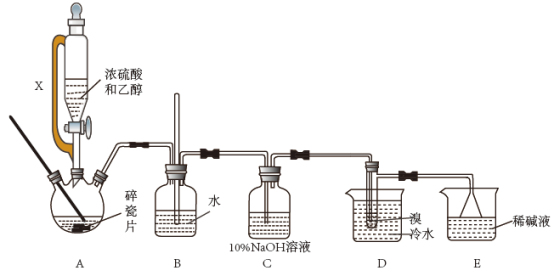
5 . 实验室用乙醇和浓硫酸反应制备乙烯,乙烯再与溴反应制备1,2—二溴乙烷。装置如图所示(加热及夹持装置省略):
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。
有关数据列表如下:
回答下列问题:
(1)该装置中盛放浓硫酸和乙醇的仪器名称___ ;装置B的作用__ 。
(2)装置C中10%NaOH溶液的作用___ 。
(3)在A中发生的化学反应方程式为___ 。
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是___ 。
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在__ (填“上”或“下”)层。
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是__ 。
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。

有关数据列表如下:
| 物质 | 乙醇 | 1,2—二溴乙烷 | 溴 |
| 密度g·cm-3 | 0.79 | 2.2 | 3.12 |
| 沸点/℃ | 78.5 | 132 | 59 |
(1)该装置中盛放浓硫酸和乙醇的仪器名称
(2)装置C中10%NaOH溶液的作用
(3)在A中发生的化学反应方程式为
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
您最近一年使用:0次
2021-05-07更新
|
268次组卷
|
2卷引用:山东省日照五莲县2020-2021学年高二下学期期中考试化学试题
解题方法
6 . 已知乙醇和浓硫酸混合加热到170℃可制得乙烯,同时乙烯中会混有少量的CO2和SO2杂质。某化学小组利用如图1装置来制备1,2—二溴乙烷,利用图2装置来进一步精制。1,2—二溴乙烷是无色液体,密度为2.18g•cm-3,沸点为131.4℃,熔点为9.79℃,微溶于水,易溶于乙醇、乙醚、丙酮等有机溶剂。实验前将无水乙醇和浓硫酸按体积比1:3混合好制得乙烯制备液。
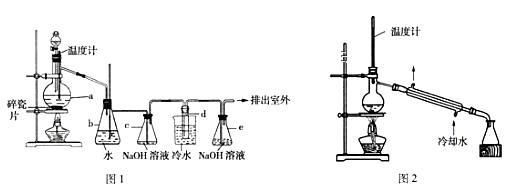
I.制备粗品
实验步骤:连接好装置,检查装置的气密性。分液漏斗中装乙烯制备液,d中装适量的液溴(表面覆盖少量水),其他药品按图1加入,打开分液漏斗旋塞滴入适量的液体后,关闭旋塞,点燃酒精灯加热使温度迅速升高到170℃直至反应完全,停止加热。回答下列问题:
(1)仪器a的名称为___ ,b装置的作用为___ 。
(2)若要配制60mL的乙烯制备液,请简述实验操作__ 。
(3)d装置中发生反应的化学方程式为__ 。
(4)如果缺少c装置会导致1,2—二溴乙烷的产率降低,原因是___ (用离子方程式表示),锥形瓶e中NaOH溶液的作用是____ 。
(5)判断d中液溴反应完全的标准是___ 。
II.制备精品
(6)d中制得的1,2—二溴乙烷中含有水,可先用____ 方法进行分离,再将1,2—二溴乙烷用如图2装置进行蒸馏,蒸馏时加入无水Na2SO4的目的是___ ,收集产品时,温度应控制在__ 左右。

I.制备粗品
实验步骤:连接好装置,检查装置的气密性。分液漏斗中装乙烯制备液,d中装适量的液溴(表面覆盖少量水),其他药品按图1加入,打开分液漏斗旋塞滴入适量的液体后,关闭旋塞,点燃酒精灯加热使温度迅速升高到170℃直至反应完全,停止加热。回答下列问题:
(1)仪器a的名称为
(2)若要配制60mL的乙烯制备液,请简述实验操作
(3)d装置中发生反应的化学方程式为
(4)如果缺少c装置会导致1,2—二溴乙烷的产率降低,原因是
(5)判断d中液溴反应完全的标准是
II.制备精品
(6)d中制得的1,2—二溴乙烷中含有水,可先用
您最近一年使用:0次
名校
7 . 某化学兴趣小组用下图所示装置进行探究实验。以验证产物中有乙烯生成,且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中的溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。

(1)写出该实验中生成乙烯的化学方程式___________________________________ ;
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是________ 。
A.乙烯与溴水易发生取代反应
B.使溴水褪色的反应,未必是加成反应
C.使溴水褪色的物质,未必是乙烯
D.浓硫酸氧化乙醇生成乙酸,也会使溴水带色
(3)乙同学经过细致观察后认为:试管中另一现象可证明反应中有乙烯生成,这个现象是___________________________________ 。为验证这一反应是加成反应而不是取代反应,可用pH试纸来测试反应后溶液的酸性,理由是________________________________ 。
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加如图所示装置,则A中的试剂应为_____________ ,其作用是_________________ ,B中的试剂为______________ 。

(5)处理上述实验后烧瓶中废液的正确方法是_______________
A.废液经冷却后倒入下水道中
B.废液经冷却后倒入空废液缸中
C.将水加入烧瓶中稀释后倒入废液缸

(1)写出该实验中生成乙烯的化学方程式
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是
A.乙烯与溴水易发生取代反应
B.使溴水褪色的反应,未必是加成反应
C.使溴水褪色的物质,未必是乙烯
D.浓硫酸氧化乙醇生成乙酸,也会使溴水带色
(3)乙同学经过细致观察后认为:试管中另一现象可证明反应中有乙烯生成,这个现象是
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加如图所示装置,则A中的试剂应为

(5)处理上述实验后烧瓶中废液的正确方法是
A.废液经冷却后倒入下水道中
B.废液经冷却后倒入空废液缸中
C.将水加入烧瓶中稀释后倒入废液缸
您最近一年使用:0次
2020-09-22更新
|
162次组卷
|
2卷引用:山东省日照市国开中学2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
8 . 实验室制备 1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备 1,2-二溴乙烷,装置如下图所示:
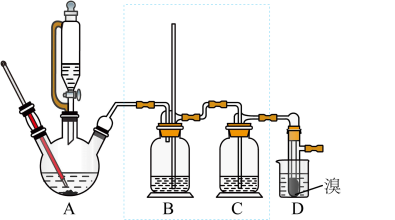
有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是_______ ; (填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置 A 中除了浓硫酸和乙醇外,还应加入___ ,装置A 中生成副产物乙醚的化学反应方程式__ 。
(3) 实验室制取乙烯,常因温度过高而使乙醇和浓 H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在 A 和 D 之间加入了 B、C 两个装置,其中 B 和C 中可分别盛放_____ 。
a.酸性 KMnO4和水 b.品红和NaOH 溶液
c.酸性 KMnO4和 NaOH 溶液 d.品红和酸性 KMnO4
(4) 将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在______ 层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______ 的方法除去。

有关数据列表如下:
物质 | 乙醇 | 1,2—二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g‧cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置 A 中除了浓硫酸和乙醇外,还应加入
(3) 实验室制取乙烯,常因温度过高而使乙醇和浓 H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在 A 和 D 之间加入了 B、C 两个装置,其中 B 和C 中可分别盛放
a.酸性 KMnO4和水 b.品红和NaOH 溶液
c.酸性 KMnO4和 NaOH 溶液 d.品红和酸性 KMnO4
(4) 将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
您最近一年使用:0次
9 . 工业中很多重要的原料都是来源于石油化工,如图所示:
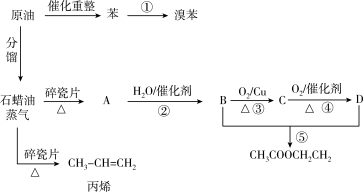
请回答下列问题:
(1) C的结构简式为_______ ,D中官能团的名称是______ 。
(2)②、⑤反应的反应类型分别是_____ 、______ 。
(3)反应①的化学方程式为_____ ;反应③的化学方程式为_____ 。
(4)丙烯分子中最多有____ 个原子共面,丙烯在一定条件下可以发生加聚反应,写出其反应的化学方程式:_____ 。
(5)某实验小组用以下装置制备乙酸乙酯。
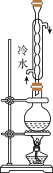
球形冷凝管的作用是_____ 。将圆底烧瓶中的液体倒入饱和碳酸钠溶液中,经过多步操作,可分离得到粗产品。此过程中定需要的操作是______ (填序号)。
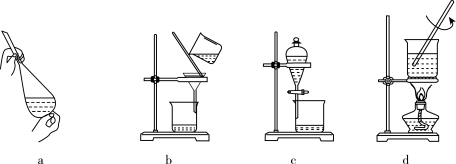

请回答下列问题:
(1) C的结构简式为
(2)②、⑤反应的反应类型分别是
(3)反应①的化学方程式为
(4)丙烯分子中最多有
(5)某实验小组用以下装置制备乙酸乙酯。

球形冷凝管的作用是

您最近一年使用:0次
10 . 某同学设计实验探究工业制乙烯的原理和乙烯主要的化学性质,实验装置如图所示。
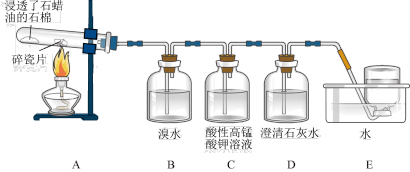
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34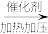 C8H18+甲,甲
C8H18+甲,甲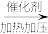 4乙,则甲的分子式为
4乙,则甲的分子式为______ ;乙的结构简式为____ 。
(2)B装置中的实验现象是______ 。
(3)C装置中的实验现象是_____ ,其中发生反应的反应类型是___ 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_ (填序号)中的实验现象可判断该资料是否真实。
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是_____ (填序号,下同);除去甲烷中乙烯的方法是____ 。
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,乙烯产生黑烟,原因是_____ 。

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34
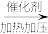 C8H18+甲,甲
C8H18+甲,甲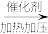 4乙,则甲的分子式为
4乙,则甲的分子式为(2)B装置中的实验现象是
(3)C装置中的实验现象是
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,乙烯产生黑烟,原因是
您最近一年使用:0次
2020-06-29更新
|
281次组卷
|
3卷引用:山东省滕州市第五中学2022-2023学年高一下学期5月月考化学试题



