名校
1 . 海洋是巨大的资源宝库,可以提取到我们需要的食盐、溴和碘。
I.从海水中提取食盐和溴的过程如下:
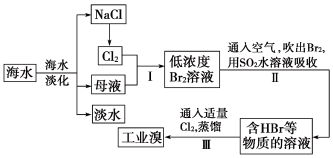
(1)步骤I中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为:_______ 。
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为:_______ 。
Ⅱ.实验:探究硫酸浓度对化学反应速率的影响
常温下,酸性KI溶液在空气中会被氧化为碘单质,现取三支试管,先向其中各加入1mL相同浓度的KI溶液(含指示剂),再分别加入2 mol∙L−1的硫酸和一定量蒸馏水,其显色时间如下表所示:
(3)V2=_______ mL。通过实验Ⅰ、Ⅱ,本小组得出的实验结论为_______ 。
Ⅲ.如图石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各问题。
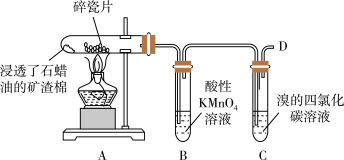
(4)B中溶液褪色,是因为乙烯被_______ 。
(5)C中溶液褪色,发生反应的化学方程式为_______ 。
(6)在D处点燃前必须进行的操作是_______ 。
I.从海水中提取食盐和溴的过程如下:

(1)步骤I中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为:
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为:
Ⅱ.实验:探究硫酸浓度对化学反应速率的影响
常温下,酸性KI溶液在空气中会被氧化为碘单质,现取三支试管,先向其中各加入1mL相同浓度的KI溶液(含指示剂),再分别加入2 mol∙L−1的硫酸和一定量蒸馏水,其显色时间如下表所示:
组别 | 硫酸/mL | 蒸馏水/mL | 显色时间/s |
i | 3 | 0 | 120 |
ii | 2 | V1 | 140 |
iii | 1 | V2 | 200 |
Ⅲ.如图石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各问题。

(4)B中溶液褪色,是因为乙烯被
(5)C中溶液褪色,发生反应的化学方程式为
(6)在D处点燃前必须进行的操作是
您最近一年使用:0次
解题方法
2 . 实验室用如图所示装置制取乙烯并验证其性质(加热及夹持仪器均省略)。请回答下列问题:
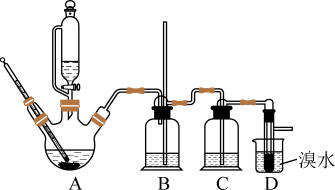
(1)写出仪器A中反应的化学方程式:_______ 。仪器A要迅速升温 到170℃,其原因是_______ (填序号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副反应的发生
(2)装置C中盛放的试剂是_______ ,作用是_______ 。
(3)实验完成时,D中现象是_______ 。

(1)写出仪器A中反应的化学方程式:
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副反应的发生
(2)装置C中盛放的试剂是
(3)实验完成时,D中现象是
您最近一年使用:0次
2022-04-28更新
|
424次组卷
|
2卷引用:新疆乌鲁木齐市第三十一中学2022-2023学年高二下学期4月期中化学试题
名校
3 . 1,2-二氯乙烷是制备杀菌剂和植物生长调节剂的中间体,在农业上可用作粮食、谷物的熏蒸剂、土壤消毒剂等。已知其沸点为83.5℃,熔点为-35℃。下图为实验室中制备1,2-二氯乙烷的装置,其中加热和夹持装置已略去。装置A中的无水乙醇的密度约为0.8 。
。
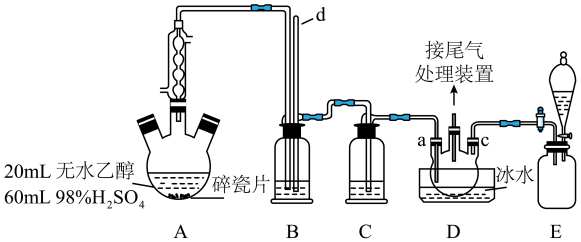
(1)装置A中还缺少的一种必要仪器是___________ ,使用冷凝管的目的是___________ ,装置A中发生主要反应的化学方程式为___________ 。
(2)装置B中玻璃管d的作用是___________ 。
(3)实验时A中三颈烧瓶内可能会产生一种刺激性气味的气体,为吸收该气体,在装置B中应加入的最佳试剂为___________。(填字母序号)。
(4)D中a、c两个导气管进入仪器中的长度不同,其优点是___________ 。
(5)实验结束后收集得到0.2 1,2-二氯乙烷,则乙醇的利用率为
1,2-二氯乙烷,则乙醇的利用率为___________ %(结果用小数表示)。
 。
。
(1)装置A中还缺少的一种必要仪器是
(2)装置B中玻璃管d的作用是
(3)实验时A中三颈烧瓶内可能会产生一种刺激性气味的气体,为吸收该气体,在装置B中应加入的最佳试剂为___________。(填字母序号)。
| A.浓硫酸 | B. 溶液 溶液 | C.酸性 溶液 溶液 | D.饱和 溶液 溶液 |
(5)实验结束后收集得到0.2
 1,2-二氯乙烷,则乙醇的利用率为
1,2-二氯乙烷,则乙醇的利用率为
您最近一年使用:0次
2022-01-21更新
|
832次组卷
|
7卷引用:题型180 气气反应型制备实验
名校
4 . 如图是石蜡油在炽热碎瓷片的作用下产乙烯并检验其性质的实验,完成下列问题。

(1)A中碎瓷片的作用是_______ 。
(2)写出乙烯的电子式_______ ,装置C中发生反应的化学方程式为_________ 。
(3)装置B中的现象是_______ 。
(4)下列物质中,可以由乙烯通过加成反应得到的是_______ (填字母代号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH
(5)由乙烯制聚乙烯的化学方程式:_______ ,聚乙烯的链节为_______ 。

(1)A中碎瓷片的作用是
(2)写出乙烯的电子式
(3)装置B中的现象是
(4)下列物质中,可以由乙烯通过加成反应得到的是
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH
(5)由乙烯制聚乙烯的化学方程式:
您最近一年使用:0次
2021-11-17更新
|
494次组卷
|
4卷引用:新疆阿克苏市实验中学2022-2023学年高一下学期第三次月考化学试题
解题方法
5 . 下图为甲同学设计的制取并检验C2H4性质的实验装置图。请回答有关问题:
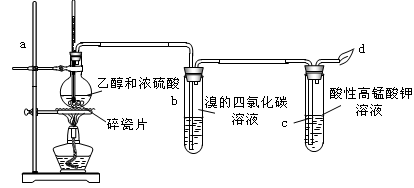
(1)写出上述制乙烯的反应的化学方程式:_______ ,
(2)加入几片碎瓷片的目的是_______ ,
(3)加热时,使混合液温度迅速升高到170℃,是为了_______ ,
(4)实验过程观察到的现象为:
①Br2的四氯化碳溶液由_______ 色变_______ ,
②酸性KMnO4溶液褪色。
(5)乙同学认为甲同学设计的实验如果仅从酸性KMnO4溶液褪色难以证明反应有乙烯生成,因为反应产生的乙烯中可能混有_______ 气体也能使酸性KMnO4溶液褪色。写出此气体使酸性KMnO4溶液褪色的离子方程式_______ 。

(1)写出上述制乙烯的反应的化学方程式:
(2)加入几片碎瓷片的目的是
(3)加热时,使混合液温度迅速升高到170℃,是为了
(4)实验过程观察到的现象为:
①Br2的四氯化碳溶液由
②酸性KMnO4溶液褪色。
(5)乙同学认为甲同学设计的实验如果仅从酸性KMnO4溶液褪色难以证明反应有乙烯生成,因为反应产生的乙烯中可能混有
您最近一年使用:0次
2021-04-26更新
|
318次组卷
|
2卷引用:北京市海淀区教师进修学校2022-2023学年高二下学期3月月考化学试题
6 . 某同学采用下列实验装置模拟工业制乙烯,并探究乙烯的主要化学性质。(已知烃类不与碱反应)回答下列问题:
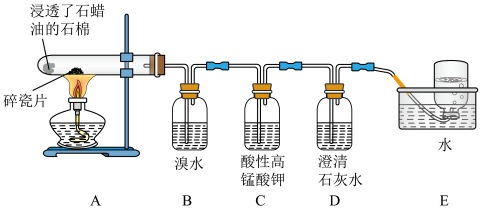
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应: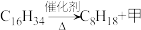 ,
,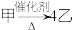 ,则甲的分子式为
,则甲的分子式为______ ,乙的结构简式为______ 。
(2) 装置中的实验现象可能是
装置中的实验现象可能是______ ,写出反应的化学方程式:______ ,其反应类型是______ 。
(3) 装置中可观察到的现象是
装置中可观察到的现象是______ ,反应类型是______ 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置______ (填装置序号)中的实验现象可判断该资料是否真实。
(5)通过上述实验探究,检验甲烷和乙烯的方法是______ (填序号,下同);除去甲烷中乙烯的方法是______ 。
A. 气体通入水中
B. 气体通过盛溴水的洗气瓶
C. 气体通过盛酸性高锰酸钾溶液的洗气瓶
D. 气体通过氢氧化钠溶液

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:
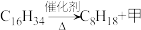 ,
,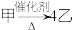 ,则甲的分子式为
,则甲的分子式为(2)
 装置中的实验现象可能是
装置中的实验现象可能是(3)
 装置中可观察到的现象是
装置中可观察到的现象是(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(5)通过上述实验探究,检验甲烷和乙烯的方法是
A. 气体通入水中
B. 气体通过盛溴水的洗气瓶
C. 气体通过盛酸性高锰酸钾溶液的洗气瓶
D. 气体通过氢氧化钠溶液
您最近一年使用:0次
2021-02-25更新
|
1009次组卷
|
4卷引用:2.2 烯烃、炔烃-同步学习必备知识
(已下线)2.2 烯烃、炔烃-同步学习必备知识江苏省无锡市市北高级中学2023-2024学年高二上学期10月阶段检测化学试题广东省珠海市2020-2021学年高二上学期期末考试化学试题(已下线)专题二 烯烃 炔烃-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修3)3月刊 (同步课堂必刷题)
名校
解题方法
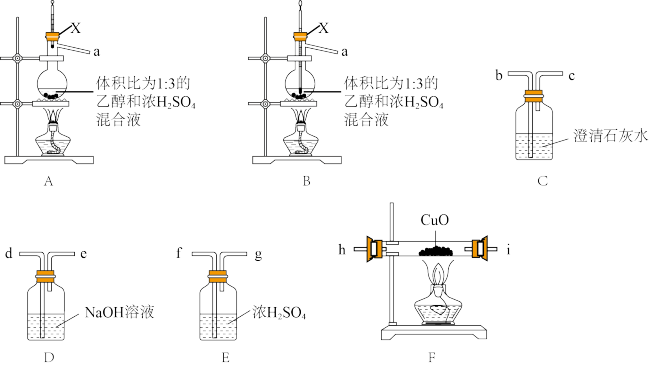
7 . 某学习小组欲用下列装置探究乙烯还原氧化铜。
已知:i.乙醇在170℃、浓硫酸的作用下能产生乙烯,方程式为CH3CH2OH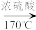 CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
ii.加热条件下,少量乙醇被浓硫酸碳化。
回答下列问题:
(1)仪器X的名称为___________ 。
(2)制备乙烯时应选用装置___________ (填“A”或“B”);反应开始后,仪器X中观察到的现象为___________ 。
(3)实验时装置的连接顺序是a→___________ →尾气处理(按气流方向,用小写字母表示);其中NaOH溶液的作用为___________ 。
(4)实验时,装置F应___________ (填“先加热”或“后加热”),原因为___________ 。
(5)能证明乙烯还原氧化铜的实验现象为___________ 。

已知:i.乙醇在170℃、浓硫酸的作用下能产生乙烯,方程式为CH3CH2OH
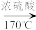 CH2=CH2↑+H2O;
CH2=CH2↑+H2O;ii.加热条件下,少量乙醇被浓硫酸碳化。
回答下列问题:
(1)仪器X的名称为
(2)制备乙烯时应选用装置
(3)实验时装置的连接顺序是a→
(4)实验时,装置F应
(5)能证明乙烯还原氧化铜的实验现象为
您最近一年使用:0次
2021-01-27更新
|
848次组卷
|
4卷引用:第一部分 二轮专题突破 大题突破2 综合实验题题型研究
(已下线)第一部分 二轮专题突破 大题突破2 综合实验题题型研究湖南省湘潭市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)01 常考题空1 常考仪器的辨认、选择与连接 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题
名校
8 . 实验室常用如图装置制取乙烯,反应原理为CH3CH2OH CH2
CH2 CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。
CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。______ 。
(2)制取时,关键要控制好温度。
①温度过高而发生副反应,生成________ 、________ 、水蒸气和炭黑。为了除水蒸气外的杂质气体,常用装有下列试剂的洗气瓶进行洗气,则应选用的试剂是____ 。
A.酸性KMnO4溶液B.浓硫酸C.NaOH溶液D.溴水
②要检验除水蒸气外的气体生成物,应该首先检验______ ,常选用的药品为______ 。
(3)制取时温度过低,在140℃时主要发生分子间取代反应生成乙醚(CH3CH2OCH2CH3),试写出其反应方程式:______________________________________________ 。
 CH2
CH2 CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。
CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。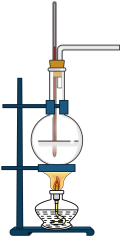
(2)制取时,关键要控制好温度。
①温度过高而发生副反应,生成
A.酸性KMnO4溶液B.浓硫酸C.NaOH溶液D.溴水
②要检验除水蒸气外的气体生成物,应该首先检验
(3)制取时温度过低,在140℃时主要发生分子间取代反应生成乙醚(CH3CH2OCH2CH3),试写出其反应方程式:
您最近一年使用:0次
2020-11-06更新
|
437次组卷
|
3卷引用:河北省石家庄市新乐市第一中学2022-2023学年高二下学期4月月考化学试题
河北省石家庄市新乐市第一中学2022-2023学年高二下学期4月月考化学试题吉林省长春市长春外国语学校2020-2021学年高二上学期期中考试化学(理科)试题(已下线)【教材实验热点】10 乙烯的实验室制取和性质探究
名校
9 . 某同学设计实验探究工业制乙烯的原理和乙烯主要的化学性质,实验装置如图所示。

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:
C16H34 C8H18+甲,甲
C8H18+甲,甲 4乙,C8H18
4乙,C8H18 C3H8+丙,
C3H8+丙,
则甲的分子式为__ ;丙的所有同分异构体中能够共面的碳原子最多有__ 个。
(2)B装置中的实验现象是____ ,其中发生反应的反应类型是_____ 。
(3)C装置中的实验现象是________ 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_____ (填序号)中的实验现象可判断该资料是否真实。
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是______ (填序号);除去甲烷中乙烯的方法是 __ (填序号)。
A.气体通入水中
B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,乙烯产生黑烟,原因是______ 。

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:
C16H34
 C8H18+甲,甲
C8H18+甲,甲 4乙,C8H18
4乙,C8H18 C3H8+丙,
C3H8+丙,则甲的分子式为
(2)B装置中的实验现象是
(3)C装置中的实验现象是
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是
A.气体通入水中
B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,乙烯产生黑烟,原因是
您最近一年使用:0次
2020-08-07更新
|
496次组卷
|
3卷引用:河南省栾川县第一高级中学2022-2023学年高一下学期6月阶段测试化学试题
河南省栾川县第一高级中学2022-2023学年高一下学期6月阶段测试化学试题江西省宜春市上高县第二中学2019-2020学年高一下学期期末考试化学试题(已下线)【教材实验热点】10 乙烯的实验室制取和性质探究
10 . 某同学设计实验探究工业制乙烯的原理和乙烯主要的化学性质,实验装置如图所示。
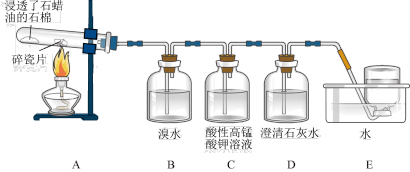
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34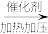 C8H18+甲,甲
C8H18+甲,甲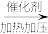 4乙,则甲的分子式为
4乙,则甲的分子式为______ ;乙的结构简式为____ 。
(2)B装置中的实验现象是______ 。
(3)C装置中的实验现象是_____ ,其中发生反应的反应类型是___ 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_ (填序号)中的实验现象可判断该资料是否真实。
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是_____ (填序号,下同);除去甲烷中乙烯的方法是____ 。
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,乙烯产生黑烟,原因是_____ 。

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34
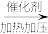 C8H18+甲,甲
C8H18+甲,甲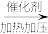 4乙,则甲的分子式为
4乙,则甲的分子式为(2)B装置中的实验现象是
(3)C装置中的实验现象是
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,乙烯产生黑烟,原因是
您最近一年使用:0次
2020-06-29更新
|
288次组卷
|
3卷引用:山东省滕州市第五中学2022-2023学年高一下学期5月月考化学试题



