河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题
河南
高三
阶段练习
2021-02-23
269次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学实验基础、认识化学科学、化学反应原理、物质结构与性质
河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题
河南
高三
阶段练习
2021-02-23
269次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学实验基础、认识化学科学、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
解题方法
1. 化学与人类生活密切相关,下列叙述错误的是
| A.向煤中添加生石灰可以降低温室气体的排放 |
| B.小苏打可作发酵剂、灭火剂 |
| C.体积分数为75%的乙醇抑菌、消毒效果最好 |
| D.高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂 |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
解题方法
2. 下列关于基本营养物质的描述正确的是
| A.淀粉和纤维素的化学式均为(C6H12O6)n |
| B.油脂分子量越大熔点一定越高 |
| C.可通过灼烧的方法鉴别蛋白质和纤维素 |
| D.麦芽糖能在人体内水解成葡萄糖和果糖 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
5. 下表各组物质之间能实现如图所示转化的是


| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | CH4 | CH3Cl | CH2Cl2 | Cl2 |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | NaHCO3 | Na2CO3 | CO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-27更新
|
121次组卷
|
2卷引用:河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题
单选题
|
适中(0.65)
名校
6. 常温下,下列离子在指定溶液中一定能大量共存的是
A.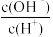 =10-9的溶液中:Na+、Mg2+、 =10-9的溶液中:Na+、Mg2+、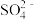 、Cl- 、Cl- |
B.0.1 mol·L-1NaHCO3溶液中:K+、Al3+、Cl-、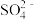 |
| C.0.1 mol·L-1KNO3溶液中:Na+、H+、Cl-、I- |
D.pH=5的溶液中:K+、Fe3+、 、 、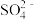 |
【知识点】 限定条件下的离子共存解读
您最近一年使用:0次
2021-01-27更新
|
125次组卷
|
2卷引用:河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题
单选题
|
容易(0.94)
名校
7. 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.18.0 g葡萄糖和果糖的混合物中含有氢原子的数目为1.2 NA |
| B.pH=13的NaOH溶液中所含OH-的数目为0.1 NA |
| C.11.2 L O2(标准状况)与足量SO2混合反应后转移电子的数目为2 NA |
| D.0.1 mol Fe与足量Cl2完全反应转移电子的数目为0.2 NA |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
8. 2,3—二氢呋喃( )和环丙甲醛(
)和环丙甲醛( )都是有机合成中重要的中间体。下列说法错误的是
)都是有机合成中重要的中间体。下列说法错误的是
 )和环丙甲醛(
)和环丙甲醛( )都是有机合成中重要的中间体。下列说法错误的是
)都是有机合成中重要的中间体。下列说法错误的是| A.环丙甲醛中所有碳原子可能处于同一平面 |
| B.2,3—二氢呋喃可发生加成反应和取代反应 |
| C.等质量的二者完全燃烧,耗氧量相等 |
| D.2,3—二氢呋喃的二氯取代物有8种(不包含立体异构) |
您最近一年使用:0次
单选题
|
较易(0.85)
9. 反应2SO2(g)+O2(g)  2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是
2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是
 2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是
2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是| A.反应物的总能量高于生成物的总能量 |
| B.催化剂可以降低硫氧键键能 |
| C.加压有利于SO3生成,所以工业上压强越高越好 |
| D.升高温度可以增大正反应速率,降低逆反应速率 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
10. 短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y同主族,W原子的最外层电子数是电子层数的3倍。X和Z两种元素形成的化合物是厨房常用的食品调味剂和防腐剂。下列说法正确的是
| A.X的简单离子半径是同周期简单离子中最大的 |
| B.W、Y在自然界中均存在游离态 |
| C.工业上常用电解X和Z形成化合物的水溶液冶炼X单质 |
| D.W、Y、Z的简单氢化物中,同条件下Y的沸点最高 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
11. 碳酸锰(MnCO3)是生产电讯器材用铁氧体的原料。利用软锰矿(主要成分为MnO2,还含有少量Al2O3和SiO2等杂质)合成碳酸锰的流程如下:

下列说法错误的是

下列说法错误的是
| A.“滤液1”的成分为NaAlO2、Na2SiO3和NaOH |
B.“沉锰”时发生的离子方程式为:Mn2++ =MnCO3+H+ =MnCO3+H+ |
| C.取最后一次洗涤液少许,滴加氯化钡可检验产品是否洗涤干净 |
| D.实验室中“过滤、洗涤”操作均用到漏斗 |
【知识点】 含氧化铝的混合物的提纯解读 物质分离、提纯综合应用解读
您最近一年使用:0次
12. 下列对实验事实的解释错误的是
| 选项 | 实验事实 | 解释 |
| A | 用盐酸滴定未知浓度的NaOH溶液,滴定至终点时仰视读数使滴定结果浓度偏高 | 读取标准液体积偏大 |
| B | 用标准AgNO3溶液滴定溶液中Cl-时,标准液盛放在棕色滴定管中 | AgNO3见光分解 |
| C | 向10 mL0.5 mol·L-1MgCl2溶液中加入10 mL2.0 mol·L-1NaOH溶液,产生白色沉淀,再滴加CuCl2溶液,沉淀变蓝 | Ksp[ Cu(OH)2 ]<KSP[Mg(OH)2] |
| D | KMnO4受热分解制氧气的试管,可用热的浓盐酸洗去不溶性黑色固体 | MnO2能溶于热的浓盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
13. 随着电化学技术的发展和成熟,利用电解池合成的物种也越来越多。利用电化学法制备己二腈 [NC(CH2)4CN]的原理如图所示。下列说法正确的是


| A.电极C(Ⅰ)为阴极 |
| B.若交换膜为阴离子交换膜,可维持两极区溶液浓度基本不变 |
| C.电解过程中阴极附近pH增大 |
| D.电极C(Ⅱ)上的电极反应式为2CH2=CHCN+2H2O+2e-=NC(CH2)4CN+2OH- |
【知识点】 电解原理
您最近一年使用:0次
单选题
|
适中(0.65)
名校
14. 25℃时,向20.00 mL 0.1 mol·L-1H2X溶液中滴入0.1 mol·L-1NaOH溶液,溶液中由水电离出的 (OH-)的负对数[-lgc水(OH-)]与所加NaOH溶液体积的关系如图所示。下列说法中错误的是
(OH-)的负对数[-lgc水(OH-)]与所加NaOH溶液体积的关系如图所示。下列说法中错误的是

 (OH-)的负对数[-lgc水(OH-)]与所加NaOH溶液体积的关系如图所示。下列说法中错误的是
(OH-)的负对数[-lgc水(OH-)]与所加NaOH溶液体积的关系如图所示。下列说法中错误的是
| A.M点时:c(X2-)>c(H2X) |
| B.N点时:pH=7 |
| C.P点时:c(Na+)>c(X2-)>c(HX-)>c(OH-)>c(H+) |
| D.水的电离程度:P>Q>M |
【知识点】 盐溶液中离子浓度大小的比较解读
您最近一年使用:0次
2021-01-27更新
|
196次组卷
|
2卷引用:广东省肇庆市2020-2021学年高二上学期期末教学质量检测化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
15. 某学习小组欲用下列装置探究乙烯还原氧化铜。
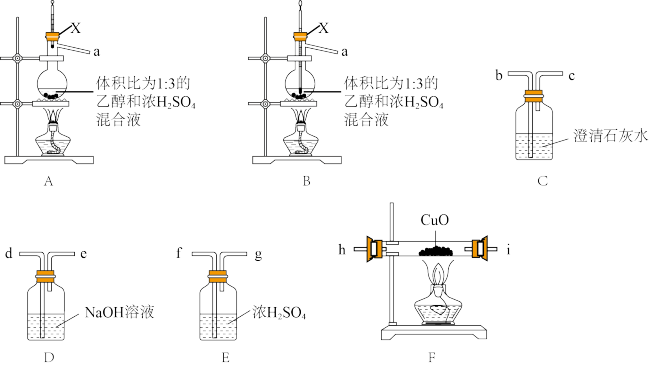
已知:i.乙醇在170℃、浓硫酸的作用下能产生乙烯,方程式为CH3CH2OH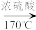 CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
ii.加热条件下,少量乙醇被浓硫酸碳化。
回答下列问题:
(1)仪器X的名称为___________ 。
(2)制备乙烯时应选用装置___________ (填“A”或“B”);反应开始后,仪器X中观察到的现象为___________ 。
(3)实验时装置的连接顺序是a→___________ →尾气处理(按气流方向,用小写字母表示);其中NaOH溶液的作用为___________ 。
(4)实验时,装置F应___________ (填“先加热”或“后加热”),原因为___________ 。
(5)能证明乙烯还原氧化铜的实验现象为___________ 。

已知:i.乙醇在170℃、浓硫酸的作用下能产生乙烯,方程式为CH3CH2OH
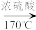 CH2=CH2↑+H2O;
CH2=CH2↑+H2O;ii.加热条件下,少量乙醇被浓硫酸碳化。
回答下列问题:
(1)仪器X的名称为
(2)制备乙烯时应选用装置
(3)实验时装置的连接顺序是a→
(4)实验时,装置F应
(5)能证明乙烯还原氧化铜的实验现象为
您最近一年使用:0次
2021-01-27更新
|
841次组卷
|
4卷引用:河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题
河南省沈丘县第一高级中学2021届高三尖子生12月调研考试化学试题(已下线)第一部分 二轮专题突破 大题突破2 综合实验题题型研究湖南省湘潭市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)01 常考题空1 常考仪器的辨认、选择与连接 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
16. 某工业废料中主要含CoO、Fe3O4、Al2O3、NiO、SiO2等,现欲利用以下工业流程回收某些金属资源。

已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
②空气中氧气的体积分数为20%。
回答下列问题:
(1)“粉碎”的目的为___________ 。
(2)“滤渣1”为___________ ;“氧化”过程中温度控制在40℃,温度避免过高和过低,原因为___________ 。
(3)调pH的范围为___________ ;流程中可循环利用的物质为___________ 。
(4)“沉铝”过程中反应的离子方程式为___________ 。
(5)“煅烧”过程中,每制备1 mol CoO,至少需要标准状况下的空气体积为___________ L。
(6)某新型富钴电池的电解液为ZnSO4和CoSO4的混合溶液。已知放电时正极上Co3O4转化为CoO,则放电过程中正极的电极反应式为___________ 。

已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀的pH | 7.5 | 2.2 | 4.1 | 6.4 | 9.0 |
| 完全沉淀的pH | 9.5 | 3.5 | 5.4 | 8.4 | 11.0 |
回答下列问题:
(1)“粉碎”的目的为
(2)“滤渣1”为
(3)调pH的范围为
(4)“沉铝”过程中反应的离子方程式为
(5)“煅烧”过程中,每制备1 mol CoO,至少需要标准状况下的空气体积为
(6)某新型富钴电池的电解液为ZnSO4和CoSO4的混合溶液。已知放电时正极上Co3O4转化为CoO,则放电过程中正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易(0.85)
名校
解题方法
17. 研究氮的固定及含氮化合物的转化对工农业发展及消除环境污染有重要的意义。
已知:Ⅰ.N2(g)+3H2(g) 2NH3(g) △H1=-92.4 kJ·mol-1;
2NH3(g) △H1=-92.4 kJ·mol-1;
Ⅱ.N2(g)+O2(g) 2NO(g) △H2=+180 kJ·mol-1;
2NO(g) △H2=+180 kJ·mol-1;
Ⅲ.2NO(g)+O2(g) 2NO2(g) △H3=-112.3 kJ·mol-1。
2NO2(g) △H3=-112.3 kJ·mol-1。
请回答下列问题:
(1)反应Ⅰ是工业固氮的重要反应,在体积为2 L的恒温恒容密闭容器中,充入1 mol N2和3 mol H2,5 min末达到平衡,此时容器内压强变为原来的0.75倍。
①下列事实可以判断该反应达到平衡状态的是___________ 。
a.相同时间内每消耗0.1 mol N2的同时消耗0.2 mol NH3
b.c(N2):c(H2)=1:3
c.混合气体的密度不再发生变化时
d.氢气的分压不再发生变化时
②5 min内该反应的反应速率v(N2)=___________ 。
③若将容器扩大一倍,再次平衡后该反应的化学平衡常数会___________ (填“增大”“减小”或“不变”,下同),N2和H2的转化率之比α(N2):α(H2)会___________ 。
(2)反应N2(g)+2O2(g)=2NO2(g) △H=___________ 。
(3)反应Ⅲ是由以下两步反应完成:
i.___________ △H4<0;
ii.N2O2(g)+O2(g) 2NO2(g) △H5<0。
2NO2(g) △H5<0。
①第i步反应的化学方程式为___________ 。
②△H4___________ 112.3 kJ·mol-1(填“>”“=”或“<”,下同);若第i步反应为快反应,则活化能E(i)___________ E(ii)。
③若反应ii的正反应速率 =
=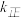 ×c(N2O2)·c(O2),
×c(N2O2)·c(O2),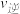 =
=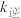 ×c2(NO2);则该反应的化学平衡常数K=
×c2(NO2);则该反应的化学平衡常数K=___________ (用含“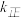 ”和“
”和“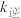 ”的代数式表示)。
”的代数式表示)。
已知:Ⅰ.N2(g)+3H2(g)
 2NH3(g) △H1=-92.4 kJ·mol-1;
2NH3(g) △H1=-92.4 kJ·mol-1;Ⅱ.N2(g)+O2(g)
 2NO(g) △H2=+180 kJ·mol-1;
2NO(g) △H2=+180 kJ·mol-1;Ⅲ.2NO(g)+O2(g)
 2NO2(g) △H3=-112.3 kJ·mol-1。
2NO2(g) △H3=-112.3 kJ·mol-1。请回答下列问题:
(1)反应Ⅰ是工业固氮的重要反应,在体积为2 L的恒温恒容密闭容器中,充入1 mol N2和3 mol H2,5 min末达到平衡,此时容器内压强变为原来的0.75倍。
①下列事实可以判断该反应达到平衡状态的是
a.相同时间内每消耗0.1 mol N2的同时消耗0.2 mol NH3
b.c(N2):c(H2)=1:3
c.混合气体的密度不再发生变化时
d.氢气的分压不再发生变化时
②5 min内该反应的反应速率v(N2)=
③若将容器扩大一倍,再次平衡后该反应的化学平衡常数会
(2)反应N2(g)+2O2(g)=2NO2(g) △H=
(3)反应Ⅲ是由以下两步反应完成:
i.
ii.N2O2(g)+O2(g)
 2NO2(g) △H5<0。
2NO2(g) △H5<0。①第i步反应的化学方程式为
②△H4
③若反应ii的正反应速率
 =
=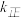 ×c(N2O2)·c(O2),
×c(N2O2)·c(O2),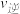 =
=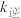 ×c2(NO2);则该反应的化学平衡常数K=
×c2(NO2);则该反应的化学平衡常数K=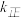 ”和“
”和“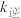 ”的代数式表示)。
”的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
名校
解题方法
18. 钛单质及其化合物在医疗器械和军工业生产中有重要应用。
(1)基态钛原子核外电子排布式为___________ ;同周期与其未成对电子数相等的基态原子还有___________ 种。
(2)氢氟酸是钛的最强溶剂,可发生反应:Ti+4HF=TiF4+2H2↑。
①上述反应涉及的三种元素电负性由强到弱的顺序为___________ 。
②HF和HCl相比较,沸点较高的是___________ ,原因为___________ 。
(3)钛酸钡(BaTiO3)被誉为“电子陶瓷工业的支柱”,其制备原理为BaTiO(C2O4)2·4H2O BaTiO3+2CO↑+2CO2↑+4H2O。
BaTiO3+2CO↑+2CO2↑+4H2O。
①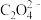 中碳原子的杂化方式为
中碳原子的杂化方式为___________ ;CO2分子的空间构型为___________ 。
②钛酸钡(BaTiO3)的晶胞为立方晶胞,结构如下图。其中部分原子坐标为W(0,0, 0)、M(1/2,1/2,1/2)、N(1/2,0,0)。

晶胞中Ba与Ti的配位数分别为___________ 、___________ ;X点的坐标为___________ ;若晶胞参数为a pm,则该晶胞的密度为___________ (NA表示阿伏加德罗常数的值,列出代数式)g·cm-3。
(1)基态钛原子核外电子排布式为
(2)氢氟酸是钛的最强溶剂,可发生反应:Ti+4HF=TiF4+2H2↑。
①上述反应涉及的三种元素电负性由强到弱的顺序为
②HF和HCl相比较,沸点较高的是
(3)钛酸钡(BaTiO3)被誉为“电子陶瓷工业的支柱”,其制备原理为BaTiO(C2O4)2·4H2O
 BaTiO3+2CO↑+2CO2↑+4H2O。
BaTiO3+2CO↑+2CO2↑+4H2O。①
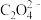 中碳原子的杂化方式为
中碳原子的杂化方式为②钛酸钡(BaTiO3)的晶胞为立方晶胞,结构如下图。其中部分原子坐标为W(0,0, 0)、M(1/2,1/2,1/2)、N(1/2,0,0)。

晶胞中Ba与Ti的配位数分别为
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
名校
19. H( )是一种抗痉挛药物的合成中间体,实验室制备H的一种合成路线如下:
)是一种抗痉挛药物的合成中间体,实验室制备H的一种合成路线如下:

已知:I.
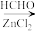

II.RCN RCOOH
RCOOH
III. RCN RCH2NH2(R为烃基)
RCH2NH2(R为烃基)
回答下列问题:
(1)A的化学名称为___________ ,H的分子式是___________ 。
(2)反应①和反应②的反应类型分别为___________ 、___________ 。
(3)F中所含官能团的名称为___________ 。
(4)反应⑦的化学方程式为___________ 。
(5)满足下列条件的D的同分异构体的结构简式为___________ 。
i.苯环上含三个取代基,其中两个为羟基; ii.核磁共振氢谱有4组峰。
(6)根据上述信息写出以乙醇为原料制备丙酸乙酯的合成路线:___________ 。(无机试剂任选)
 )是一种抗痉挛药物的合成中间体,实验室制备H的一种合成路线如下:
)是一种抗痉挛药物的合成中间体,实验室制备H的一种合成路线如下:
已知:I.

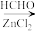

II.RCN
 RCOOH
RCOOHIII. RCN
 RCH2NH2(R为烃基)
RCH2NH2(R为烃基)回答下列问题:
(1)A的化学名称为
(2)反应①和反应②的反应类型分别为
(3)F中所含官能团的名称为
(4)反应⑦的化学方程式为
(5)满足下列条件的D的同分异构体的结构简式为
i.苯环上含三个取代基,其中两个为羟基; ii.核磁共振氢谱有4组峰。
(6)根据上述信息写出以乙醇为原料制备丙酸乙酯的合成路线:
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学实验基础、认识化学科学、化学反应原理、物质结构与性质
试卷题型(共 19题)
题型
数量
单选题
14
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 二氧化硫与二氧化碳的性质区别 碳酸氢钠的俗称、物理性质及用途 高铁酸钠 | |
| 2 | 0.94 | 油脂 糖类综合 淀粉和纤维素 蛋白质 | |
| 3 | 0.94 | 配制一定物质的量浓度的溶液实验的仪器 | |
| 4 | 0.94 | 氧化还原反应基本概念 | |
| 5 | 0.85 | 碳酸氢钠 铝与强碱溶液反应 铁与非金属单质反应 甲烷的取代反应 | |
| 6 | 0.65 | 限定条件下的离子共存 | |
| 7 | 0.94 | 阿伏加德罗常数的应用 铁与非金属单质反应 pH定义式及计算 葡萄糖、果糖的组成与结构 | |
| 8 | 0.85 | 有机反应类型 同分异构体的数目的确定 有机分子中原子共面的判断 | |
| 9 | 0.85 | 化学反应中热量(Q)及(△H)相关判断 温度对化学反应速率的影响 催化剂对化学反应速率的影响 压强对化学平衡移动的影响 | |
| 10 | 0.65 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | |
| 11 | 0.85 | 含氧化铝的混合物的提纯 物质分离、提纯综合应用 | |
| 12 | 0.65 | 氯气的实验室制法 酸碱中和滴定 溶度积 | |
| 13 | 0.65 | 电解原理 | |
| 14 | 0.65 | 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 15 | 0.65 | 乙烯的制备实验 常见气体的制备与收集 物质性质的探究 综合实验设计与评价 | 实验探究题 |
| 16 | 0.65 | 含氧化铝的混合物的提纯 Fe2+的还原性 电解原理 常见无机物的制备 | 工业流程题 |
| 17 | 0.85 | 化学反应速率计算 化学平衡的有关计算 化学平衡状态的判断方法 化学平衡常数的概念及表达方式 | 原理综合题 |
| 18 | 0.4 | 元素性质与电负性的关系 杂化轨道理论 价层电子对互斥理论的应用 晶胞的有关计算 | 结构与性质 |
| 19 | 0.65 | 有机反应类型 含有苯环的化合物的命名 同分异构体书写 根据题给物质选择合适合成路线 | 有机推断题 |







