真题
解题方法
1 . 实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
A.稀盐酸:配制 溶液 溶液 |
| B.稀硫酸:蔗糖和淀粉的水解 |
| C.稀硝酸:清洗附有银镜的试管 |
| D.浓硫酸和浓硝酸的混合溶液:苯的磺化 |
您最近一年使用:0次
2023-06-19更新
|
7188次组卷
|
10卷引用:2023年高考山东卷化学真题
2023年高考山东卷化学真题(已下线)2023年高考山东卷化学真题变式题(选择题1-5)(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)第36讲生物大分子和合成高分子(已下线)考点4 生物大分子和合成高分子(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)FHgkyldyjhx14浙江省2024届高三下学期5月选考适应性考试化学试题
名校
2 . 云南大学钱德云课题组最近合成一种用途广泛的手性N—烷基吲哚分子。反应历程如图所示:


已知:图示中 、
、 、R等表示烃基或氢原子且均不相同。下列叙述错误的是
、R等表示烃基或氢原子且均不相同。下列叙述错误的是


已知:图示中
 、
、 、R等表示烃基或氢原子且均不相同。下列叙述错误的是
、R等表示烃基或氢原子且均不相同。下列叙述错误的是| A.物质A是总反应的催化剂 |
| B.物质3分子含手性碳原子 |
| C.上述总反应为取代反应 |
| D.上述转化中Ni形成的共价键数目发生了变化 |
您最近一年使用:0次
名校
解题方法
3 . 苯胺(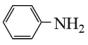 )是重要的化工原料,其制备原理为:
)是重要的化工原料,其制备原理为:
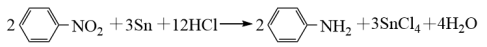
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐 。
。
乙醚为极易挥发的液体,是用途广泛的有机溶剂,与空气接触会形成易爆混合物。部分物质物理性质见表:
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为_______ 。
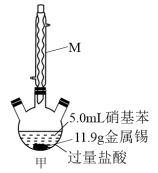
(2)图甲中 装置的名称为
装置的名称为_______ ,往硝基苯中加入 和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量
和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量 溶液得碱化液。加
溶液得碱化液。加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为_______ 。
(3)分离提纯:
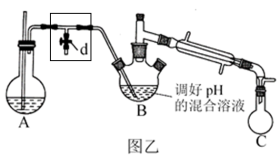
步骤i.如图乙,加热装置 产生水蒸气,采用水蒸气蒸馏的方法,用
产生水蒸气,采用水蒸气蒸馏的方法,用热的水蒸气 将 中的苯胺逐渐吹出至
中的苯胺逐渐吹出至 中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
步骤ⅱ.步骤i所得水溶液中加 至饱和,用乙醚萃取得萃取液与粗苯胺合并。
至饱和,用乙醚萃取得萃取液与粗苯胺合并。
步骤ⅲ.合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度T时的馏分得到苯胺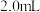 。
。
①图乙中T型管 处方框区域玻璃导管不宜过长,原因是
处方框区域玻璃导管不宜过长,原因是_______ 。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是_______ 。步骤ⅲ中干燥剂可以选用_______ (填序号)
a.浓硫酸 b.五氧化二磷 c.碱石灰
③步骤ⅲ中蒸馏获得苯胺需控制温度为_______ 左右。
④该实验中所得苯胺的产率为_______ (保留三位有效数字)。
 )是重要的化工原料,其制备原理为:
)是重要的化工原料,其制备原理为: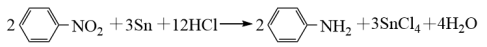
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐
 。
。乙醚为极易挥发的液体,是用途广泛的有机溶剂,与空气接触会形成易爆混合物。部分物质物理性质见表:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 溶解性 | 密度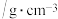 |
| 苯胺 | 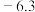 | 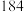 |  | 微溶于水,易溶于乙醚 |  |
| 硝基苯 | 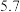 | 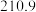 | 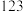 | 难溶于水,易溶于乙醚 | 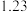 |
| 乙醚 | 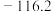 | 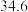 |  | 微溶于水 | 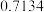 |
(1)实验室用苯制取硝基苯的化学方程式为
(2)图甲中
 装置的名称为
装置的名称为 和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量
和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量 溶液得碱化液。加
溶液得碱化液。加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为
(3)分离提纯:

步骤i.如图乙,加热装置
 产生水蒸气,采用水蒸气蒸馏的方法,用
产生水蒸气,采用水蒸气蒸馏的方法,用 中的苯胺逐渐吹出至
中的苯胺逐渐吹出至 中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。步骤ⅱ.步骤i所得水溶液中加
 至饱和,用乙醚萃取得萃取液与粗苯胺合并。
至饱和,用乙醚萃取得萃取液与粗苯胺合并。步骤ⅲ.合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度T时的馏分得到苯胺
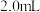 。
。①图乙中T型管
 处方框区域玻璃导管不宜过长,原因是
处方框区域玻璃导管不宜过长,原因是②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是
a.浓硫酸 b.五氧化二磷 c.碱石灰
③步骤ⅲ中蒸馏获得苯胺需控制温度为
④该实验中所得苯胺的产率为
您最近一年使用:0次
4 . 硝基苯是重要的化工原料,用途广泛。
I.制备硝基苯的化学反应方程式如下:
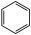 +HO-NO2
+HO-NO2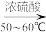
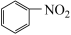 +H2O
+H2O
II.可能用到的有关数据列表如下:
III.制备硝基苯的反应装置图如下:
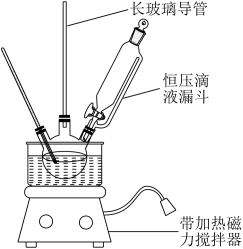
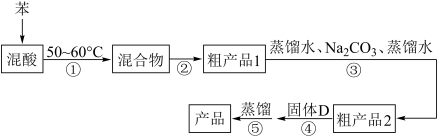
IV .制备、提纯硝基苯的流程如下:
请回答下列问题:
(1)配制混酸时,应在烧杯中先加入___________ ;反应装置中的长玻璃导管最好用___________ 代替(填仪器名称);恒压滴液漏斗的优点是___________ 。
(2)步骤①反应温度控制在50~60°C的主要原因是___________ ;步骤②中分离混合物获得粗产品1的实验操作名称是___________ 。
(3)最后一次水洗后分液得到粗产品2时,粗产品2应___________ (填“a” 或“b”)。
a.从分液漏斗上口倒出 b.从分液漏斗下口放出
b.从分液漏斗下口放出
(4)粗产品1呈浅黄色,粗产品2为无色。粗产品1呈浅黄色的原因是___________ 。
(5)步骤④用到的固体D的名称为___________ 。
(6)步骤⑤蒸馏操作中,锥形瓶中收集到的物质为___________ 。
I.制备硝基苯的化学反应方程式如下:
 +HO-NO2
+HO-NO2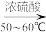
 +H2O
+H2OII.可能用到的有关数据列表如下:
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | ___ | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | ___ | 338 | 1.84 | 易溶于水 |

IV .制备、提纯硝基苯的流程如下:

请回答下列问题:
(1)配制混酸时,应在烧杯中先加入
(2)步骤①反应温度控制在50~60°C的主要原因是
(3)最后一次水洗后分液得到粗产品2时,粗产品2应
a.从分液漏斗上口倒出
 b.从分液漏斗下口放出
b.从分液漏斗下口放出(4)粗产品1呈浅黄色,粗产品2为无色。粗产品1呈浅黄色的原因是
(5)步骤④用到的固体D的名称为
(6)步骤⑤蒸馏操作中,锥形瓶中收集到的物质为
您最近一年使用:0次
2021-03-14更新
|
2122次组卷
|
5卷引用:吉林省长春市普通高中2021届高三质量监测(二)(二模)理综化学试题
吉林省长春市普通高中2021届高三质量监测(二)(二模)理综化学试题宁夏石嘴山市2021届高三下学期3月高考质量监测(一模) 化学试题(已下线)第30讲 常见的烃——甲烷、乙烯、苯(精练)-2022年高考化学一轮复习讲练测(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)第二节 研究有机化合物的一般方法 第1课时 有机化合物的分类、提纯
5 . 非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛。
(1)O2-的离子结构示意图为__________ ,CS2的晶体类型为________ 晶体;
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例________ (写化学式,任写两种);
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是______________________________ ;
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用___________________________ 。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是________________ 。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于___________ 。
(5)镁是一种较活泼的金属,Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体。该气体被溴水全部吸收后,溴水增重2.6g。请写出该水解反应方程式__________________________ 。
(1)O2-的离子结构示意图为
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
| 危险性 |  |
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于
(5)镁是一种较活泼的金属,Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体。该气体被溴水全部吸收后,溴水增重2.6g。请写出该水解反应方程式
您最近一年使用:0次



