名校
解题方法
1 . 环己酮可作为涂料和油漆的溶剂。在实验室中以环己醇为原料制备环己酮。
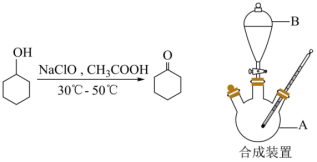
已知:①环己醇、环己酮、醋酸的部分物理性质如下表:
②两种互不相溶的液体,密度相差越大分层越易发生。
回答下列问题:
(1)B装置的名称是___________ 。
(2)酸化NaClO时一般不选用盐酸,原因是___________ (用离子方程式表示)。
(3)该制备反应很剧烈,且放出大量的热。为控制反应体系温度在30~35℃范围内,可采取的加热方式是___________ 。
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮、水和___________ (填写化学式)的混合物。
(5)环己酮的提纯过程为:
①在馏分中加NaCl固体至饱和,静置,分液;加NaCl的目的是___________ 。
②加入无水MgSO4块状固体;目的是___________ 。
③___________ (填操作名称)后进行蒸馏,收集150~155℃的馏分。
(6)数据处理。反应开始时加入8.4mL(0.08mol)环己醇,20mL冰醋酸和过量的NaClO溶液。实验结束后收集到产品0.06mol,则该合成反应的产率为____________ 。

已知:①环己醇、环己酮、醋酸的部分物理性质如下表:
| 物质 | 沸(熔)点/(℃,1atm) | 密度/(g/cm3) | 溶解性 |
| 环己醇 | 161.1( 21) 21) | 0.96 | 能溶于水,易溶于常见有机溶剂 |
| 环己酮 | 155.6( 47) 47) | 0.94 | 微溶于水 |
| 醋酸 | 118(16.6) | 1.05 | 易溶于水 |
回答下列问题:
(1)B装置的名称是
(2)酸化NaClO时一般不选用盐酸,原因是
(3)该制备反应很剧烈,且放出大量的热。为控制反应体系温度在30~35℃范围内,可采取的加热方式是
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮、水和
(5)环己酮的提纯过程为:
①在馏分中加NaCl固体至饱和,静置,分液;加NaCl的目的是
②加入无水MgSO4块状固体;目的是
③
(6)数据处理。反应开始时加入8.4mL(0.08mol)环己醇,20mL冰醋酸和过量的NaClO溶液。实验结束后收集到产品0.06mol,则该合成反应的产率为
您最近一年使用:0次
2024-01-13更新
|
652次组卷
|
5卷引用:四川省成都七中万达学校2023-2024学年高三上学期第一次诊断化学试卷
四川省成都七中万达学校2023-2024学年高三上学期第一次诊断化学试卷2024届四川省成都市第七中学高三上学期一诊模拟考试理科综合试卷(已下线)实验综合题(已下线)化学(九省联考考后提升卷,吉林、黑龙江卷)-2024年1月“九省联考”真题完全解读与考后提升四川省遂宁市射洪市四川省射洪中学校2023-2024学年高三下学期开学理综试题-高中化学
名校
解题方法
2 . 常温下,二甲基亚砜(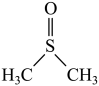 )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸占为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸占为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
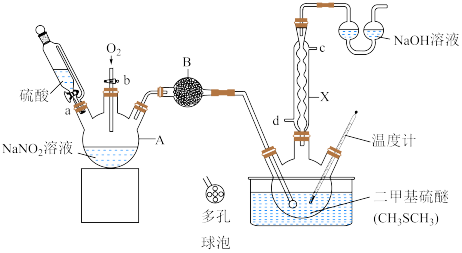
已知:①制备二甲基亚砜的反应原理为NO2+CH3SCH3
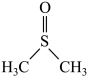 +NO。
+NO。
②二甲基硫醚(CH3SCH3)和二甲基亚砜的密度分别为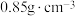 和
和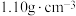 。
。
③ 遇微热易分解为
遇微热易分解为 、
、 和水。
和水。
实验过程:将 仪器中制得的气体通入
仪器中制得的气体通入 二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到
二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到 二甲基亚砜纯品。回答下列问题:
二甲基亚砜纯品。回答下列问题:
(1) 的名称为
的名称为___________ ;仪器 的进水口为
的进水口为______ (填“ ”或“
”或“ ”)口;
”)口; 中盛放的试剂的目的是干燥
中盛放的试剂的目的是干燥 ,则
,则 中盛放的试剂可能是
中盛放的试剂可能是___________ (填名称)。
(2)通常采用水浴加热来控制温度为60~80℃,该方法的优点是___________ 。
(3)实验中 需过量的原因是
需过量的原因是___________ 。
(4) 溶液吸收尾气中
溶液吸收尾气中 和
和 的化学方程式为
的化学方程式为___________ ,该反应中m(氧化剂):m(还原剂)=___________ 。
(5)本实验的产率是___________ (保留2位小数)%。
 )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸占为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸占为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
已知:①制备二甲基亚砜的反应原理为NO2+CH3SCH3

 +NO。
+NO。②二甲基硫醚(CH3SCH3)和二甲基亚砜的密度分别为
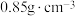 和
和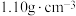 。
。③
 遇微热易分解为
遇微热易分解为 、
、 和水。
和水。实验过程:将
 仪器中制得的气体通入
仪器中制得的气体通入 二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到
二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到 二甲基亚砜纯品。回答下列问题:
二甲基亚砜纯品。回答下列问题:(1)
 的名称为
的名称为 的进水口为
的进水口为 ”或“
”或“ ”)口;
”)口; 中盛放的试剂的目的是干燥
中盛放的试剂的目的是干燥 ,则
,则 中盛放的试剂可能是
中盛放的试剂可能是(2)通常采用水浴加热来控制温度为60~80℃,该方法的优点是
(3)实验中
 需过量的原因是
需过量的原因是(4)
 溶液吸收尾气中
溶液吸收尾气中 和
和 的化学方程式为
的化学方程式为(5)本实验的产率是
您最近一年使用:0次
名校
解题方法
3 . 2-甲基-2-丁醇是一种重要的有机化合物,可用于合成香料、农药等。某化学兴趣小组欲利用格氏试剂法制备2-甲基-2-丁醇。实验原理及具体操作步骤如下:
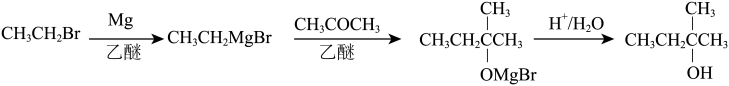
Ⅰ.乙基溴化镁的制备
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产率。
已知:①RMgBr化学性质活泼,易与 、R′X等发生反应生成RH、R-R′;
、R′X等发生反应生成RH、R-R′;
②各物质的沸点见下表:
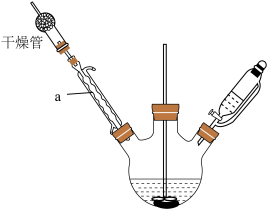
回答下列问题:
(1)仪器a的名称是___________ 。
(2)干燥管中无水氯化钙的作用是___________ 。
(3)微热或加入小颗粒碘单质可引发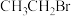 与镁屑的反应,其中碘的作用可能是
与镁屑的反应,其中碘的作用可能是___________ ;不宜使用长时间放置的镁屑进行实验,其原因是___________ 。
(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是___________ 。
(5)蒸去乙醚时采用热水浴的原因是___________ 。
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.69g,则2-甲基-2-丁醇的产率为___________ (结果保留2位有效数字)。

Ⅰ.乙基溴化镁的制备
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产率。
已知:①RMgBr化学性质活泼,易与
 、R′X等发生反应生成RH、R-R′;
、R′X等发生反应生成RH、R-R′;②各物质的沸点见下表:
| 物质 | 无水乙醚 | 溴乙烷 | 丙酮 | 2-甲基-2-丁醇 |
| 沸点(℃) | 34.6 | 38.4 | 56.5 | 102.5 |

回答下列问题:
(1)仪器a的名称是
(2)干燥管中无水氯化钙的作用是
(3)微热或加入小颗粒碘单质可引发
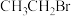 与镁屑的反应,其中碘的作用可能是
与镁屑的反应,其中碘的作用可能是(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是
(5)蒸去乙醚时采用热水浴的原因是
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.69g,则2-甲基-2-丁醇的产率为
您最近一年使用:0次
2023-05-18更新
|
270次组卷
|
2卷引用:湖北省武汉市武昌区2022-2023学年高三下学期5月质量检测化学试卷
名校
解题方法
4 . 实验室用以下装置(夹持和水浴加热装置略)制备环己酮缩乙二醇。
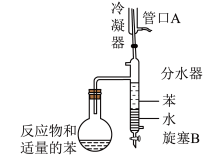

| A.以共沸体系带出水促使反应正向进行 |
| B.当观察到分水器中苯层液面高于支管口时,必须打开旋塞B将水放出 |
| C.管口A是冷凝水的进水口 |
| D.根据带出水的体积可估算反应进度 |
您最近一年使用:0次
2023-12-20更新
|
2109次组卷
|
8卷引用:辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题
辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题(已下线)化学01(14+4模式)2024年1月“九省联考”考前化学猜想卷(已下线)热点19 化学微型实验福建省泉州市永春一中、培元中学、石光中学、季延中学2023-2024学年高三下学期第二次联合考试化学试题河南省漯河市高级中学2023-2024学年高三下学期3月月考化学试题(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)(已下线)专题02 元素化合物 有机化合物-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)2024届湖南省长沙市第一中高三下学期高考适应性演练(一)化学试题
名校
解题方法
5 . 三苯甲醇是一种重要的有机合成中间体,可以通过下列原理进行合成:
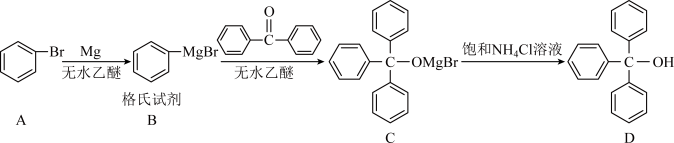
已知:①格氏试剂(RMgBr)性质活泼,可与水、卤代烃、醛、酮等物质反应。
②ROMgBr可发生水解。
③几种物质的物理性质如表所示(表中括号内的数据表示该有机物与水形成的具有固定组成的混合物的共沸点):
实验步骤如下:
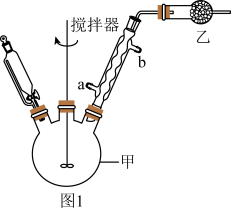
制备三苯甲醇:在图1所示的仪器甲中加入1.5 g镁屑,恒压滴液漏斗中加入25.0 mL无水乙醚和7.0 mL溴苯(约0.065 mol)的混合液,启动搅拌器,先将部分混合液加入甲中,开始反应,再逐滴加入余下的混合液,充分反应后,将甲置于冰水浴中,滴加11.0 g二苯酮(约0.060 mol)和25.0 mL无水乙醚的混合液,水浴回流60 min,慢慢滴加30.0 mL饱和 溶液。
溶液。
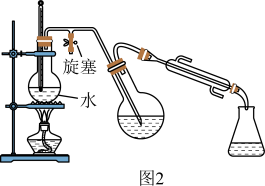
提纯三苯甲醇:用图2所示的水蒸气蒸馏装置分离出乙醚、溴苯并回收利用,向残留液中加入石油醚,获取粗产品。
请回答下列问题:
(1)除去镁条表面氧化膜并将其剪成屑状的目的是___________ 。
(2)仪器甲的名称为___________ ,球形冷凝管的进水口为___________ (填“a”或“b”),装置乙的作用为___________ 。
(3)反应原理中C→D使用饱和 溶液的作用是
溶液的作用是___________ 。
(4)水蒸气蒸馏能除去溴苯的原因是___________ ,加入石油醚后分离出粗产品的操作为___________ 。
(5)若粗产品经___________ (填提纯方法)得到8.8 g三苯甲醇,则三苯甲醇的产率为___________ (保留三位有效数字)。

已知:①格氏试剂(RMgBr)性质活泼,可与水、卤代烃、醛、酮等物质反应。
②ROMgBr可发生水解。
③几种物质的物理性质如表所示(表中括号内的数据表示该有机物与水形成的具有固定组成的混合物的共沸点):
| 物质 | 相对分子质量 | 沸点/℃ | 存在状态及溶解性 |
| 乙醚 | 74 | 34.6 | 微溶于水 |
| 溴苯 | 157 | 156.2(92.8) | 不溶于水的液体,溶于乙醚、乙醇 |
| 二苯酮 | 182 | 305.4 | 不溶于水的晶体,溶于乙醚 |
| 三苯甲醇 | 260 | 380.0 | 不溶于水及石油醚的白色晶体,溶于乙醇、乙醚 |
制备三苯甲醇:在图1所示的仪器甲中加入1.5 g镁屑,恒压滴液漏斗中加入25.0 mL无水乙醚和7.0 mL溴苯(约0.065 mol)的混合液,启动搅拌器,先将部分混合液加入甲中,开始反应,再逐滴加入余下的混合液,充分反应后,将甲置于冰水浴中,滴加11.0 g二苯酮(约0.060 mol)和25.0 mL无水乙醚的混合液,水浴回流60 min,慢慢滴加30.0 mL饱和
 溶液。
溶液。
提纯三苯甲醇:用图2所示的水蒸气蒸馏装置分离出乙醚、溴苯并回收利用,向残留液中加入石油醚,获取粗产品。

请回答下列问题:
(1)除去镁条表面氧化膜并将其剪成屑状的目的是
(2)仪器甲的名称为
(3)反应原理中C→D使用饱和
 溶液的作用是
溶液的作用是(4)水蒸气蒸馏能除去溴苯的原因是
(5)若粗产品经
您最近一年使用:0次
2023-04-28更新
|
425次组卷
|
2卷引用:云南省楚雄州2022-2023学年高二下学期期中学业质量监测化学试题



