解题方法
1 . Cu元素在生命活动中占有举足轻重的地位,缺铜会造成贫血、记忆力减退、反应迟钝、运动失常等。设计如下实验制备有机补铜剂顺式甘氨酸合铜水合物并测定其组成。
查阅资料:
①制备反应为:
②该反应同时生成顺式产物(天蓝色针状)和反式产物(蓝紫色鳞片状),其反应进程如图所示:

制备有机补铜剂顺式甘氨酸合铜水合物实验过程为:
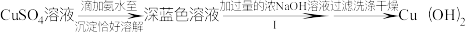

回答下列问题:
(1)步骤Ⅱ中控制反应温度为70℃的原因是_______ ,可采用的加热方式为_______ 。
(2)下列有关说法正确的是_______。
(3)用间接碘量法测定产物中Cu(Ⅱ)的质量分数。
已知: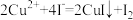
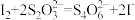
请选择以下正确的操作排序:
取2.0g所制备的产品,用稀硫酸溶解配成100L溶液→a→________ ,重复操作3次,消耗Na2S2O3标准液平均值为amL。
a.取25mL该溶液转移入锥形瓶
b.立即用酸式滴定管中0.01 molL-1Na2S2O3标准液快速进行滴定
c.立即用碱式滴定管中0.01 mol L-1Na2S2O3标准液快速进行滴定
d.当溶液变为浅黄色时,加入1mL淀粉溶液
e.加入蒸馏水和过量的KI溶液,得到棕黄色溶液
f.继续滴定至溶液蓝色恰好褪去
g.继续滴定至溶液由无色变为蓝色
根据实验数据,所得晶体中Cu(Ⅱ)质量分数为_______ ,若要提高产品的纯度,所用的实验方法名称是_______ 。
查阅资料:
①制备反应为:

②该反应同时生成顺式产物(天蓝色针状)和反式产物(蓝紫色鳞片状),其反应进程如图所示:

制备有机补铜剂顺式甘氨酸合铜水合物实验过程为:
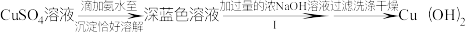

回答下列问题:
(1)步骤Ⅱ中控制反应温度为70℃的原因是
(2)下列有关说法正确的是_______。
| A.CuSO4和NaOH快速生成的Cu(OH)2絮状沉淀易裹挟杂质,故不采用CuSO4和NaOH直接反应制备Cu(OH)2 |
| B.步骤Ⅲ中趁热过滤是为了防止杂质析出 |
| C.步骤IV加入95%的乙醇可以得到纯度更高的产品,说明顺式甘氨酸的极性大于反式甘氨酸 |
| D.步骤V用25%酒精和丙酮分别洗涤晶体的目的是:25%酒精用于除去可溶性杂质(剩余反应物),丙酮用于除去晶体中残余的水 |
(3)用间接碘量法测定产物中Cu(Ⅱ)的质量分数。
已知:
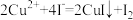
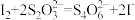
请选择以下正确的操作排序:
取2.0g所制备的产品,用稀硫酸溶解配成100L溶液→a→
a.取25mL该溶液转移入锥形瓶
b.立即用酸式滴定管中0.01 molL-1Na2S2O3标准液快速进行滴定
c.立即用碱式滴定管中0.01 mol L-1Na2S2O3标准液快速进行滴定
d.当溶液变为浅黄色时,加入1mL淀粉溶液
e.加入蒸馏水和过量的KI溶液,得到棕黄色溶液
f.继续滴定至溶液蓝色恰好褪去
g.继续滴定至溶液由无色变为蓝色
根据实验数据,所得晶体中Cu(Ⅱ)质量分数为
您最近一年使用:0次
解题方法
2 . 部分含氮物质的分类与相应化合物关系如图所示。下列说法错误的是

| A.b具有碱性和还原性 |
| B.反应Ⅰ中氧化产物和还原产物的物质的量之比为1∶1 |
C.反应Ⅱ过程中生成0.1mol  时,转移1mol电子 时,转移1mol电子 |
| D.反应Ⅲ能有效降低水体中的氮元素含量 |
您最近一年使用:0次
20-21高一下·浙江·阶段练习
3 . I.用水煤气制天然气的反应过程涉及如下反应:CO(g)+3H2(g)⇌CH4(g)+H2O(g)。现在300°C、容积为2 L的密闭容器中进行有关合成天然气的实验,相关数据记录如下:
根据表中信息回答下列问题:
(1)前30 min内该反应的平均反应速率v(H2)____________ 。
(2)反应达到平衡后,点燃混合气体,充分燃烧后消耗氧气的物质的量为__________ mol。
II.某有机物由碳、氢、氧、氮4种元素组成,其中含碳32%,氢6.7%,氮18.7% (均为质量分数)。该有机物的相对分子质量为75。
(3)通过计算写出该有机物的分子式___________ 。
(4)该有机物是蛋白质水解的产物,它与乙醇反应生成的酯可用于合成医药和农药,请写出生成该酯的化学方程式_______________ 。
| 时间 | CO/mol | H2/mol | CH4/mol | H2O/mol |
| 0 min | 4 | 40 | 0 | 0 |
| 30 min | 2 |
根据表中信息回答下列问题:
(1)前30 min内该反应的平均反应速率v(H2)
(2)反应达到平衡后,点燃混合气体,充分燃烧后消耗氧气的物质的量为
II.某有机物由碳、氢、氧、氮4种元素组成,其中含碳32%,氢6.7%,氮18.7% (均为质量分数)。该有机物的相对分子质量为75。
(3)通过计算写出该有机物的分子式
(4)该有机物是蛋白质水解的产物,它与乙醇反应生成的酯可用于合成医药和农药,请写出生成该酯的化学方程式
您最近一年使用:0次
名校
解题方法
4 . 化合物M是一种新型有机酰胺,在工业生产中有重要的作用,其合成路线如下:
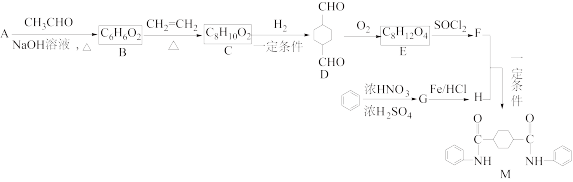
已知:①A是烃的含氧衍生物,相对分子质量为58,碳和氢的质量分数之和为44.8%,核磁共振氢谱显示为一组峰,可发生银镜反应,且5.8 g A完全发生反应生成0.4 mol银。
②R1-CHO+R2-CH2CHO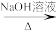
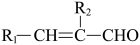
③R-COOH R-COCl
R-COCl
④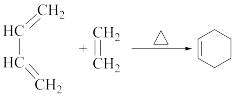
回答下列问题:
(1)A的名称______ E的结构简式为____________ ;G的名称为__________ 。
(2)B中含有官能团的名称为_______________________ 。
(3)C→D、D→E的反应类型分别为_____________ 、_______________ 。
(4)写出 F+H→M的化学反应方程式_________________ 。
(5)芳香族化合物W有三个取代基,是C的同分异构体,能与FeCl3溶液发生显色反应。0.5 mol W可与足量的Na反应生成1 g H2,且核磁共振氢谱显示为五组峰,符合以上条件的W的同分异构体共有_______ 种,写出其中一种的结构简式____________ 。
(6)参照上述合成路线,以C2H4和HOCH2CH2OH为原料(无机试剂任选),设计制备 的合成路线
的合成路线_____________ 。

已知:①A是烃的含氧衍生物,相对分子质量为58,碳和氢的质量分数之和为44.8%,核磁共振氢谱显示为一组峰,可发生银镜反应,且5.8 g A完全发生反应生成0.4 mol银。
②R1-CHO+R2-CH2CHO
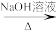
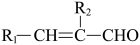
③R-COOH
 R-COCl
R-COCl④
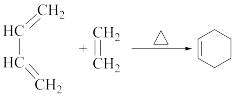
回答下列问题:
(1)A的名称
(2)B中含有官能团的名称为
(3)C→D、D→E的反应类型分别为
(4)写出 F+H→M的化学反应方程式
(5)芳香族化合物W有三个取代基,是C的同分异构体,能与FeCl3溶液发生显色反应。0.5 mol W可与足量的Na反应生成1 g H2,且核磁共振氢谱显示为五组峰,符合以上条件的W的同分异构体共有
(6)参照上述合成路线,以C2H4和HOCH2CH2OH为原料(无机试剂任选),设计制备
 的合成路线
的合成路线
您最近一年使用:0次
5 . 氨基酸分子(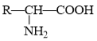 )中,既有碱性的氨基(—NH2),又有酸性的羧基(—COOH)。在一定的酸碱性条件下,能自身成盐(
)中,既有碱性的氨基(—NH2),又有酸性的羧基(—COOH)。在一定的酸碱性条件下,能自身成盐(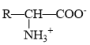 )。所以在氨基酸分析中不能用碱溶液测定氨基酸水溶液中羧基的数目,而应先加入甲醛,使它与—NH2缩合(R-NH2+
)。所以在氨基酸分析中不能用碱溶液测定氨基酸水溶液中羧基的数目,而应先加入甲醛,使它与—NH2缩合(R-NH2+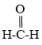 →R-N=CH2+H2O),然后再用碱液滴定法,测定羧基含量。氨基酸中—NH2的数目可用与HNO2反应定量放出N2而测得,氨基在反应中变成-OH(R—NH2+HNO2→R—OH+N2+H2O)。
→R-N=CH2+H2O),然后再用碱液滴定法,测定羧基含量。氨基酸中—NH2的数目可用与HNO2反应定量放出N2而测得,氨基在反应中变成-OH(R—NH2+HNO2→R—OH+N2+H2O)。
化合物A分子式为C8H15O4N3。中和lmolA与甲醛作用后的产物消耗1molNaOH。1molA与HNO2反应放出lmolN2,并生成B(C8H14O5N2)。B经水解后得羟基乙酸和丙氨酸。
(1)A的结构简式为_______
(2)B的结构简式为_______
(3)A跟亚硝酸反应的化学方程式为:_______
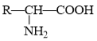 )中,既有碱性的氨基(—NH2),又有酸性的羧基(—COOH)。在一定的酸碱性条件下,能自身成盐(
)中,既有碱性的氨基(—NH2),又有酸性的羧基(—COOH)。在一定的酸碱性条件下,能自身成盐(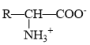 )。所以在氨基酸分析中不能用碱溶液测定氨基酸水溶液中羧基的数目,而应先加入甲醛,使它与—NH2缩合(R-NH2+
)。所以在氨基酸分析中不能用碱溶液测定氨基酸水溶液中羧基的数目,而应先加入甲醛,使它与—NH2缩合(R-NH2+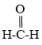 →R-N=CH2+H2O),然后再用碱液滴定法,测定羧基含量。氨基酸中—NH2的数目可用与HNO2反应定量放出N2而测得,氨基在反应中变成-OH(R—NH2+HNO2→R—OH+N2+H2O)。
→R-N=CH2+H2O),然后再用碱液滴定法,测定羧基含量。氨基酸中—NH2的数目可用与HNO2反应定量放出N2而测得,氨基在反应中变成-OH(R—NH2+HNO2→R—OH+N2+H2O)。化合物A分子式为C8H15O4N3。中和lmolA与甲醛作用后的产物消耗1molNaOH。1molA与HNO2反应放出lmolN2,并生成B(C8H14O5N2)。B经水解后得羟基乙酸和丙氨酸。
(1)A的结构简式为
(2)B的结构简式为
(3)A跟亚硝酸反应的化学方程式为:
您最近一年使用:0次
6 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是一种用于治疗缺铁性贫血的药物,用下图装置可以在实验室中制备甘氨酸亚铁:

有关物质性质如下表所示:
实验步骤如下:
Ⅰ.打开K1、K3,向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合液中加入无水乙醇,析出沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称是___________ ,d的作用是___________ 。
(2)步骤Ⅰ中将b中溶液加入到c中的操作是关闭___________ 打开___________ (填“K2”或“K3”);步骤Ⅱ中若调节溶液pH偏高,则所得粗产品中会混有杂质___________ (写化学式)。
(3)c中生成甘氨酸亚铁的化学方程式是___________ 。
(4)下列关于该实验的说法正确的是___________ (填字母)。
a.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
b.步骤Ⅰ中可由d中导管是否还有气泡冒出来判断装置中的空气是否排尽
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
(5)①工业上常用高氯酸(不与冰醋酸反应)标准溶液在非水体系中滴定甘氨酸的方法测定产品中的甘氨酸的含量。请设计实验,将所得粗产品中的甘氨酸分离出来直接用于滴定:_______ 。
②滴定过程中下列操作会使甘氨酸的测定结果偏高的是_______ (填字母)。
a.滴定时未用高氯酸标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后消失

有关物质性质如下表所示:
| 甘氨酸(H2NCH2COOH) | 易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中溶解度大于在乙醇中的溶解度。 |
| 柠檬酸 | 易溶于水和乙醇,酸性较强,有强还原性。 |
| 甘氨酸亚铁 | 易溶于水且在水中难电离,难溶于乙醇、冰醋酸。 |
Ⅰ.打开K1、K3,向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合液中加入无水乙醇,析出沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称是
(2)步骤Ⅰ中将b中溶液加入到c中的操作是关闭
(3)c中生成甘氨酸亚铁的化学方程式是
(4)下列关于该实验的说法正确的是
a.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
b.步骤Ⅰ中可由d中导管是否还有气泡冒出来判断装置中的空气是否排尽
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
(5)①工业上常用高氯酸(不与冰醋酸反应)标准溶液在非水体系中滴定甘氨酸的方法测定产品中的甘氨酸的含量。请设计实验,将所得粗产品中的甘氨酸分离出来直接用于滴定:
②滴定过程中下列操作会使甘氨酸的测定结果偏高的是
a.滴定时未用高氯酸标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后消失
您最近一年使用:0次
7 . 某种含氮有机物的水溶液,既能与酸反应,有能与碱反应。该有机物分子中碳原子数等于氧原子数,碳、氧、氮的原子数之和等于氢原子数。每个有机物分子中只含1个氮原子。实验测得该有机物的含氮质量分数为18.6%。试推测该有机物的结构简式________ ,并写出一种与它互为类别异构的有机物的结构简式 _______ 和 名称___________ 。
您最近一年使用:0次



