名校
解题方法
1 . 常用的补铁剂甘氨酸亚铁[(NH2CH2COO)2Fe],是一种易溶于水的粉末,性稳定,久储不变。实验室利用以下实验装置(部分夹持和加热仪器省略),以11.6g新制碳酸亚铁(FeCO3)为铁源与足量甘氨酸(NH2CH2COOH)反应制备甘氨酸亚铁。

实验步骤如下:
①组装仪器,检验装置气密性良好,添加试剂。
②打开a的活塞,向A中加入适量盐酸。待装置C中空气排净后,向装置C中滴入适量柠檬酸,关闭活塞并加热,待反应结束后,取出C中的反应液,过滤。
③滤液经蒸发浓缩,加入无水乙醇,过滤,干燥得到产品。
已知:相关物质的性质如下表
回答下列问题:
(1)预先制备CO2的目的:_______ 。
(2)仪器b的名称是_______ ,装置B的作用_______ 。
(3)装置C中滴加柠檬酸可调节溶液pH,体系pH与产率的关系如下表
pH过高和过低均会使产率下降的原因是甘氨酸有_______ 性质。
(4)装置D功能表现的现象和结论_______ 。
(5)步骤③中加入无水乙醇的目的是_______ 。
(6)经测定本实验实际制得甘氨酸亚铁的质量为15.3g,则此实验的产率是_______ 。

实验步骤如下:
①组装仪器,检验装置气密性良好,添加试剂。
②打开a的活塞,向A中加入适量盐酸。待装置C中空气排净后,向装置C中滴入适量柠檬酸,关闭活塞并加热,待反应结束后,取出C中的反应液,过滤。
③滤液经蒸发浓缩,加入无水乙醇,过滤,干燥得到产品。
已知:相关物质的性质如下表
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有还原性和较强的酸性 | 易溶于水,难溶于乙醇 |
(1)预先制备CO2的目的:
(2)仪器b的名称是
(3)装置C中滴加柠檬酸可调节溶液pH,体系pH与产率的关系如下表
| 体系pH | 4.0 | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 |
| 产率/% | 65.74 | 74.96 | 78.78 | 83.13 | 85.57 | 72.98 | 62.31 |
(4)装置D功能表现的现象和结论
(5)步骤③中加入无水乙醇的目的是
(6)经测定本实验实际制得甘氨酸亚铁的质量为15.3g,则此实验的产率是
您最近一年使用:0次
名校
解题方法
2 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是新一代畜禽饲料补铁添加剂。某实验小组以碳酸亚铁和甘氨酸反应制备甘氨酸亚铁的装置如下(夹持和加热仪器略去):
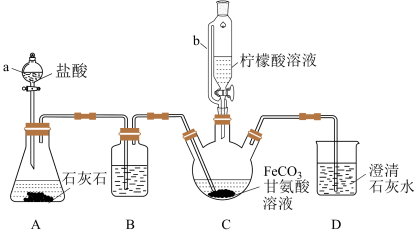
已知:①反应原理为2H2NCH2COOH+FeCO3 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。
②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为_______ 。
(2)装置A制备CO2的用途是_______ 。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为_______ 。
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是_______ 。
②柠檬酸溶液除了起酸性作用外,还有的作用是_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是_______ %。

已知:①反应原理为2H2NCH2COOH+FeCO3
 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为
(2)装置A制备CO2的用途是
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是
②柠檬酸溶液除了起酸性作用外,还有的作用是
(5)过程II中加入无水乙醇的目的是
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是
您最近一年使用:0次
3 . 甘氨酸亚铁是营养性饲料添加剂。实验室利用FeCO3与甘氨酸(H2NCH2COOH)制备甘氨酸亚铁[(H2NCH2COO)2Fe],实验装置如图所示(夹持和加热仪器已省略)
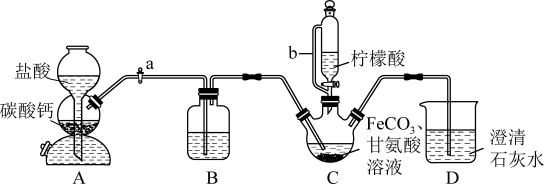
查阅资料:①甘氨酸易溶于水,微溶于乙醇。
②甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性。
实验过程:
I装置C中盛有17.4gFeCO3和200mL1.0mol·L-1甘氨酸溶液。实验时,先打开活塞a,待装置C中空气排尽后,再向三颈烧瓶中滴加柠檬酸溶液,加热。
II.经过一系列操作得到产品。
(1)A仪器是启普发生器,该仪器的特点是“随开随用、随关随停”,下列实验中可利用该仪器制备气体的是___________ (填序号)。
①二氧化锰与浓盐酸反应制备氯气
②锌粒与稀盐酸反应制备氢气
③亚硫酸钠固体与浓硫酸反应制备二氧化硫
④硫化亚铁固体与稀盐酸反应制备硫化氢
(2)过程1中,先打开活塞a,待___________ 时说明装置c中空气排尽,再向三颈烧瓶中滴加柠檬酸溶液,加热。仪器b的名称___________ 。
(3)过程I中,加入柠檬酸可促进FeCO3溶解并调节溶液pH,体系pH与甘氨酸亚铁产率的关系如图。由图象可知pH过低或过高均会导致产率下降,写出pH过低时有关的离子方程式___________ , 柠檬酸除了可以促进FeCO3溶解并调节溶液pH外,还可以___________ 。
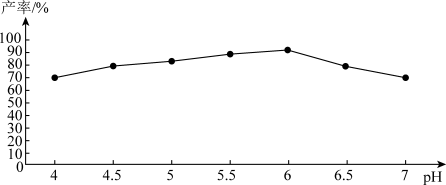
(4)完成过程II的实验操作:反应结束后过滤,将滤液进行蒸发浓缩加入___________ 、过滤、洗涤、干燥。
(5)已知浓度为0.1mol·L-1的甘氨酸亚铁溶液的导电能力远小于0.1mol·L-1的FeSO4溶液的导电能力,其原因可能是___________ 。
(6)最终得到的产品质量为16. 32g,该实验产率为___________ 。

查阅资料:①甘氨酸易溶于水,微溶于乙醇。
②甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性。
实验过程:
I装置C中盛有17.4gFeCO3和200mL1.0mol·L-1甘氨酸溶液。实验时,先打开活塞a,待装置C中空气排尽后,再向三颈烧瓶中滴加柠檬酸溶液,加热。
II.经过一系列操作得到产品。
(1)A仪器是启普发生器,该仪器的特点是“随开随用、随关随停”,下列实验中可利用该仪器制备气体的是
①二氧化锰与浓盐酸反应制备氯气
②锌粒与稀盐酸反应制备氢气
③亚硫酸钠固体与浓硫酸反应制备二氧化硫
④硫化亚铁固体与稀盐酸反应制备硫化氢
(2)过程1中,先打开活塞a,待
(3)过程I中,加入柠檬酸可促进FeCO3溶解并调节溶液pH,体系pH与甘氨酸亚铁产率的关系如图。由图象可知pH过低或过高均会导致产率下降,写出pH过低时有关的离子方程式

(4)完成过程II的实验操作:反应结束后过滤,将滤液进行蒸发浓缩加入
(5)已知浓度为0.1mol·L-1的甘氨酸亚铁溶液的导电能力远小于0.1mol·L-1的FeSO4溶液的导电能力,其原因可能是
(6)最终得到的产品质量为16. 32g,该实验产率为
您最近一年使用:0次
名校
解题方法
4 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如图所示(夹持和加热、搅拌仪器已省略)。
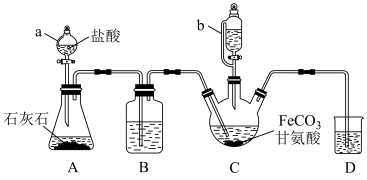
有关物质性质如下表:
实验过程:
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是_______ 。
(2)装置B中盛有的试剂是_______ ;实验过程中装置D的导管需要一直浸入液面下的必要性是_______ 。
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和_______ 。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)可以用_______ 试剂(写化学式)检验产品中是否含有Fe3+。
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是_______ 。

有关物质性质如下表:
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
| 两性化合物 | 强酸性、强还原性 |
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是
(2)装置B中盛有的试剂是
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为
(5)过程II中加入无水乙醇的目的是
(6)可以用
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是
您最近一年使用:0次
5 . 苯胺( )是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
)是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
已知:① 和
和 相似,与盐酸反应生成易溶于水的盐(
相似,与盐酸反应生成易溶于水的盐( );
);
②用硝基苯制取苯胺的反应原理:2 +3Sn+12HCl→2
+3Sn+12HCl→2 +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质如表:
Ⅰ.比较苯胺与氨气的性质
(1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为___________ ;用苯胺代替浓氨水重复上述实验,却观察不到白烟,原因是___________ 。
Ⅱ.制备苯胺。往图1所示装置(夹持装置略,下同)的冷凝管口分批加入20 mL浓盐酸(过量),置于热水浴中回流20 min,使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量50% NaOH溶液,至溶液呈碱性。

(2)冷凝管的出水口是___________ (填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反应的离子方程式为___________ 。
Ⅲ.提取苯胺
i.取出图1所示装置中的三颈烧瓶,改装为图2所示的装置。加热装置A产生水蒸气,烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液。
ii.往所得水溶液中加入氯化钠固体,使溶液达到饱和状态,再用乙醚萃取,得到乙醚萃取液。
ⅲ.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺2.79 g。

(4)图2中B装置的名称为___________ ;操作i中,为了分离混合物,取出烧瓶C前,应先打开止水夹d,再停止加热,理由是___________ 。
(5)该实验中苯胺的产率为___________ 。
(6)欲在不加热条件下除去苯胺中的少量硝基苯杂质,简述实验方案:___________ 。
 )是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
)是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。已知:①
 和
和 相似,与盐酸反应生成易溶于水的盐(
相似,与盐酸反应生成易溶于水的盐( );
);②用硝基苯制取苯胺的反应原理:2
 +3Sn+12HCl→2
+3Sn+12HCl→2 +3SnCl4+4H2O
+3SnCl4+4H2O③有关物质的部分物理性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/( ) ) |
| 苯胺 | -6.3 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
| 硝基苯 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | -116.2 | 34.6 | 微溶于水 | 0.7134 |
(1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为
Ⅱ.制备苯胺。往图1所示装置(夹持装置略,下同)的冷凝管口分批加入20 mL浓盐酸(过量),置于热水浴中回流20 min,使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量50% NaOH溶液,至溶液呈碱性。

(2)冷凝管的出水口是
(3)滴加NaOH溶液的主要目的是析出苯胺,反应的离子方程式为
Ⅲ.提取苯胺
i.取出图1所示装置中的三颈烧瓶,改装为图2所示的装置。加热装置A产生水蒸气,烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液。
ii.往所得水溶液中加入氯化钠固体,使溶液达到饱和状态,再用乙醚萃取,得到乙醚萃取液。
ⅲ.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺2.79 g。

(4)图2中B装置的名称为
(5)该实验中苯胺的产率为
(6)欲在不加热条件下除去苯胺中的少量硝基苯杂质,简述实验方案:
您最近一年使用:0次
2021-10-19更新
|
160次组卷
|
2卷引用:黑龙江省大庆市东风中学2021-2022学年高三上学期10月质量检测化学试题
6 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是一种用于治疗缺铁性贫血的药物,用下图装置可以在实验室中制备甘氨酸亚铁:

有关物质性质如下表所示:
实验步骤如下:
Ⅰ.打开K1、K3,向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合液中加入无水乙醇,析出沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称是___________ ,d的作用是___________ 。
(2)步骤Ⅰ中将b中溶液加入到c中的操作是关闭___________ 打开___________ (填“K2”或“K3”);步骤Ⅱ中若调节溶液pH偏高,则所得粗产品中会混有杂质___________ (写化学式)。
(3)c中生成甘氨酸亚铁的化学方程式是___________ 。
(4)下列关于该实验的说法正确的是___________ (填字母)。
a.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
b.步骤Ⅰ中可由d中导管是否还有气泡冒出来判断装置中的空气是否排尽
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
(5)①工业上常用高氯酸(不与冰醋酸反应)标准溶液在非水体系中滴定甘氨酸的方法测定产品中的甘氨酸的含量。请设计实验,将所得粗产品中的甘氨酸分离出来直接用于滴定:_______ 。
②滴定过程中下列操作会使甘氨酸的测定结果偏高的是_______ (填字母)。
a.滴定时未用高氯酸标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后消失

有关物质性质如下表所示:
| 甘氨酸(H2NCH2COOH) | 易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中溶解度大于在乙醇中的溶解度。 |
| 柠檬酸 | 易溶于水和乙醇,酸性较强,有强还原性。 |
| 甘氨酸亚铁 | 易溶于水且在水中难电离,难溶于乙醇、冰醋酸。 |
Ⅰ.打开K1、K3,向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合液中加入无水乙醇,析出沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称是
(2)步骤Ⅰ中将b中溶液加入到c中的操作是关闭
(3)c中生成甘氨酸亚铁的化学方程式是
(4)下列关于该实验的说法正确的是
a.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
b.步骤Ⅰ中可由d中导管是否还有气泡冒出来判断装置中的空气是否排尽
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
(5)①工业上常用高氯酸(不与冰醋酸反应)标准溶液在非水体系中滴定甘氨酸的方法测定产品中的甘氨酸的含量。请设计实验,将所得粗产品中的甘氨酸分离出来直接用于滴定:
②滴定过程中下列操作会使甘氨酸的测定结果偏高的是
a.滴定时未用高氯酸标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后消失
您最近一年使用:0次



