真题
解题方法
1 . C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____ 周期第_____ 族。
(2)N的基态原子核外电子排布式为_____ ;Cu的基态原子最外层有___ 个电子。
(3)用“>”或“<”填空:
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
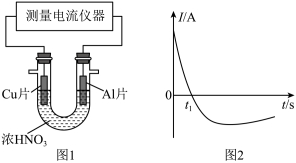
0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____ ,溶液中的H+向___ 极移动,t1时,原电池中电子流动方向发生改变,其原因是______ 。
(1)Si位于元素周期表第
(2)N的基态原子核外电子排布式为
(3)用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al | N | 金刚石 | CH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

0-t1时,原电池的负极是Al片,此时,正极的电极反应式是
您最近一年使用:0次
2016-12-09更新
|
1690次组卷
|
2卷引用:2015年全国普通高等学校招生统一考试化学(安徽卷)
真题
2 . Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
您最近一年使用:0次
2014-06-20更新
|
3035次组卷
|
6卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(安徽卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(安徽卷)(已下线)2015届安徽省黄山市徽州一中高三第一次月考化学试卷2016届四川省攀枝花十二中高三下学期第一次月考化学试卷(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)2021年天津高考化学试题变式题13-16



