1 . 氢元素及其化合物在自然界广泛存在且具有重要应用。 、
、 、
、 是氢元素的3种核素,基态H原子
是氢元素的3种核素,基态H原子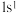 的核外电子排布,使得H既可以形成
的核外电子排布,使得H既可以形成 又可以形成
又可以形成 ,还能形成
,还能形成 、
、 、
、 、
、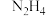 、
、 等重要化合物;水煤气法、电解水、光催化分解水都能获得
等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反应中,
,如水煤气法制氢反应中, 与足量
与足量 反应生成
反应生成 和
和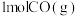 吸收131.3kJ的热量。
吸收131.3kJ的热量。 在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与
在催化剂作用下与 反应可得到
反应可得到 。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列物质结构与性质或物质性质与用途具有对应关系的是
。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列物质结构与性质或物质性质与用途具有对应关系的是
 、
、 、
、 是氢元素的3种核素,基态H原子
是氢元素的3种核素,基态H原子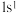 的核外电子排布,使得H既可以形成
的核外电子排布,使得H既可以形成 又可以形成
又可以形成 ,还能形成
,还能形成 、
、 、
、 、
、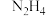 、
、 等重要化合物;水煤气法、电解水、光催化分解水都能获得
等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反应中,
,如水煤气法制氢反应中, 与足量
与足量 反应生成
反应生成 和
和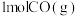 吸收131.3kJ的热量。
吸收131.3kJ的热量。 在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与
在催化剂作用下与 反应可得到
反应可得到 。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列物质结构与性质或物质性质与用途具有对应关系的是
。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列物质结构与性质或物质性质与用途具有对应关系的是A. 具有还原性,可作为氢氧燃料电池的燃料 具有还原性,可作为氢氧燃料电池的燃料 |
| B.氨极易溶于水,液氨可用作制冷剂 |
C. 分子之间形成氢键, 分子之间形成氢键, 的热稳定性比 的热稳定性比 的高 的高 |
D.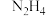 中的N原子与 中的N原子与 形成配位键, 形成配位键,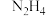 具有还原性 具有还原性 |
您最近一年使用:0次
2023-08-07更新
|
4319次组卷
|
4卷引用:2023年高考江苏卷化学真题
2 . 硫铁化合物( 、
、 等)应用广泛。
等)应用广泛。
(1)纳米 可去除水中微量六价铬
可去除水中微量六价铬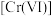 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。
已知: ,
,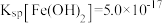 ;
; 电离常数分别为
电离常数分别为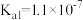 、
、 。
。
①在弱碱性溶液中, 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为_______ 。
②在弱酸性溶液中,反应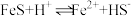 的平衡常数K的数值为
的平衡常数K的数值为_______ 。
③在 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是_______ 。
(2) 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为_______ ,在 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
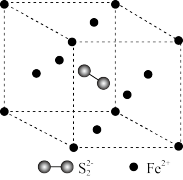
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来_______ 。
(3) 、
、 在空气中易被氧化,将
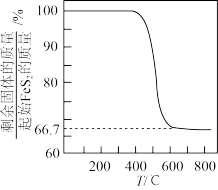
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为_______ (填化学式,写出计算过程)。
 、
、 等)应用广泛。
等)应用广泛。(1)纳米
 可去除水中微量六价铬
可去除水中微量六价铬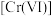 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。已知:
 ,
,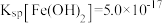 ;
; 电离常数分别为
电离常数分别为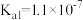 、
、 。
。①在弱碱性溶液中,
 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为②在弱酸性溶液中,反应
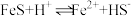 的平衡常数K的数值为
的平衡常数K的数值为③在
 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是(2)
 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来
(3)
 、
、 在空气中易被氧化,将
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为
您最近一年使用:0次
2022-07-21更新
|
8808次组卷
|
13卷引用:江苏省2022年普通高中学业水平选择性考试
江苏省2022年普通高中学业水平选择性考试(已下线)2022年江苏卷高考真题变式题14-17江苏省南京市金陵中学河西分校2022-2023学年高二上学期期末检测化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(结构与性质)(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十四 结构性质中的新材料(已下线)专题三 离子反应-实战高考·二轮复习核心突破北京市第二中学2022-2023学年高三下学期2月开学测试化学试题(已下线)2022年北京高考真题化学试题变式题(结构与性质)(已下线)专题20 结构与性质(已下线)专题20 结构与性质北京市第二中学2023-2024学年高三下学期开学考化学试卷
真题
3 . 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
(1) 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______ ;1mol 中含有的
中含有的 键数目为
键数目为___________ 。
(2)将乙炔通入 溶液生成
溶液生成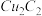 红棕色沉淀。
红棕色沉淀。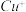 基态核外电子排布式为
基态核外电子排布式为_________________________ 。
(3)乙炔与氢氰酸反应可得丙烯腈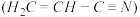 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是________________ ;分子中处于同一直线上的原子数目最多为__________________ 。
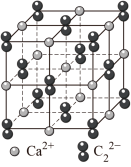
(4) 晶体的晶胞结构与
晶体的晶胞结构与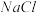 晶体相似(如图所示),但
晶体相似(如图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个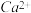 周围距离最近的
周围距离最近的 数目为
数目为______________ 。
B.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(l)上述实验中过滤的目的是_________________ 。
(2) 滤液在分液漏斗中洗涤静置后,有机层处于_______ 层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有_____________ 。
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为______________ 。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是____________________ 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有_________ 、_________ 。
A.乙炔是有机合成工业的一种原料。工业上曾用
 与水反应生成乙炔。
与水反应生成乙炔。(1)
 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的
中含有的 键数目为
键数目为(2)将乙炔通入
 溶液生成
溶液生成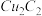 红棕色沉淀。
红棕色沉淀。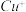 基态核外电子排布式为
基态核外电子排布式为(3)乙炔与氢氰酸反应可得丙烯腈
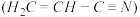 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是(4)
 晶体的晶胞结构与
晶体的晶胞结构与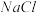 晶体相似(如图所示),但
晶体相似(如图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个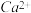 周围距离最近的
周围距离最近的 数目为
数目为
B.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在
 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。(l)上述实验中过滤的目的是
(2) 滤液在分液漏斗中洗涤静置后,有机层处于
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 | 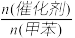 | 硝化产物中各种异构体质量分数(%) | 总产率(%) | ||
| 对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | |||
| 浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 98.0 |
| 1.2 | 36.5 | 59.5 | 4.0 | 99.8 | |
| NaHSO4 | 0.15 | 44.6 | 55.1 | 0.3 | 98.9 |
| 0.25 | 46.3 | 52.8 | 0.9 | 99.9 | |
| 0.32 | 47.9 | 51.8 | 0.3 | 99.9 | |
| 0.36 | 45.2 | 54.2 | 0.6 | 99.9 | |
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有
您最近一年使用:0次
2019-01-30更新
|
1045次组卷
|
3卷引用:2010年普通高等学校招生统一考试理综试题化学部分(江苏卷)
4 . 臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为 和
和 ,NOx也可在其他条件下被还原为N2。
,NOx也可在其他条件下被还原为N2。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ; 的空间构型为
的空间构型为_____________ (用文字描述)。
(2)Fe2+基态核外电子排布式为__________________ 。
(3)与O3分子互为等电子体的一种阴离子为_____________ (填化学式)。
(4)N2分子中σ键与π键的数目比n(σ)∶n(π)=__________________ 。
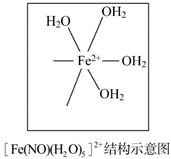
(5)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体。_____________
 和
和 ,NOx也可在其他条件下被还原为N2。
,NOx也可在其他条件下被还原为N2。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为(2)Fe2+基态核外电子排布式为
(3)与O3分子互为等电子体的一种阴离子为
(4)N2分子中σ键与π键的数目比n(σ)∶n(π)=
(5)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体。

您最近一年使用:0次
2018-06-10更新
|
4534次组卷
|
7卷引用:2018年全国普通高等学校招生统一考试化学(江苏卷)
2018年全国普通高等学校招生统一考试化学(江苏卷)江苏师范大学附属实验学校2019届高三上学期10月学情调研化学试题【全国百强校】江苏省启东中学2018-2019学年高二(创新班)下学期期中考试化学试题(已下线)2018年高考题及模拟题汇编 专题18 物质结构与性质(选修)(已下线)《2019年高考总复习巅峰冲刺》专题12 物质结构与性质应试策略(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)第31讲 分子结构与性质(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
5 . A.原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种数最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为_______ ,1mol Y2X2含有σ键的数目为_______ 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是_______ 。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是_______ 。
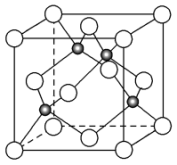
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是_______ ,它可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,反应的化学方程式为_______ 。
B.草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)
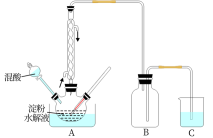
实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3 →3H2C2O4+9NO2↑ +3NO↑ +9H2O
C6H12O6+8HNO3 →6CO2+8NO↑ +10H2O
3H2C2O4+2HNO3 →6CO2+2NO↑ +4H2O
(1)检验淀粉是否水解完全所需用的试剂为_______
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是_______
(3)装置C用于尾气吸收,当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NO,全部吸收,原因是_______ (用化学方程式表示)
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是_______ 。
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有_______ 。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是

B.草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)

实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3 →3H2C2O4+9NO2↑ +3NO↑ +9H2O
C6H12O6+8HNO3 →6CO2+8NO↑ +10H2O
3H2C2O4+2HNO3 →6CO2+2NO↑ +4H2O
(1)检验淀粉是否水解完全所需用的试剂为
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是
(3)装置C用于尾气吸收,当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NO,全部吸收,原因是
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有
您最近一年使用:0次
真题
解题方法
6 . A.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_________________ 。
(2)B的氢化物的分子空间构型是____________ 。其中心原子采取_________ 杂化。
(3)写出化合物AC2的电子式____________ ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为_____________ 。
(4)E的核外电子排布式是_____________ ,ECl3形成的配合物的化学式为_______ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是________________________________________________ 。
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4①
R-OH+HBr R-Br+H2O ②
R-Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是_______ 。(填字母)
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性_______ (填“大于”、“等于”或“小于”);其原因是_______________________________________________________________________ 。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________ (填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必需进行稀释,起目的是___________ 。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是___________ 。(填字母)
a.NaI b.NaOH c.NaHSO3d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于_____________ ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是___________________________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
(4)E的核外电子排布式是
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4①
R-OH+HBr
 R-Br+H2O ②
R-Br+H2O ②可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在
(4)制备操作中,加入的浓硫酸必需进行稀释,起目的是
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是
a.NaI b.NaOH c.NaHSO3d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于
您最近一年使用:0次



