1 . 化合物X由3种短周期元素组成,某兴趣小组按如下流程进行实验。溶液D焰色反应为紫红色,气体B能使湿润的红色石蕊试纸变蓝。

请回答:
(1)组成X的3种元素是_______ (填元素符号),其中非金属元素形成的所有 单核离子半径由大到小的顺序为_______ 。
(2)将足量气体B通入硫酸铜溶液,得到深蓝色溶液,写出该反应的离子方程式_______ ,溶液E中溶质的成分为_______ (用化学式表示)。
(3)写出A→D的化学方程式是_______ 。
(4)在X的3种元素中,由相对分子质量最小的元素组成的单质与一定量的金属钠反应,请设计实验方案,验证反应结束后固体的成分_______ 。

请回答:
(1)组成X的3种元素是
(2)将足量气体B通入硫酸铜溶液,得到深蓝色溶液,写出该反应的离子方程式
(3)写出A→D的化学方程式是
(4)在X的3种元素中,由相对分子质量最小的元素组成的单质与一定量的金属钠反应,请设计实验方案,验证反应结束后固体的成分
您最近一年使用:0次
2022-04-14更新
|
1215次组卷
|
3卷引用:浙江省台州市2022届高三下学期4月教学质量评估(二模)化学试题
解题方法
2 . 下图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题

(1)表中某元素最高正价氧化物的水化物与其氢化物之间能相互反应生成离子化合物,则该离子化合物的名称是______ ,由元素④、⑥、⑦、⑧形成的简单离子的半径由大到小的顺序是_______ (用离子符号表示,下同)。②、④、⑤元素的氢化物的沸点由高到低的顺序是____________ 。
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该离子反应方程是________________ 。
(3)由表中四种元素形成X、Y、Z、M、N等常见物质,X、Y含有一种相同元素,其中X焰色反应呈黄色,可发生以下反应:

①X、Y与水混合后反应的离子方程式为________________ 。
②N→⑦的单质反应的化学方程式为_________________ 。
③若将Y溶液加热蒸干、灼烧后得到的物质的化学式是________________ 。

(1)表中某元素最高正价氧化物的水化物与其氢化物之间能相互反应生成离子化合物,则该离子化合物的名称是
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该离子反应方程是
(3)由表中四种元素形成X、Y、Z、M、N等常见物质,X、Y含有一种相同元素,其中X焰色反应呈黄色,可发生以下反应:

①X、Y与水混合后反应的离子方程式为
②N→⑦的单质反应的化学方程式为
③若将Y溶液加热蒸干、灼烧后得到的物质的化学式是
您最近一年使用:0次
2019-01-30更新
|
527次组卷
|
2卷引用:2016届重庆市南开中学高三7月月考化学试卷1
3 . X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)_______________________ 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)____________________ 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:
B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:________ ;D的电子式:________ 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为________________ ;由A转化为B的离子方程式为______________________ 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:_________________________________ 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是_________________ ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有___________ 。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
 B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:
B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:
您最近一年使用:0次
2019-01-30更新
|
2078次组卷
|
6卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)
2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)(已下线)2014高考化学二轮专题突破 专题六物质结构和元素周期律练习卷(已下线)2014届高考化学二轮复习必做训练 物质结构、元素周期律练习卷2016届陕西省西安市第七十中学高三上学期10月月考化学试卷四川省广安市第二中学2019届高三上学期第一次月考化学试题百所名校联考-物质结构 元素周期律
解题方法
4 . X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。据此回答下列问题:
(1)L的常见原子组成符号为___________ ;M在元素周期表中的位置为_________________ ;五种元素的原子半径从大到小的顺序是_________________ (用具体元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为__________ ,B的结构式为__________________ 。Z和L也能组成原子数目比2∶4的分子C, 已知1 mol 液态C和液态B燃烧时生成无毒无害物质,并释放524.5 kJ的热量,试写出该反应的热化学方程式为________________ 。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为___________ ,其最高价氧化物对应的水化物化学式为___________ 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是________ (填字母代号)。
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R。写出阳极生成R的电极反应式:______________________ 。
(1)L的常见原子组成符号为
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
| A.+99.7 kJ·mol-1 | B.+29.7 kJ·mol-1 | C.-20.6 kJ·mol-1 | D.-241.8 kJ·mol-1 |
您最近一年使用:0次
5 . 有八种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。z、e、g、h的最高价氧化物对应水化物溶液(浓度均为0.01 mol·L-1)的pH与原子序数的关系如图2所示。
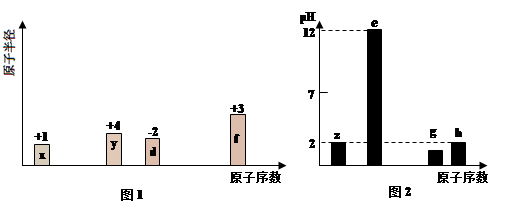
根据上述信息进行判断,并回答下列问题:
(1)h在元素周期表中的位置是____________________ 。
(2)比较f、g、h常见离子的半径大小_______ >_______ >_______ (用离子符号表示);e、f的最高价氧化物对应水化物碱性较强的是______________ (用化学式表示)。
(3)下列可作为比较f和Mg金属性强弱的依据是________ 。
a.测两种元素单质的硬度和熔、沸点
b.测等浓度相应氯化物水溶液的pH
c.比较单质与同浓度盐酸反应的剧烈程度
d.比较两种元素在化合物中化合价的高低
(4)上述元素任选三种组成六原子共价化合物,写出其化学式_______ (写一个即可)。
(5)据报道,最近意大利科学家获得了极具研究价值的z4,其分子结构与白磷分子的正四面体结构相似。已知断裂1 mol z-z键吸收167 kJ热量,生成1 mol Z≡Z键放出942 kJ热量,请写出z4气体在一定条件下生成z2气体反应的热化学方程式____________________________ 。
(6)由上述元素中的y、z、e组成的某剧毒化合物eyz不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以较少污染。反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为__________________ 。已知eyz含有z2分子中类似的化学键,写出化合物eyz的电子式____________ 。

根据上述信息进行判断,并回答下列问题:
(1)h在元素周期表中的位置是
(2)比较f、g、h常见离子的半径大小
(3)下列可作为比较f和Mg金属性强弱的依据是
a.测两种元素单质的硬度和熔、沸点
b.测等浓度相应氯化物水溶液的pH
c.比较单质与同浓度盐酸反应的剧烈程度
d.比较两种元素在化合物中化合价的高低
(4)上述元素任选三种组成六原子共价化合物,写出其化学式
(5)据报道,最近意大利科学家获得了极具研究价值的z4,其分子结构与白磷分子的正四面体结构相似。已知断裂1 mol z-z键吸收167 kJ热量,生成1 mol Z≡Z键放出942 kJ热量,请写出z4气体在一定条件下生成z2气体反应的热化学方程式
(6)由上述元素中的y、z、e组成的某剧毒化合物eyz不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以较少污染。反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为
您最近一年使用:0次
解题方法
6 . A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)元素F在周期表中的位置________ 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)________ 。
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有______ 。检验该化合物中的阳离子的方法是________ (用离子方程式表示)。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出D元素的最高价氧化物对应的水化物与E的最高价氧化物反应的离子方程式:________________________ 。若E是非金属元素,其单质在电子工业中有重要应用,请写出其单质溶于强碱溶液的离子方程式:_______________ 。
(1)元素F在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出D元素的最高价氧化物对应的水化物与E的最高价氧化物反应的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
387次组卷
|
3卷引用:2015届山东齐鲁名校教科研协作体19所名校高三第二次调研化学试卷
7 . 各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。
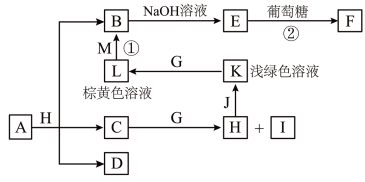
请回答下列问题:
(1)G元素在周期表中的位置_________________ ,C的电子式____________________ 。
(2)比较Y与Z的原子半径大小______ >________ (填写元素符号)。
(3)写出E和乙醛反应的化学反应方程式(有机物用结构简式表示)________ ;反应类型:_________ 。
(4)写出实验室制备G的离子反应方程式________________________________________ 。
(5)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为____________ 。
(6)实验室中检验L溶液中的阳离子常选用___________ 溶液,现象是_____________ 。
(7)A中包含X、Y、Z元素,A的化学式为____________ 。
(8)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其1种同素异形体的名称______________ 、____________ 。

请回答下列问题:
(1)G元素在周期表中的位置
(2)比较Y与Z的原子半径大小
(3)写出E和乙醛反应的化学反应方程式(有机物用结构简式表示)
(4)写出实验室制备G的离子反应方程式
(5)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为
(6)实验室中检验L溶液中的阳离子常选用
(7)A中包含X、Y、Z元素,A的化学式为
(8)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其1种同素异形体的名称
您最近一年使用:0次
解题方法
8 . (I)已知X.Y.Z.W为短周期四种常见元素,共中X是原子半径最小的元素,Y原子的最外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应也能与NaOH溶液反应。试回答下列问题:
(1)请写出下列元素的名称:Y____________,W____________.
(2)请写出X2Z2的电子式________________.
(3)请写出W元素的单质与NaOH溶液反应的离子方程式____________.
(II)A是由X、 Y、 Z和Cu四种元素组成的绿色固体,发生如下图所示转化(反应条件及部分产物已略去)。

常温下,D为无色无味气体,B为黑色粉末,75%的F水溶液常做医用消毒剂。请回答下列问题:
(4)D跟G反应的化学方程式____________________.
(5)E中含有官能团的名称__________。请写出检脸E中官能团的化学方程式_ ______________。.
(1)请写出下列元素的名称:Y____________,W____________.
(2)请写出X2Z2的电子式________________.
(3)请写出W元素的单质与NaOH溶液反应的离子方程式____________.
(II)A是由X、 Y、 Z和Cu四种元素组成的绿色固体,发生如下图所示转化(反应条件及部分产物已略去)。

常温下,D为无色无味气体,B为黑色粉末,75%的F水溶液常做医用消毒剂。请回答下列问题:
(4)D跟G反应的化学方程式____________________.
(5)E中含有官能团的名称__________。请写出检脸E中官能团的化学方程式_ ______________。.
您最近一年使用:0次
9 . 元素X、Y、Z、W、M、N原子序数依次增大,X与M、W与N分别同主族,且元素X、Y、Z、W分属两个短周期,它们四者原子序数之和为22,最外层电子数之和为16,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,请回答下列问题:
(1)Y元素在周期表中的位置是__________________________ ,X、Y、Z、W、M的原子半径由大到小的顺序为:_______________ (用元素符号表示)。
(2)写出Y2X2的电子式____________ ;Z2X4结构式 _______________ 。
(3)X、Z、W形成的化合物,水溶液一定显酸性的盐是______________ ,其原因是_____________ (用离子方程式表示),该物质所含化学键的类型是_____________ 。
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为_______________ 。
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式___________________ 。
(6)写出NW2通入硝酸钡溶液中的离子方程式______________ 。
(1)Y元素在周期表中的位置是
(2)写出Y2X2的电子式
(3)X、Z、W形成的化合物,水溶液一定显酸性的盐是
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式
(6)写出NW2通入硝酸钡溶液中的离子方程式
您最近一年使用:0次



