名校
解题方法
1 . 某种钾盐具有鲜艳的颜色,其阴离子结构如图所示。X、Y、Z为原子序数依次增加的短周期元素,X的一种同位素可以用于测定文物的年代,Y的一种氧化物是红棕色气体,Z的最高化合价与最低化合价的代数和为4,W在自然界中的含量位居第四。下列说法正确的是

| A.W的化合价为+3 |
| B.原子半径:Z>Y>X |
| C.Y的氧化物对应的水化物一定为强酸 |
| D.在该阴离子中,所有原子均满足最外层8电子结构 |
您最近一年使用:0次
名校
解题方法
2 . 元素X、Y、Z、W均属前4周期,基态X原子的2p轨道中成对电子与未成对电子相等;Y是地壳含量最多的金属元素;Z的单质常温下是黄绿色气体;基态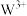 的3d轨道为半充满。下列说法正确的是
的3d轨道为半充满。下列说法正确的是
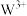 的3d轨道为半充满。下列说法正确的是
的3d轨道为半充满。下列说法正确的是
A.简单离子半径: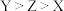 |
B.简单氢化物沸点: |
| C.Y与Z形成的化合物是电解质,熔融状态能导电 |
D. 晶胞的 晶胞的 结构如图所示, 结构如图所示,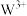 已标出, 已标出, 应位于c处 应位于c处 |
您最近一年使用:0次
3 . 同一短周期元素 、
、 、
、 、
、 的原子序数依次增大,其中
的原子序数依次增大,其中 被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是
被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是
 、
、 、
、 、
、 的原子序数依次增大,其中
的原子序数依次增大,其中 被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是
被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是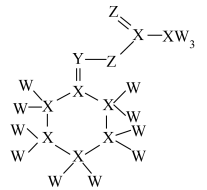
A.简单离子半径: |
B.元素的第一电离能: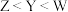 |
| C.分子中各原子最外层均满足8电子稳定结构 |
D.W的氢化物分子间形成了直线形氢键,故简单氢化物的沸点: |
您最近一年使用:0次
4 . 对金属材料中C、O、N、S的含量进行定性和定量分析,可以确定金属材料的等级。下列说法正确的是
| A.电离能大小:I1(N)>I1(O)>I1(S) | B.沸点高低:H2S>H2O>NH3 |
| C.酸性强弱:H2SO3>HNO3>H2CO3 | D.半径大小:r(S2-)>r(O2-)>r(N3-) |
您最近一年使用:0次
名校
5 . 某离子液体的阴离子结构如图所示,其中X、Y、Z、R、Q是原子序数依次增大的短周期非金属元素,其中X原子的最外层电子中未成对电子数目与成对电子数目相同,Z与Q同主族。下列说法正确的是

| A.电负性:Z>R>Q |
| B.简单离子半径:Q>Z>Y |
| C.五种元素形成的简单氢化物中沸点最高的是Z |
| D.该阴离子中∠Q—Y—Q为180° |
您最近一年使用:0次
2024-06-04更新
|
105次组卷
|
2卷引用:2024届贵州省贵阳市第一中学高三下学期三模化学试题
名校
6 . 化合物M(如图所示)可用于制备各种高性能防腐蚀涂料。W、X、Y、Z是原子序数依次增大的短周期主族元素,且占据三个不同周期,W与Z的质子数之和是X的2倍。下列说法不正确的是
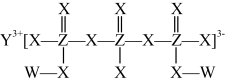
| A.原子半径:Y>Z>X |
| B.工业上电解熔融Y2X3化合物制备单质Y |
| C.X简单氢化物的稳定性大于Z简单氢化物的稳定性 |
| D.W与X形成的所有化合物都只含极性共价键 |
您最近一年使用:0次
名校
7 . 已知X、Y、Z、W、M为原子序数依次增大的前20号主族元素,且只有X、M为金属元素,Y的简单氢化物是最稳定的非金属氢化物。工业上用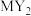 等物质制备电池电解质
等物质制备电池电解质 时,XY、
时,XY、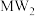 是其中间产物。下列叙述错误的是
是其中间产物。下列叙述错误的是
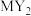 等物质制备电池电解质
等物质制备电池电解质 时,XY、
时,XY、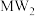 是其中间产物。下列叙述错误的是
是其中间产物。下列叙述错误的是A.XY与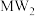 均是离子化合物 均是离子化合物 |
B. 分子中各原子最外层均满足8电子结构 分子中各原子最外层均满足8电子结构 |
| C.原子半径:M>Z>W |
| D.Z的最高价氧化物对应的水化物是强酸 |
您最近一年使用:0次
8 . Q、W、X、Y、Z为原子序数依次增大的前30号元素。W、X、Y同周期且相邻,W的基态原子各能级的电子数相同;Q和Z的基态原子都只有一个未成对电子,基态Z原子的其他电子层电子均处于饱和状态。由它们组成的某种离子的结构如图所示,其中Z显 价。下列说法错误的是
价。下列说法错误的是
 价。下列说法错误的是
价。下列说法错误的是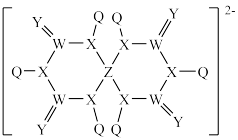
A.简单离子半径: |
B.电负性: |
| C.W、Y均可与Q形成至少两种化合物 |
D.最高价氧化物对应水化物的酸性: |
您最近一年使用:0次
名校
9 . 某水系离子电池的电解质的阴离子结构如下图所示,构成元素均为短周期元素,期中X、Y、Z、M在同一周期且原子序数依次增大。下列有关说法错误的是
| A.X、Y、Z、M原子半径依次减小 |
| B.X、Y、Z元素的简单氢化物的稳定性依次增强 |
| C.Y的最高价氧化物水化物是一种强酸 |
| D.XZ2和NZ2分子均为非极性分子 |
您最近一年使用:0次
名校
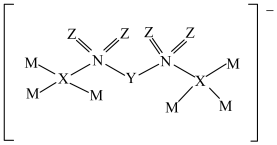
10 . 某有机离子液体结构为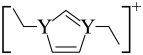
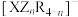 ,元素X、Y、Z、R为原子序数依次增大的短周期主族元素,基态Z原子的p能级电子总数比s能级电子总数多1,R与Z同主族。下列说法错误的是
,元素X、Y、Z、R为原子序数依次增大的短周期主族元素,基态Z原子的p能级电子总数比s能级电子总数多1,R与Z同主族。下列说法错误的是
A.分子极性: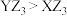 | B.同周期第一电离能大于X的元素有5种 |
| C.简单离子半径:R>Y>Z | D.该离子液体中存在离子键、极性键和配位键 |
您最近一年使用:0次
2024-05-24更新
|
238次组卷
|
3卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题



