名校
1 . 应用元素周期律可预测我们不知道的一些元素及其化合物的性质,下列预测正确的是
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液反应均产生氢气
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是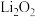 ,其溶液是一种强碱
,其溶液是一种强碱
⑤ 可能是难溶于水的白色固体
可能是难溶于水的白色固体
⑥ 无色,有毒,比
无色,有毒,比 稳定
稳定
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液反应均产生氢气
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是
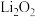 ,其溶液是一种强碱
,其溶液是一种强碱⑤
 可能是难溶于水的白色固体
可能是难溶于水的白色固体⑥
 无色,有毒,比
无色,有毒,比 稳定
稳定| A.①②③④ | B.②④⑥ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
2023-09-15更新
|
229次组卷
|
2卷引用:北京市十一学校2022-2023学年高三下学期1月月考化学试题
名校
解题方法
2 . 中国科学家经过光谱分析发现了一颗锂元素含量极高的恒星。下列说法不正确 的是
| A.LiOH的碱性弱于Be(OH)2 |
| B.在碱金属元素中,锂元素的金属键能最大 |
| C.依据对角线规则,锂元素和镁元素的有些性质相似 |
| D.原子光谱的产生与电子跃迁有关,可利用原子光谱中的特征谱线来鉴定锂元素 |
您最近一年使用:0次
21-22高二上·湖北·期末
3 . 下列示意图和化学用语内容正确,且表述相符的是(水合离子用相应离子符号表示)
| A | B | C | D |
 与 与 反应能量变化 反应能量变化 |  溶于水 溶于水 | 对角线规则 | 锌铜原电池工作原理 |
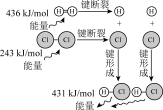 | 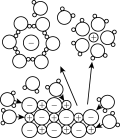 |  |  |
 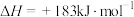 | 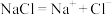 | 对角线元素及化合物性质具有相似性 | 盐桥主要作用是连接内电路和平衡电荷 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . X、Y、Z、M、N分别为五种原子序数不大于20的元素,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动状态不同的电子,Z元素形成的化合物在自然界中种类最多,M的阳离子通常存在于硝石、明矾和草木灰中,N的原子序数比M大1。下列说法正确的是
| A.熔点:Y4Z晶体低于单质Z |
| B.X与Al的某些化学性质相似,XO是两性氧化物 |
| C.M的阳离子半径是同周期主族元素的简单离子中半径最大的 |
| D.NZ2仅含离子键,可用于制备乙炔 |
您最近一年使用:0次
2020-09-25更新
|
276次组卷
|
4卷引用:北京市清华大学附属中学中学生标准学术能力基础性测试2021届高三9月测试化学试题
北京市清华大学附属中学中学生标准学术能力基础性测试2021届高三9月测试化学试题(已下线)北京市清华大学附属中学2021届高三上学期9月月考化学试题山东省济南市历城第二中学2022届高三上学期开学考试化学试卷(A)山东省聊城市第二中学2022-2023学年高三上学期开学考试化学试题
名校
5 . 金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是_________________ 。
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是_______________ (填字母)。
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因______________________________ 。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式________________________________________ 。
(1)铝在元素周期表中的位置是
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式
您最近一年使用:0次
6 . 元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在周期表的位置______________________ 。
(2)比较Be2+、Li+、H+微粒半径的大小_______________________ 。
(3)下列有关Be性质的推断正确的是_______________________ 。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点
c.常温时,BeCl2溶液的pH<7
(4)已知:Al4C3+ 12H2O === 4Al(OH)3 + 3CH4↑,写出Be2C与NaOH溶液反应的方程式(铍酸根离子:BeO22-)_________________________ 。
(1)Be元素在周期表的位置
(2)比较Be2+、Li+、H+微粒半径的大小
(3)下列有关Be性质的推断正确的是
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点
c.常温时,BeCl2溶液的pH<7
(4)已知:Al4C3+ 12H2O === 4Al(OH)3 + 3CH4↑,写出Be2C与NaOH溶液反应的方程式(铍酸根离子:BeO22-)
您最近一年使用:0次
名校
7 . X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
(1)Z在元素中期表中的位置是______________________________ 。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是__________ (填离子符号)。
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式______________________________ 。
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是____________________ 。
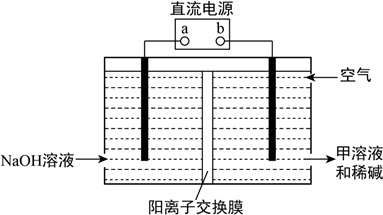
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是__________ 极,阴极的电极反应式是____________________ 。
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在元素中期表中的位置是
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是

您最近一年使用:0次
2018-01-10更新
|
237次组卷
|
4卷引用:北京市清华大学附属中学2018届高三10月月考化学试题
2014·北京西城·二模
8 . 已知:Li与Mg、Be与Al的性质相似。下列判断正确的是
| A.LiOH是强碱 |
| B.Be与冷水剧烈反应 |
| C.Li在空气中不易被氧化 |
| D.Be(OH)2能与NaOH溶液反应 |
您最近一年使用:0次



