名校
1 . 以下类比结论中正确的是
A. 的沸点高于 的沸点高于 ,则 ,则 的沸点高于 的沸点高于 |
B. 分子结构为直线形,则 分子结构为直线形,则 分子结构也是直线形 分子结构也是直线形 |
C. 能与 能与 溶液发生反应,则 溶液发生反应,则 也能与 也能与 溶液发生反应 溶液发生反应 |
D. 用作耐火材料,则 用作耐火材料,则 也可用作耐火材料 也可用作耐火材料 |
您最近一年使用:0次
2024-05-11更新
|
254次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
2 . 根据对角线规则,下列物质的性质具有相似性的是
| A.碳和铝 | B.铝和铁 | C.硼和硅 | D.铜和金 |
您最近一年使用:0次
名校
3 . 下表为周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)③基态原子的核外电子轨道表示式是___________ 。
(2)写出元素⑩的一价离子的核外电子排布式:___________ ,该元素属于___________ 区元素。
(3)由元素④构成的三原子分子的空间结构为___________ 。
(4)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:___________ (填化学式)。
(5)③与①以原子个数比为 形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为
形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为___________ ,X为___________ (极性分子或非极性分子)
(6)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑨ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑩ | |||||||||||||||||
(1)③基态原子的核外电子轨道表示式是
(2)写出元素⑩的一价离子的核外电子排布式:
(3)由元素④构成的三原子分子的空间结构为
(4)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:
(5)③与①以原子个数比为
 形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为
形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为(6)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
您最近一年使用:0次
4 . 指出下列反应的氧化剂和还原剂
(1)2H2+O2=2H2O:氧化剂_______ ;还原剂_______ 。
(2)4P+5O2=2P2O5:氧化剂_______ ;还原剂_______ 。
(3)Fe+H2SO4=FeSO4+H2 :氧化剂
:氧化剂_______ ;还原剂_______ 。
(4)WO3+3H2=W+3H2O:氧化剂_______ ;还原剂_______ 。
(5)已知 与
与 属于两性氢氧化物,写出
属于两性氢氧化物,写出 分别溶于
分别溶于 溶液、盐酸的化学方程式:
溶液、盐酸的化学方程式:_______ 、_______ 。
(1)2H2+O2=2H2O:氧化剂
(2)4P+5O2=2P2O5:氧化剂
(3)Fe+H2SO4=FeSO4+H2
 :氧化剂
:氧化剂(4)WO3+3H2=W+3H2O:氧化剂
(5)已知
 与
与 属于两性氢氧化物,写出
属于两性氢氧化物,写出 分别溶于
分别溶于 溶液、盐酸的化学方程式:
溶液、盐酸的化学方程式:
您最近一年使用:0次
解题方法
5 . 下列关于原子结构和性质的叙述中,正确的为
①2p、3p、4p能级的轨道数依次增多
②ds区全部是金属元素
③在一个原子轨道中最多能容纳2个电子且自旋相反,称为洪特规则
④Be和Al在化学性质上具有一定的相似性
⑤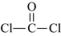 中的σ键与π键个数比为1:3
中的σ键与π键个数比为1:3
①2p、3p、4p能级的轨道数依次增多
②ds区全部是金属元素
③在一个原子轨道中最多能容纳2个电子且自旋相反,称为洪特规则
④Be和Al在化学性质上具有一定的相似性
⑤
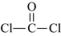 中的σ键与π键个数比为1:3
中的σ键与π键个数比为1:3| A.②④ | B.①②④ | C.②④⑤ | D.③④⑤ |
您最近一年使用:0次
名校
6 . W、X、Y、Z、M、R、Q均为短周期主族元素,其原子序数与原子半径关系如图所示。

请回答下列问题:
(1)R在元素周期表中的位置是_______ ;X的质量数分别为16和18的两种核素互为_______ 。
(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为_______ 。
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,W单质及其化合物与M单质及其化合物的性质相似,写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式_______ 。
(4)用电子式表示 形成过程
形成过程_______ , 与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式_______ 。

请回答下列问题:
(1)R在元素周期表中的位置是
(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,W单质及其化合物与M单质及其化合物的性质相似,写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式
(4)用电子式表示
 形成过程
形成过程 与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
您最近一年使用:0次
解题方法
7 . 下列说法不正确的是
| A.SiO2、GeO2结构相似均为原子晶体,但SiO2熔点较高,其原因是Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高 |
| B.只含原子的晶体一定是共价晶体 |
| C.干冰为分子晶体采用密堆积方式,一个CO2为中心,其周围最多可以有12个紧邻的分子 |
| D.根据对角线规则Li元素的某些性质与Mg元素的相似 |
您最近一年使用:0次
名校
解题方法
8 . 铍(4Be)的右下角元素是铝,根据“对角线规则”,下列描述不正确的
| A.BeO是两性氧化物 |
| B.Be(OH)2既能与H2SO4溶液反应也能与NaOH溶液反应 |
| C.Be(OH)2与NaOH溶液反应后生成Na2BeO2和H2O |
| D.BeCl2是离子化合物 |
您最近一年使用:0次
9 . 回答下列问题:
(1)Mn位于元素周期表中第四周期_______ 族。
(2)比较离子半径:F-_______ O2-(填“大于”“等于”或“小于)。
(3)Li+与H-具有相同的电子构型,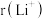 小于
小于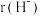 ,原因是
,原因是_______ 。
(4)在周期表中,与Li的化学性质最相似的邻族元素是_______ 。
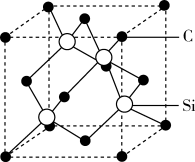
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示,则金刚砂晶体类型为_______ ;在SiC中,每个C原子周围最近的C原子数目为_______ ;若晶胞的边长为a pm,阿伏加德罗常数为 ,则金刚砂的密度表达式为
,则金刚砂的密度表达式为_______ 。
(1)Mn位于元素周期表中第四周期
(2)比较离子半径:F-
(3)Li+与H-具有相同的电子构型,
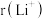 小于
小于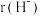 ,原因是
,原因是(4)在周期表中,与Li的化学性质最相似的邻族元素是
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示,则金刚砂晶体类型为
 ,则金刚砂的密度表达式为
,则金刚砂的密度表达式为
您最近一年使用:0次
10 . 在元素周期表中的某些元素之间存在着特殊的“对角线关系”,下列说法中错误的是
| A.氢氧化铍是两性氢氧化物 | B.锂的氧化物和钠一样,都有两种 |
C.锂在氮气中燃烧能生成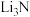 | D.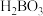 为弱酸 为弱酸 |
您最近一年使用:0次
2022-03-24更新
|
69次组卷
|
2卷引用:黑龙江省齐齐哈尔市2022-2023学年高二下学期4月期中考试化学试题



