名校
解题方法
1 . 五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的气态化合物在水中呈碱性,C和E形成化合物CE。下列说法正确的是( )
| A.D、E、B和C四种元素简单离子半径比较:C>D>E>B |
| B.B、D、E简单气态氢化物稳定性比较:B>D>E |
| C.E最高价氧化物对应水化物的化学式为HEO4 |
| D.C的单质在空气中燃烧产物的化学式为CO |
您最近一年使用:0次
2019-02-15更新
|
1917次组卷
|
4卷引用:山西省晋中市和诚中学2019-2020学年高一3月月考化学试题
名校
2 . 短周期元素X、Y、Z、W、R的原子序数依次增大,Y与W同主族,Z与R同主族,它们形成的甲、乙两种物质(如图所示)是有机合成中常用的还原剂。下列说法正确的是
甲: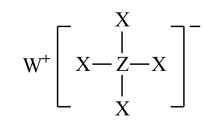 乙:
乙: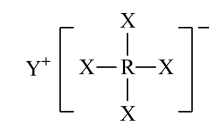
甲:
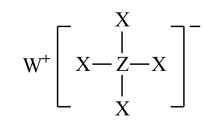 乙:
乙: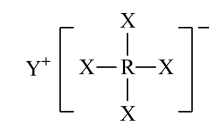
| A.电负性:X>R>Z |
| B.W形成的过氧化物在工业上常用做消毒剂 |
| C.单质Y和W在空气中燃烧的产物所含化学键类型完全相同 |
| D.甲、乙两化合物中的元素都满足8电子稳定结构 |
您最近一年使用:0次
2022-09-18更新
|
267次组卷
|
2卷引用:山西省榆次第一中学校 2022-2023学年高三上学期10 月模拟考试化学试题
名校
3 . 短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数。X与Y位于不同周期,X与W的最高化合价之和为8,元素Z的单质是目前使用量最大的主族金属元素单质。下列说法中正确的是
| A.化合物YX4W溶于水后,得到的溶液呈碱性 |
B.化合物YW3为共价化合物,电子式为 |
| C.Y、Z形成的一种化合物强度高,热膨胀系数小,是良好的耐热冲击材料 |
| D.原子半径大小:W>Z>Y>X |
您最近一年使用:0次
2019-03-28更新
|
1353次组卷
|
5卷引用:山西省晋中市和诚中学2019-2020学年高一3月月考化学试题
名校
解题方法
4 . 南京理工大学合成的一种离子化合物的局部结构如图所示,该物质由两种阳离子和两种阴离子构成,其中有两种10电子离子和一种18电子离子. 均为短周期元素,且均不在同一族.回答下列问题:
均为短周期元素,且均不在同一族.回答下列问题:
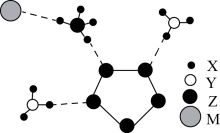
(1)M元素在元素周期表中的位置为______________ .
(2)该化合物中存在的化学键类型有______________ .
(3)该化合物中的两种10电子离子是______________ (填离子符号,下同),18电子离子是______________ .
(4) 形成的一种化合物具有很强的漂白性,写出它的电子式:
形成的一种化合物具有很强的漂白性,写出它的电子式:______________ .
(5) 和
和 的稳定性相对较强的是
的稳定性相对较强的是______________ (填化学式).
(6) 两元素的最高价氧化物对应水化物的酸性由强到弱的顺序是
两元素的最高价氧化物对应水化物的酸性由强到弱的顺序是______________ (用化学式表示).
(7) 和
和 在催化剂作用下可以反应生成
在催化剂作用下可以反应生成 和
和 ,写出该反应的化学方程式,并用单线桥法表示电子转移的方向和数目:
,写出该反应的化学方程式,并用单线桥法表示电子转移的方向和数目:____________________________ .
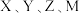 均为短周期元素,且均不在同一族.回答下列问题:
均为短周期元素,且均不在同一族.回答下列问题:
(1)M元素在元素周期表中的位置为
(2)该化合物中存在的化学键类型有
(3)该化合物中的两种10电子离子是
(4)
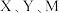 形成的一种化合物具有很强的漂白性,写出它的电子式:
形成的一种化合物具有很强的漂白性,写出它的电子式:(5)
 和
和 的稳定性相对较强的是
的稳定性相对较强的是(6)
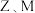 两元素的最高价氧化物对应水化物的酸性由强到弱的顺序是
两元素的最高价氧化物对应水化物的酸性由强到弱的顺序是(7)
 和
和 在催化剂作用下可以反应生成
在催化剂作用下可以反应生成 和
和 ,写出该反应的化学方程式,并用单线桥法表示电子转移的方向和数目:
,写出该反应的化学方程式,并用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
2024-02-02更新
|
200次组卷
|
2卷引用:山西省晋中市2023-2024学年高一上学期1月期末考试化学试题
11-12高一下·黑龙江·期末
名校
解题方法
5 . 图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )


| A.原子半径:Z>Y>X |
| B.气态氢化物稳定性:R<W |
| C.WX3和水反应生成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
您最近一年使用:0次
2020-03-25更新
|
684次组卷
|
47卷引用:2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷
(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2011-2012年黑龙江龙东地区高一下学期期末考试化学试卷(已下线)2011-2012学年吉林省长春市十一高中高一下学期期末考试化学试卷(已下线)2013届黑龙江省大庆实验中学高三上学期开学考试化学试卷(已下线)2012-2013学年湖北省黄冈中学高二上学期期中考试化学试卷(已下线)2012-2013学年四川省成都外国语学校高一下学期期中考试化学试卷(已下线)2013届山东省泰安市高三第二轮复习质量检测理综化学试卷(已下线)2014届上海市长宁区高三上学期期末(一模)考试化学试卷(已下线)2014年高考化学一轮复习课后规范训练5-2练习卷(已下线)2014届江西省南昌一中、南昌十中高三上学期联考化学试卷(已下线)2013-2014湖北省黄石市三中高一下学期期中考试化学试卷2014-2015学年河北省广平县第一中学高一4月月考理科化学试卷2014-2015学年吉林省长春市十一中高一下期中化学试卷2014-2015学年内蒙古霍林郭勒市第三中学高一下期中考试化学试卷2014-2015学年福建省永春美岭中学高一下学期期中考试化学试卷2015-2016学年上海市理工大学附属中学高二上学期期中测试化学试卷2015-2016学年江苏省清江中学高一下学期周练化学试卷2015-2016学年河北省定兴三中高一下3月月考(文)化学试卷辽宁省葫芦岛高级中学2015-2016学年高一下第一次月考化学卷2015-2016学年陕西西安长安一中高一下第一次月考化学卷2015-2016学年河南省周口市商水一中高一下学期期中考试化学试卷2015-2016学年福建省清流一中高一实验班下第三段测化学试卷2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷2016-2017学年江西省南昌市第二中学高一下学期第一次月考化学试卷2016-2017学年上海市金山区高三上期期末质量调研化学试卷河北省石家庄市第一中学2016-2017学年高一下学期期中考试化学试题山西省大同市第一中学2017-2018学年高一3月月考化学试题福建省莆田第六中学2017-2018学年高一6月月考B化学试题山西省实验中学2017-2018学年高一下学期第一次月考化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题安徽省砀山县第二中学2018-2019学年高一下学期第一次月考化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高二下学期4月月考化学试题上海市向明中学2018-2019学年高二第一学期期末考试化学试题(已下线)【新东方】2020-82(已下线)上海市宝山区2014届高三上学期期末教学质量监测化学试题上海市宝山区交大附中2017-2018学年高三上学期期中考试化学试题江苏省苏州市西安交通大学苏州附属中学2019-2020学年高一下学期自主检测化学试题山西省运城市永济涑北中学2019-2020学年高一下学期3月月考化学试题广东省茂名市信宜中学2019-2020学年高一下学期级线上段考化学试题北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题(已下线)5.1.2 元素周期表 元素周期表的应用练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)第04章 物质结构 元素周期律(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)第18讲 元素周期律和元素周期表(精练)-2021年高考化学一轮复习讲练测上海市行知中学2021届高三下学期3月月考化学试题甘肃省会宁县第一中学2020-2021学年高一下学期期中考试化学试题河南省洛阳市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
6 . W、X、Y、Z是原子序数依次增大的四种短周期元素。n、p、r是由这些元素组成的二元化合物。m 是元素W的单质。q是元素Y的单质且是制作太阳能电池的原料。p在常温下为常见无色液体,0.010mol·L-1的r溶液中c(H+)为0.010 mol·L-1,s是弱酸且不溶于水。上述物质的转化关系如图所示。下列说法不正确的是


| A.r易溶于p |
| B.原子半径:Z<Y |
| C.最高价氧化物对应水化物的酸性:Y<Z |
| D.最简单氢化物的稳定性:X<Y |
您最近一年使用:0次
2020-04-29更新
|
385次组卷
|
2卷引用:山西省晋中市和诚中学2019-2020学年高一4月月考化学试题
解题方法
7 . 有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题:
(1)D基态原子中能量最高的电子其原子轨道呈______ 形。
(2)G位于元素周期表的位置为:____________ ,位于______ 区,价电子排布式为______ 。
(3)写出由A、B、E三种元素形成的离子化合物的电子式____________ 。
(4)检验F元素的方法是____________ ,请用原子结构的知识解释产生此现象的原因是________________________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1个 |
C元素原子的第一至第四电离能分别是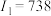 kJ·mol kJ·mol ; ;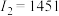 kJ·mol kJ·mol ; ;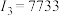 kJ·mol kJ·mol ; ;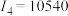 kJ·mol kJ·mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)G位于元素周期表的位置为:
(3)写出由A、B、E三种元素形成的离子化合物的电子式
(4)检验F元素的方法是
您最近一年使用:0次
名校
8 . 现有A、B、C、D四种短周期主族元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子均为10电子粒子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图所示。

(1)根据以上条件可以确定A、B、C、D四种元素中的三种元素。不能被确定的第四种元素是____ (填A、B、C、D中的一种)。
(2)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应;②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙=乙+丁的化学方程式:___________ 。
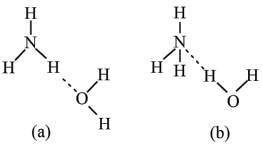
(3)NH3•H2O的电离方程式为NH3•H2O NH4++OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构
NH4++OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构 ________ (填字母代号)。

(1)根据以上条件可以确定A、B、C、D四种元素中的三种元素。不能被确定的第四种元素是
(2)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应;②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙=乙+丁的化学方程式:
(3)NH3•H2O的电离方程式为NH3•H2O
 NH4++OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构
NH4++OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构 
您最近一年使用:0次
2019-05-10更新
|
417次组卷
|
2卷引用:【全国百强校】山西省晋中市平遥中学2018-2019学年高一下学期期中考试化学试题
9 . 下表为元素周期表的一部分,表中的一个序号代表一种元素。某种融雪剂在机场、高速公路等地被广泛使用,该融雪剂的主要成分是由下表中部分元素(①~①)组成的化合物A(化学式为 )。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。
)。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。
(1)A的化学式为___________ ,该化合物中存在的化学键类型有___________ ;元素M在周期表中位置为___________ 。
(2)X、Z和③的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)⑥的单质在④的单质中燃烧的现象为___________ ,生成物的电子式为___________ 。
(4)⑥⑦①三种元素的氢氧化物,碱性由强到弱的顺序为___________ (填化学式)。
(5)元素⑨的单质和元素⑩的最高价氧化物的水化物反应的离子方程式为___________ 。
(6)我们可以利用如图装置通过实验比较元素②和⑧的非金属性强弱;从下列选项中选出实验所需的物质(已知: 不溶于水):
不溶于水):
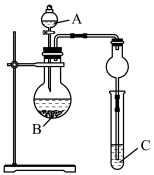
a.稀盐酸 b.稀硫酸
c.碳酸钙 d. 溶液
溶液
试剂A为___________ (填字母,下同);试剂C为___________ 。请指出该装置存在的一个缺陷:___________ 。
 )。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。
)。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。| 族 周期 | Ⅰ A | 0 | |||||||
| 1 | ① | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | ||
| 2 | ② | ③ | ④ | ⑤ | |||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | |||||
| 4 | ⑩ | ||||||||
(2)X、Z和③的原子半径由大到小的顺序为
(3)⑥的单质在④的单质中燃烧的现象为
(4)⑥⑦①三种元素的氢氧化物,碱性由强到弱的顺序为
(5)元素⑨的单质和元素⑩的最高价氧化物的水化物反应的离子方程式为
(6)我们可以利用如图装置通过实验比较元素②和⑧的非金属性强弱;从下列选项中选出实验所需的物质(已知:
 不溶于水):
不溶于水):
a.稀盐酸 b.稀硫酸
c.碳酸钙 d.
 溶液
溶液试剂A为
您最近一年使用:0次
名校
解题方法
10 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X、Z的原子最外层电子数之和为5;W与Y同族;X是形成化合物种类最多的元素,W的单质为常见气体,其水溶液具有漂白性。下列说法正确的是
| A.Y的最高正化合价为+7 |
| B.元素X的氢化物中,各原子均满足8电子的稳定结构 |
| C.Z的氧化物中阴阳离子个数比为1:2 |
| D.W的单质与过量的铁反应产物为FeW2 |
您最近一年使用:0次
2020-07-14更新
|
204次组卷
|
4卷引用:山西省晋中市祁县第二中学2019-2020学年高一下学期期末考试化学试题
山西省晋中市祁县第二中学2019-2020学年高一下学期期末考试化学试题山东省菏泽市第一中学2019-2020学年高一下学期期末模拟化学试题(已下线)第五单元 元素周期表和元素周期律测试题-2021年高考化学一轮复习名师精讲练山西省朔州市怀仁县大地学校2019-2020学年高二上学期第一次月考化学试题



