1 . 物质的类别和核心元素的化合价是研究物质性质的重要视角。下图是硫及其化合物的价类二维图,下列说法不正确的是
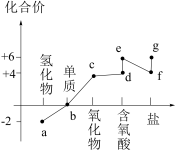

| A.向d的水溶液中滴加几滴紫色石蕊试液,溶液变红色,说明d的水溶液呈酸性 |
| B.b在过量O2中燃烧生成bO3 |
| C.图中由d转化为e需加入氧化剂 |
| D.将a与c混合,可生成淡黄色固体 |
您最近一年使用:0次
名校
2 . “医用酒精”和“84消毒液”混合,产生ZQ、X2W4Y、XW3Q等多种物质,已知W、X、Y、Z、Q为原子序数依次增大的短周期主族元素。下列叙述错误的是
| A.在XW3Q物质中X、W、Q均满足8电子稳定结构 |
| B.W与Z可形成离子化合物ZW |
| C.简单离子半径:Q->Y2->Z+ |
| D.简单气态氢化物热稳定性: Y>X |
您最近一年使用:0次
2022-03-17更新
|
261次组卷
|
3卷引用:广东省大联考2021-2022学年高一下学期期中检测化学试题
名校
3 . 短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径在短周期主族元素中最大,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,Z是同周期中电负性最强的元素。下列说法错误的是
A.最简单氢化物的稳定性: |
| B.Z的含氧酸均为强酸 |
| C.W和Y形成的物质可能为原子晶体(共价晶体) |
D.W、X形成的简单离子半径: |
您最近一年使用:0次
4 . 元素周期表反映元素之间的内在联系,是化学学习、研究和应用的一种重要工具。对元素周期表中有关元素的研究有利于认识能源物质及开发新能源。
(1)减少化石燃料使用有利于实现“碳中和”。碳位于周期表中____ 周期______ 族。
(2)我国储量丰富的可燃冰(CH4·nH2O)是清洁能源。16gCH4含________ mol 共价键。
(3)g单质是常用光伏电池材料,它可由 b单质与SiO2反应制得,化学方程式为______ 。
(4)比较非金属性强弱:h__ c__ d(填“>”或“<”)。
(5)a与i的单质均可用于高能电池材料,a与i的单质发生反应的化学方程式为________ 不要求写反应条件)。
(6)将下表中“对象”“原子半径”“性质”之间的正确关系用直线连接______ 。
| 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | a | b | c | D | |||||
| 3 | e | f | g | h | i | ||||
(2)我国储量丰富的可燃冰(CH4·nH2O)是清洁能源。16gCH4含
(3)g单质是常用光伏电池材料,它可由 b单质与SiO2反应制得,化学方程式为
(4)比较非金属性强弱:h
(5)a与i的单质均可用于高能电池材料,a与i的单质发生反应的化学方程式为
(6)将下表中“对象”“原子半径”“性质”之间的正确关系用直线连接
原子半径 | 对象 | 性质 |
大 b 比 g 气态氢化物的热稳定性高 小 e 比 f 最高价氧化物对应水化物碱性强 | ||
您最近一年使用:0次
名校
5 . 短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数。X与Y位于不同周期,X与W的最高化合价之和为8,元素Z的单质是目前使用量最大的主族金属元素单质。下列说法中正确的是
| A.化合物YX4W溶于水后,得到的溶液呈碱性 |
B.化合物YW3为共价化合物,电子式为 |
| C.Y、Z形成的一种化合物强度高,热膨胀系数小,是良好的耐热冲击材料 |
| D.原子半径大小:W>Z>Y>X |
您最近一年使用:0次
2019-03-28更新
|
1353次组卷
|
5卷引用:【市级联考】广东省揭阳市2019届高三高考第一次模拟考试理科综合化学试题
6 . X、Y、Z是短周期原子序数依次增大的主族元素,X是地壳中含量最多的元素,X和Z属于同一主族,Y原子的M层电子数为K层电子数的一半,三种元素组成的一种食品抗氧化剂M的结构如图所示,下列说法错误的是
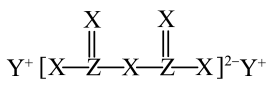
| A.最简单氢化物的稳定性:X>Z |
| B.Z元素最高价氧化物对应的水化物为强酸 |
| C.原子半径:Z>Y>X |
| D.M在熔融状态下能够导电 |
您最近一年使用:0次
2024-03-01更新
|
192次组卷
|
4卷引用:广东省惠州市实验中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
7 . 原子序数依次增大的短周期元素 X、Y、Z、R,含 0.9%YR的水溶液称为生理盐水,X、Y、Z三种元素组成两种化合物 A、B 的性质如图,Z的质子数是X质子数的2 倍。下列说法正确的是


| A.简单氢化物沸点 Z>X |
| B.简单离子半径 X<Y<Z<R |
| C.Y与X形成的一种化合物含有离子键和非极性键 |
| D.化合物 A 和 B的水溶液皆呈中性 |
您最近一年使用:0次
2021-03-03更新
|
535次组卷
|
4卷引用:广东省珠海市2021届高三第一次学业质量监测化学试题
广东省珠海市2021届高三第一次学业质量监测化学试题(已下线)小题15 元素周期表、律(根据物质性质角度的元素推断)——备战2021年高考化学经典小题考前必刷(全国通用)宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期5月月考化学试题
8 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
回答下列问题:
(1)W在元素周期表中的位置为___________ ,X的最高价氧化物对应的水化物的化学式为___________ 。
(2)Y的单质与水反应的离子方程式是___________ 。
(3)用电子式表示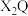 的形成过程:
的形成过程:___________ 。
(4)金属性:Y___________ (填“>”或“<”)X,用原子结构解释原因:___________ 。
(5)下列对于Z及其化合物的推断中正确的是___________ (填标号)。
A.Z的化合价中有-1和+7
B.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性
C.Z元素单质的氧化性强于W元素单质的氧化性
(6)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是___________ 。
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰呈紫色 |
| Z | 原子结构示意图为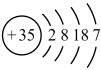 |
(1)W在元素周期表中的位置为
(2)Y的单质与水反应的离子方程式是
(3)用电子式表示
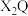 的形成过程:
的形成过程:(4)金属性:Y
(5)下列对于Z及其化合物的推断中正确的是
A.Z的化合价中有-1和+7
B.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性
C.Z元素单质的氧化性强于W元素单质的氧化性
(6)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是
您最近一年使用:0次
9 . 一种矿石(Z2X6Y11·5W2Y)的组成元素W、X、Y、Z为原子序数依次增大的1-20号元素,Z是牙齿的主要组成元素,W2Y分子中含有10个电子,X是一种非金属元素。下列说法正确的是
| A.Z的最高价氧化物的水化物是弱碱 | B.简单离子半径:Y>Z>W |
| C.X的单质在通常条件下是气体 | D.化合物ZY2中含有非极性共价键 |
您最近一年使用:0次
10 . A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期数与主族序数相等。请用化学用语 回答下列问题:
(1)B元素在周期表中的位置为_______ ;由A、C、D三种元素组成的化合物中含有的化学键为_______ 。
(2)写出BC2的电子式:_______ 。
(3)元素E的单质与元素D的最高价氧化物的水化物反应的离子方程式:_______ 。
(4)常温下,A2C与元素D的单质反应后,所得溶液的pH_______ 7(填“<”、“=”或“>”)。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,灼烧该化合物时,火焰呈_______ 色, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是_______ L。
(1)B元素在周期表中的位置为
(2)写出BC2的电子式:
(3)元素E的单质与元素D的最高价氧化物的水化物反应的离子方程式:
(4)常温下,A2C与元素D的单质反应后,所得溶液的pH
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,灼烧该化合物时,火焰呈
您最近一年使用:0次



