22-23高一上·全国·课时练习
名校
解题方法
1 . 联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。以下短周期主族元素中,含元素a的化合物被广泛用于制作手机电池,古迪纳夫因在该领域做出了杰出贡献荣获2019年诺贝尔化学奖。
(1)a原子结构示意图为_______ 。
(2)d在周期表中的位置是_______ 。
(3)元素g的单质与NaOH溶液反应的离子方程式为_______ 。
(4)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为_______ 。
(5)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为_______ 。
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应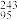 Am+
Am+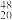 Ca→Mc+3
Ca→Mc+3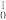 n得到。Mc用核素符号表示为
n得到。Mc用核素符号表示为_______ 。
| a | … | b | c | d | |||
| e | … | g | h | j |
(2)d在周期表中的位置是
(3)元素g的单质与NaOH溶液反应的离子方程式为
(4)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为
(5)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应
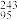 Am+
Am+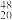 Ca→Mc+3
Ca→Mc+3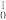 n得到。Mc用核素符号表示为
n得到。Mc用核素符号表示为
您最近一年使用:0次
22-23高一上·全国·课时练习
2 . 已知元素W、X、Y、Z为原子序数依次增大的短周期主族元素,其中W的最高价氧化物的水化物能与其气态氢化物反应生成离子化合物,X原子的最外层电子数是次外层电子数的一半,Y与W同主族,Z元素的单质常温下为气体。
(1)W与X可以形成一种高温结构陶瓷材料甲,其中W、X的化合价分别是它们各自的最低价和最高价,其化学式为___________ 。
(2)X、Y、Z的气态氢化物的稳定性由强到弱的顺序是___________ (用分子式表示)。
(3)W、Z的气态氢化物分别为乙和丙,X与Z元素形成的化学物为丁。结构陶瓷材料甲的一种合成方法的反应如下:①丁+乙→丙+戊;②戊→甲+乙
其中,戊中含有三种元素,原子个数比为1︰4︰8,上述反应均在高温下进行。请写出反应的化学方程式:
①___________ 。
②___________ 。
(1)W与X可以形成一种高温结构陶瓷材料甲,其中W、X的化合价分别是它们各自的最低价和最高价,其化学式为
(2)X、Y、Z的气态氢化物的稳定性由强到弱的顺序是
(3)W、Z的气态氢化物分别为乙和丙,X与Z元素形成的化学物为丁。结构陶瓷材料甲的一种合成方法的反应如下:①丁+乙→丙+戊;②戊→甲+乙
其中,戊中含有三种元素,原子个数比为1︰4︰8,上述反应均在高温下进行。请写出反应的化学方程式:
①
②
您最近一年使用:0次
解题方法
3 . 短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组成的氧化物;甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体;K是红棕色气体;丙的浓溶液具有强氧化性。上述物质的转化关系如图所示。下列说法不正确的是
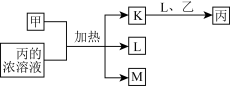

| A.K、L、M形成的晶体都是分子晶体 |
| B.X和Z形成的分子晶体中一定不存在非极性键 |
| C.L的沸点一定比X、Y组成的化合物沸点高 |
| D.由X、Y、Z、W构成的化合物中可能只含有共价键 |
您最近一年使用:0次
名校
解题方法
4 . 有三种物质 ,在常温下分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体
,在常温下分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体 ;元素D的负一价阴离子的电子层结构与氩原子相同。则:
;元素D的负一价阴离子的电子层结构与氩原子相同。则:
(1)A、B、C、D元素的名称分别为____ 、____ 、____ 、____ 。
(2)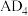 分子中含有的
分子中含有的 键类型为
键类型为____ (填“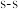 ”“
”“ ”或“
”或“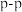 ”)
”) 键。
键。
(3)D的负一价阴离子的电子排布式为___________ , 属于
属于___________ (填“离子”或“共价”)化合物。
 ,在常温下分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体
,在常温下分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体 ;元素D的负一价阴离子的电子层结构与氩原子相同。则:
;元素D的负一价阴离子的电子层结构与氩原子相同。则:(1)A、B、C、D元素的名称分别为
(2)
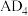 分子中含有的
分子中含有的 键类型为
键类型为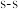 ”“
”“ ”或“
”或“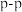 ”)
”) 键。
键。(3)D的负一价阴离子的电子排布式为
 属于
属于
您最近一年使用:0次
2022-08-22更新
|
515次组卷
|
4卷引用:专题3 微粒间作用力与物质性质 第三单元 共价键共价晶体 第1课时 共价键的形成及类型
5 . 现有六种元素A、B、C、D、E、F,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的轨道表示式为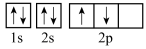 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了_______ 。
(2)B元素的电负性_______ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物所含有的化学键类型为_______ 。
(4)E基态原子中能量最高的电子,其电子云在空间有_______ 个伸展方向。
(5)下列关于F原子的价电子轨道表示式正确的是_______ 。
a.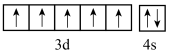 b.
b.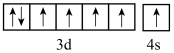
c. d.
d.
(6)基态 核外电子排布式为
核外电子排布式为_______ 。过量单质F与B的最高价氧化物对应的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为_______ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
D元素原子的第一至第四电离能分别是: ; ;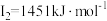 ; ;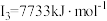 ; ; |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)B元素的电负性
(3)C与D形成的化合物所含有的化学键类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)下列关于F原子的价电子轨道表示式正确的是
a.
 b.
b.
c.
 d.
d.
(6)基态
 核外电子排布式为
核外电子排布式为
您最近一年使用:0次
2022-08-22更新
|
778次组卷
|
4卷引用:第一章 本章达标检测2
21-22高一上·甘肃兰州·期末
名校
6 . 四种短周期元素在元素周期表中的位置如图所示,T是地壳中含量最高的金属元素。下列说法不正确的是
Q | |||
T | R | W |
| A.W的氢化物比R的氢化物稳定 |
| B.T的最高价氧化物对应的水化物可能为强碱 |
| C.Q的原子半径比T的小 |
| D.W和Q的原子序数相差10 |
您最近一年使用:0次
2022-01-07更新
|
448次组卷
|
6卷引用:4.2.2 元素周期表和元素周期律的应用-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)4.2.2 元素周期表和元素周期律的应用-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)甘肃省兰州市教育局第四片区2021-2022学年高一上学期期末考试化学试题(已下线)专题33 元素的综合推断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)新疆生产建设兵团第二中学2022-2023学年高一上学期期末考试化学试题甘肃省民勤县第一中学2022-2023学年 高一下学期开学考试化学试题甘肃省武威市民勤县第一中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
7 . 几种短周期元素的原子半径及某些化合价见下表
分析判断下列说法正确的是
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A.D、H、J的氧化物分别为酸性氧化物、两性氧化物、碱性氧化物 |
| B.A、H、J的离子半径由大到小的顺序是A>J>H |
| C.G元素的单质不存在同素异形体 |
| D.I在DB2中燃烧生成两种化合物 |
您最近一年使用:0次
2021-12-27更新
|
2251次组卷
|
6卷引用:第二节 元素周期律 第1课时 元素性质的周期性变化规律
第二节 元素周期律 第1课时 元素性质的周期性变化规律(已下线)专题九 元素周期律 化学键(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)黑龙江省鹤岗市第一中学2022-2023学年高三上学期10月月考化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题1-5)黑龙江省大庆铁人中学2021-2022学年高一上学期期末考试化学试题
2021·全国·模拟预测
名校
解题方法
8 . 短周期主族元素A、W、X、Y、Z原子序数依次增大,W原子的最外层电子数是内层电子数的3倍,Y的简单离子半径在同周期元素中最小,Z的最高正价与最低负价绝对值之差为4,X与W形成的一种化合物可用供氧剂;X与A形成的离子化合物还原性很强,与水反应产生气体。下列说法不正确的是
| A.原子半径大小一定是X>Y>Z>W>A |
| B.分别与A形成的化合物的稳定性一定是W>Z |
| C.最高价氧化物对应的水化物,Y的既能与X的反应又能与Z的反应 |
| D.Y、Z的简单离子均能影响水的电离 |
您最近一年使用:0次
21-22高三上·江苏镇江·期中
名校
9 . X、Y、Z、W为原子序数依次增大的前四周期元素,X的一种单质是天然存在的最坚硬矿物质,Z原子最外层电子数为次外层电子数的三倍,W基态原子的价电子排布为3d64s2。下列说法正确的是
| A.原子半径:Z>Y>X |
| B.元素的第一电离能:Z>Y>X |
| C.X、Y最简单气态氢化物分子的键角:X>Y |
D.W2+价电子轨道表示式: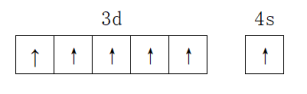 |
您最近一年使用:0次
2021-11-18更新
|
871次组卷
|
3卷引用:第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)
(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)湖南省常德市桃源县第一中学2022-2023学年高三上学期10月月考化学试题江苏省镇江市2021-2022学年高三上学期期中考试化学试题
20-21高二下·黑龙江大庆·期末
名校
10 . 几种短周期元素的原子半径及主要化合价如图所示,下列叙述不正确的是


| A.X、Y的最高价氧化物都可以作耐火材料 |
| B.Y的最高价氧化物对应的水化物能溶于稀氨水 |
| C.Z的非金属性小于W |
| D.X的单质可分别与Z、W的单质发生氧化还原反应 |
您最近一年使用:0次
2021-07-31更新
|
748次组卷
|
5卷引用:4.2.1 元素性质的周期性变化规律-2021-2022学年高一化学课后培优练(人教版2019必修第一册)
(已下线)4.2.1 元素性质的周期性变化规律-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)人教必修第一册第4章第2节第1课时元素性质的周期性变化规律(课后)(已下线)第四章 物质结构 元素周期律(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)黑龙江省大庆实验中学2020-2021学年高二下学期期末化学试题2021年天津高考化学试题变式题1-12



