1 . 周期表中特殊位置的短周期元素
①族序数等于周期数的元素:_______ ;
②族序数等于周期数2倍的元素:_______ ;
③族序数等于周期数3倍的元素:_______ ;
④周期数是族序数2倍的元素:_______ ;
⑤周期数是族序数3倍的元素是:_______ ;
⑥只有负价的元素是:_______ ;
⑦最高正价等于最低负价的元素是_______ 。
①族序数等于周期数的元素:
②族序数等于周期数2倍的元素:
③族序数等于周期数3倍的元素:
④周期数是族序数2倍的元素:
⑤周期数是族序数3倍的元素是:
⑥只有负价的元素是:
⑦最高正价等于最低负价的元素是
您最近半年使用:0次
名校
解题方法
2 . A+、B+、C-、D、E五种微粒(分子或离子),它们都分别含有10个电子,已知它们有如下转化关系:
①A++C- D+E↑ ②B++C-→2D
D+E↑ ②B++C-→2D
(1)写出①的离子方程式:________________________________________________________ ;
(2)除D、E外,请再写出两种含10个电子的分子:_______________________
(3)除A+、B+外,请再写出两种含10个电子的阳离子:__________________________________ 。
①A++C-
 D+E↑ ②B++C-→2D
D+E↑ ②B++C-→2D(1)写出①的离子方程式:
(2)除D、E外,请再写出两种含10个电子的分子:
(3)除A+、B+外,请再写出两种含10个电子的阳离子:
您最近半年使用:0次
名校
解题方法
3 . 根据元素周期表1~20号元素的性质和递变规律,回答下列问题:
(1)属于金属元素的有_________ 种,其中金属性最强的元素的单质与氧气反应生成的化合物的化学式为 _________ 、 _________ (填两种)。
(2)最高正化合价最高的元素是________ (填元素符号),其最高正化合价为__________ 。
(3)单质既能与盐酸反应,又能与NaOH溶液反应的是_________ ,并写出这两个方程式_________ ,________ 。
(4)第三周期中,原子半径最大的元素是(稀有气体元素除外)_____________ 。
(1)属于金属元素的有
(2)最高正化合价最高的元素是
(3)单质既能与盐酸反应,又能与NaOH溶液反应的是
(4)第三周期中,原子半径最大的元素是(稀有气体元素除外)
您最近半年使用:0次
名校
解题方法
4 . A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两种元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M层的电子数之和。
(1)A为___________ (填元素名称,下同),C为___________ ;
(2)写出E的电子式___________ 。
(3)A、B的一种化合物与E反应的化学方程式为___________ ;
(4)A、B两种元素形成的化合物属于___________ (填“离子”或“共价”)化合物;
(5)D的最高价氧化物对应的水化物的浓溶液和A的单质反应的化学方程式为___________ 。
(1)A为
(2)写出E的电子式
(3)A、B的一种化合物与E反应的化学方程式为
(4)A、B两种元素形成的化合物属于
(5)D的最高价氧化物对应的水化物的浓溶液和A的单质反应的化学方程式为
您最近半年使用:0次
5 . 已知有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,B、C组成的某一种化合物能引起温室效应.常温下,金属D单质投入水中能与水剧烈反应.常温下E单质是常见的气体.请按要求回答下列几个问题:
(1)B、D的元素名称分别为:_____ 、_____ ;
(2)E在周期表中的位置为:_____ ,
(3)C离子的结构示意图为:_____ ;
(4)B、C、D三种元素的原子半径从大到小的顺序为_____ (用元素符号表示);
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:_____ (用对应的化学式表示)
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:_____ ;
(7)写出E与水反应的离子方程式:_____ .
(1)B、D的元素名称分别为:
(2)E在周期表中的位置为:
(3)C离子的结构示意图为:
(4)B、C、D三种元素的原子半径从大到小的顺序为
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:
(7)写出E与水反应的离子方程式:
您最近半年使用:0次
2018-12-23更新
|
1263次组卷
|
5卷引用:甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(实验班)试题
名校
6 . 随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
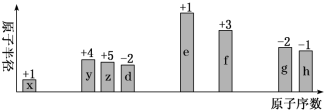
根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
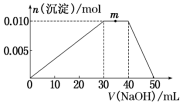
(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________ 。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是
(2)写出m点反应的离子方程式:
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近半年使用:0次
2018-09-24更新
|
250次组卷
|
4卷引用:甘肃省师范大学附属中学2019届高三上学期第一次月考化学试题
7 . 在1~18号元素中,稀有气体元素除外(请用元素符号或化学式表示):
(1)原子半径最大的元素是___________ ;
(2)最外层电子数是内层电子数的一半的元素__________________ ;
(3)单质还原性最强的元素是__________________ ;
(4)最高价氧化物对应的水化物酸性最强的是_____________ ;
(5)最高正价与负价的绝对值之差为6的元素是_________ ;
(6)常温下既能溶于强酸,又能溶于强碱的氧化物是__________________ ;
(1)原子半径最大的元素是
(2)最外层电子数是内层电子数的一半的元素
(3)单质还原性最强的元素是
(4)最高价氧化物对应的水化物酸性最强的是
(5)最高正价与负价的绝对值之差为6的元素是
(6)常温下既能溶于强酸,又能溶于强碱的氧化物是
您最近半年使用:0次
10-11高一下·甘肃天水·阶段练习
解题方法
8 . 有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1) A2B2的电子式为____________ 。
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。
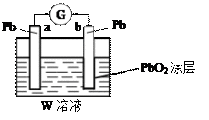
在b电极上发生的反应可表示为:PbO2+4H++SO +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________ 。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为____________________________________ 。
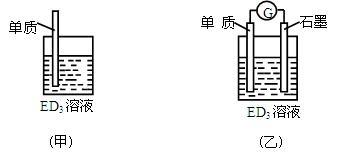
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池,则在该原电池工作时,石墨一极发生的反应可以表示为_____________________ 。比较甲、乙两图,说明石墨除形成闭合回路外所起的作用是_______________ 。
(1) A2B2的电子式为
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。

在b电极上发生的反应可表示为:PbO2+4H++SO
 +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为

(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池,则在该原电池工作时,石墨一极发生的反应可以表示为
您最近半年使用:0次
12-13高三上·甘肃兰州·期末
9 . 表为元素周期表的一部分,A、B、C、D、E、X、Y是表中给出元素组成的常见单质或化合物。
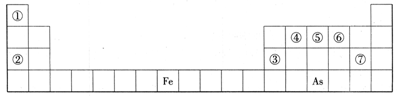
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
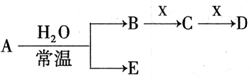
(1)若E为单质气体,D为白色沉淀, C与X反应的离子方程式为________ 。
(2)若E为氧化物,则A的化学式为_______ ,A与水反应的化学方程式为_______ 。
①当X是显碱性的盐溶液,C分子中有22个电子时,则C的电子式为______ ,表示X呈碱性的离子方程式为________ 。
②当X为金属单质时,X与B的稀溶液反应生成C的离子方程式为______ 。

已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)

(1)若E为单质气体,D为白色沉淀, C与X反应的离子方程式为
(2)若E为氧化物,则A的化学式为
①当X是显碱性的盐溶液,C分子中有22个电子时,则C的电子式为
②当X为金属单质时,X与B的稀溶液反应生成C的离子方程式为
您最近半年使用:0次



