名校
解题方法
1 . 物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,实验室中常用CS2洗涤残留在试管壁上的N单质。下列说法正确的是
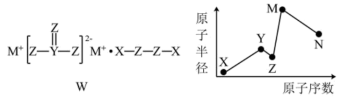

| A.简单阴离子的还原性:Z>N |
| B.Z的氢化物的沸点一定大于Y的氢化物的沸点 |
| C.Z、M、N三种元素形成化合物的水溶液呈中性 |
| D.X、Z形成的化合物与M、N形成的化合物可能发生氧化还原反应 |
您最近一年使用:0次
2022-10-29更新
|
138次组卷
|
2卷引用:内蒙古赤峰二中2023届高三上学期10月第二次月考化学试题
名校
解题方法
2 . a、b、c、d为四种由短周期元素构成的中性粒子,它们都有14个电子,且粒子内部以共价键结合。请回答下列问题。
(1)a单质由原子组成,a单质可用作半导体材料,a原子核外电子排布式为____ 。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为____ 。人一旦吸入b气体后,就易引起中毒,是因为____ 。
(3)c是双核单质,写出其电子式:____ 。分子中所含共价键的类型为____ (填“极性键”或“非极性键”)。
(4)d是四核化合物,其结构式为____ ;d分子内σ键与π键的强度大小关系为σ___ π(填“>”“<”或“=”),原因是____ 。
(1)a单质由原子组成,a单质可用作半导体材料,a原子核外电子排布式为
(2)b是双核化合物,常温下为无色无味气体。b的化学式为
(3)c是双核单质,写出其电子式:
(4)d是四核化合物,其结构式为
您最近一年使用:0次
名校
解题方法
3 . 短周期元素A、B、C、D的原子序数依次增大,X、Y、Z、W是由这四种元素中的两种元素组成的常见化合物,X为有刺激性气味的气体,Y为淡黄色固体,甲是由C元素形成的气体单质,乙为红棕色气体,上述物质之间的转化关系如图所示(部分反应物或生成物省略)。
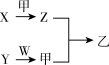
(1)A、B、C、D的原子半径大小顺序为_______ 。(用元素符号表示)
(2)B、C的气态氢化物的稳定性顺序为_______ 。(用化学式表示)
(3)B的最高价氧化物的水化物为_______ 。(用化学式表示)
(4)Y生成甲的化学方程式_______ 。
(5)若Z与甲反应生成1.12L乙(标准状况下),则该反应转移的电子数目为_______ 。

(1)A、B、C、D的原子半径大小顺序为
(2)B、C的气态氢化物的稳定性顺序为
(3)B的最高价氧化物的水化物为
(4)Y生成甲的化学方程式
(5)若Z与甲反应生成1.12L乙(标准状况下),则该反应转移的电子数目为
您最近一年使用:0次
名校
4 . A、B、C、D为短周期元素,请根据下表信息回答问题。
(1)D元素的名称为_______ ,其最高价氧化物对应的水化物化学式为_______ 。
(2)B气态氢化物的电子式_______ 。
(3)C的最高价氧化物与强碱反应的离子方程式为_______ 。
(4)D的单质与A的一种氢化物反应生成具有漂白性的物质的化学方程式为_______ 。
| 元素 | A | B | C | D |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
(2)B气态氢化物的电子式
(3)C的最高价氧化物与强碱反应的离子方程式为
(4)D的单质与A的一种氢化物反应生成具有漂白性的物质的化学方程式为
您最近一年使用:0次
名校
5 . 有A—F六种短周期元素,它们的结构、性质等信息如下表所示:
请根据表中信息回答下列问题
(1)A元素原子的核外价电子排布图为_______ 。
(2)B元素在元素周期表中的位置为_______ ;离子半径:B_______ A(填“>”或“<”)。
(3)C元素可形成[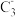 ]离子,试利用等电子原理写出其电子式
]离子,试利用等电子原理写出其电子式_______ 。
(4)第四周期中与D元素原子具有相同的未成对电子数的元素有_______ 种。
(5)E元素的气态氢化物是_______ 分子(填极性或非极性)。
(6)F元素的阴离子[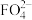 ]的等电子体中属于分子的是
]的等电子体中属于分子的是_______ 。(写1个)
(7)R元素形成的+1价阳离子的原子结构示意图_______ 。R元素形成的配合物 中存在
中存在_______ (填标号)。
A.离子键 B.σ键 C.π键 D、氢键
| 元素 | 结构,性质等信息 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易落于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
| F | 与E同主族 |
| R | 基态原子M层全充满,N层只有一个电子 |
(1)A元素原子的核外价电子排布图为
(2)B元素在元素周期表中的位置为
(3)C元素可形成[
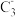 ]离子,试利用等电子原理写出其电子式
]离子,试利用等电子原理写出其电子式(4)第四周期中与D元素原子具有相同的未成对电子数的元素有
(5)E元素的气态氢化物是
(6)F元素的阴离子[
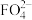 ]的等电子体中属于分子的是
]的等电子体中属于分子的是(7)R元素形成的+1价阳离子的原子结构示意图
 中存在
中存在A.离子键 B.σ键 C.π键 D、氢键
您最近一年使用:0次
名校
6 . 短周期主族元素X、Y、Z、W的原子序数依次增大,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物 的结构式为
的结构式为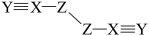 。下列说法正确的是
。下列说法正确的是
A.第一电离能: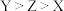 |
| B.W位于元素周期表的s区 |
C.电负性: |
D.简单气态氢化物的热稳定性: |
您最近一年使用:0次
2021-07-02更新
|
378次组卷
|
9卷引用:内蒙古赤峰二中2021-2022学年高二下学期第二次月考化学试题
内蒙古赤峰二中2021-2022学年高二下学期第二次月考化学试题湖南省郴州市2021-2022学年高二下学期期末考试化学试题安徽省亳州市第二中学2021-2022学年高二下学期期末考试化学试题河南省开封市官庄乡联合中学2022-2023高三上学期开学考试化学试题江西省九江市濂溪区第一中学2022-2023学年高二上学期期末考试化学试题陕西省汉中市西乡县第一中学2023-2024学年高二下学期3月月考化学试题江苏省徐州市2020-2021学年高二下学期期末抽测化学试题吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二下学期4月期中考试化学试题
名校
7 . 几种短周期元素的原子半径及主要化合价见下表:
根据表中信息,判断以下说法正确的是
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2、+4、+6 | +3 | -2 |
| A.单质与稀硫酸反应的速率快慢:R>Y>X | B.离子半径:X2+ >T2- |
| C.元素最高价氧化物对应的水化物的碱性:Y > R >X | D.相同条件下,气态氢化物的稳定性:T>Z |
您最近一年使用:0次
2018-04-28更新
|
625次组卷
|
16卷引用:内蒙古赤峰市元宝山区第一中学2021-2022学年高一下学期4月月考化学试题
内蒙古赤峰市元宝山区第一中学2021-2022学年高一下学期4月月考化学试题四川省遂宁中学校2021-2022学年高一下学期6月月考化学试题四川省南充市第一中学2021-2022学年高一下学期6月月考化学试题四川省达州市第一中学校2021-2022学年高一下学期第一次月考化学试题【全国百强校】四川省成都市第七中学2018-2019学年高一下学期3月月考化学试题四川省遂宁市射洪县射洪中学校2019-2020学年高一下学期第一次学月考试化学试题四川省成都外国语学校2020-2021学年高一4月月考化学试题四川省南充市李渡中学2020-2021学年高一下学期第二次月考化学试题四川省成都市东部新区2021-2022学年高一下学期期中考试化学试题四川省广元市八二一中学2021-2022学年高一下学期期中考试化学试题成都外国语学校2017-2018学年高一下学期期中考试化学试题湖北省荆门市2019-2020学年高一下学期期末考试化学试题(已下线)【全国百强校】四川省棠湖中学2018-2019学年高一下学期期中考试化学试题专题5 第一单元 元素周期律和元素周期表 第2课时 元素周表及其应用-高中化学苏教2019版必修第一册江西省景德镇一中2020-2021学年高一下学期期中考试化学试题四川省广安友谊中学2020-2021学年高一下学期半期考试化学试题
名校
8 . 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )
| X | |||||
| Y | Z | W | Q | ||
| A.尽管X与W同族,但W的化合物有多种价态而X的化合物只能形成-2价 |
| B.其最高价氧化物对应的水化物的酸性由弱到强的顺序是元素Q、W 、Z |
| C.Y、Z的常见氧化物可通过加入过量的NaOH溶液来分离. |
| D.Y单质做的容器可盛装W的最高价含氧酸的浓溶液 |
您最近一年使用:0次
2018-03-13更新
|
195次组卷
|
4卷引用:内蒙古赤峰市元宝山区第一中学2021-2022学年高一下学期4月月考化学试题



