解题方法
1 . 四种短周期元素X、Y、Z和W在周期表中的位置如图所示,它们的原子序数之和为43。下列说法不正确 的是
| X | Y | |
| Z | W | |
| Q |
A.原子半径(r):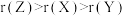 |
| B.Y、Z、W元素在自然界中均存在游离态 |
| C.Q的原子序数为32,Q元素的单质可作半导体材料 |
| D.X的最简气态氢化物比Y的最简气态氢化物沸点低,热稳定性差 |
您最近一年使用:0次
2 . 化合物[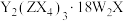 ](
]( )由
)由 、
、 、
、 、
、 四种原子序数依次增大的短周期主族元素构成,原子序数相加为38。
四种原子序数依次增大的短周期主族元素构成,原子序数相加为38。 分子总电子数为偶数,常温下为气体。该化合物的热重曲线如图所示,在
分子总电子数为偶数,常温下为气体。该化合物的热重曲线如图所示,在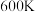 以下分解无刺激性气体逸出。下列叙述正确的是
以下分解无刺激性气体逸出。下列叙述正确的是

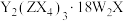 ](
]( )由
)由 、
、 、
、 、
、 四种原子序数依次增大的短周期主族元素构成,原子序数相加为38。
四种原子序数依次增大的短周期主族元素构成,原子序数相加为38。 分子总电子数为偶数,常温下为气体。该化合物的热重曲线如图所示,在
分子总电子数为偶数,常温下为气体。该化合物的热重曲线如图所示,在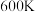 以下分解无刺激性气体逸出。下列叙述正确的是
以下分解无刺激性气体逸出。下列叙述正确的是
A. 、 、 、 、 的单质常温下均为气体 的单质常温下均为气体 |
B.最高价氧化物对应水化物的酸性: |
C.升温到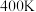 ,热分解失去晶体结构中的18个 ,热分解失去晶体结构中的18个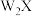 |
D. 以上温度下热分解后生成固体为 以上温度下热分解后生成固体为 |
您最近一年使用:0次
解题方法
3 . 分子TCCA(结构式如图)是一种高效消毒漂白剂。W、X、Y、Z处于两个不同短周期且原子序数依次递增的主族元素,Y的最外层电子数是电子层数的3倍。下列叙述正确的是
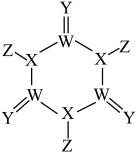

| A.元素Y与W形成的化合物一定含有离子键 |
| B.元素Z与X之间形成了非极性键 |
| C.该分子中所有原子最外层均满足8电子结构,且无孤电子对存在 |
D.该分子可发生水解反应生成物质 ,该水解液具有漂白功能 ,该水解液具有漂白功能 |
您最近一年使用:0次
解题方法
4 . 某新型电池材料结构如图所示,X、Y、Z、M、W是同周期主族元素,其中除M外均能满足8电子稳定结构,而X的最外层电子数是W次外层电子数的3倍,下列说法正确的是


| A.最简单氢化物的热稳定性和沸点均为Y<X |
| B.原子半径;Y<X<Z<W,离子半径:Y<X |
C.M的单质需保存在煤油中,W的氢化物常表示为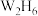 |
| D.W的最高价氧化物对应的水化物是一种三元弱酸 |
您最近一年使用:0次
解题方法
5 . A、B、C、D、F是周期表中前四周期的元素,其有关性质或结构信息如表:
(1) 、
、 元素的第一电离能
元素的第一电离能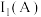
_______ 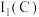 ;
;
(2) 元素原子的核外电子排布式为
元素原子的核外电子排布式为_______ ;
(3)B元素最高价含氧酸比D元素最高价含氧酸的酸性_______ (填“强”或“弱”);
(4) 单质分子中
单质分子中 键和
键和 键的个数比为
键的个数比为_______ ,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是_______ ;
(5)用高能射线照射液态 时,一个
时,一个 分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:
分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:_______ ;写出该阳离子与硫的氢化物的水溶液反应的离子方程式:_______ 。
| 元素 | 有关性质或结构信息 |
 | 负二价的 元素的氢化物在通常状况下是一种液体,其中 元素的氢化物在通常状况下是一种液体,其中 的质量分数为 的质量分数为 |
 |  原子得到一个电子后 原子得到一个电子后 轨道全充满 轨道全充满 |
 |  原子的 原子的 轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应 轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应 |
 |  元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体 元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体 |
 |  元素的核电荷数比 元素的核电荷数比 原子和 原子和 原子的核电荷数之和少1 原子的核电荷数之和少1 |
 、
、 元素的第一电离能
元素的第一电离能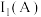
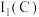 ;
;(2)
 元素原子的核外电子排布式为
元素原子的核外电子排布式为(3)B元素最高价含氧酸比D元素最高价含氧酸的酸性
(4)
 单质分子中
单质分子中 键和
键和 键的个数比为
键的个数比为(5)用高能射线照射液态
 时,一个
时,一个 分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:
分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:
您最近一年使用:0次
22-23高一上·浙江·阶段练习
解题方法
6 . 原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1原子核内质子数是2n2-1。下列有关X的说法中不正确的是
| A.X能形成氢化物可能呈碱性 |
| B.X可能形成化学式为KXO3的含氧酸钾盐 |
| C.X原子的最外层电子数和核电荷数可能为奇数 |
| D.X能与某些金属元素形成化合物 |
您最近一年使用:0次
7 . 元素在周期表中的位置反映了元素的原子结构和性质,矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1)Al元素在元素周期表中的位置为_____ ,K2O的电子式为_____ 。
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为_____ 。
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第_____ 族。
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是_____ 。
(1)Al元素在元素周期表中的位置为
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是
您最近一年使用:0次
名校
8 . 几种短周期元素的原子半径及主要化合价如表,下列说法正确的是
| 元素代号 | X | Y | Z | N | M | R | Q |
| 原子半径/nm | 0.37 | 1.86 | 1.43 | 0.88 | 0.99 | 0.75 | 0.74 |
| 最高正价 | +1 | +1 | +3 | +3 | +7 | +5 | |
| 最低负价 | -1 | -1 | -3 | -2 |
| A.由元素X、R、Q组成的化合物只能是共价化合物 |
| B.由水溶液的酸性:HM>H2S(氢硫酸),可推断元素的非金属性:M>S |
| C.Y和Q形成的两种常见化合物中,阴、阳离子个数比不同 |
| D.Y、Z、M三种元素的最高价氧化物的水化物两两之间能反应 |
您最近一年使用:0次
2023-01-04更新
|
283次组卷
|
3卷引用:浙江省绍兴市2022-2023学年高一上学期期末统测化学试题
名校
解题方法
9 . X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的元素;在同周期元素中,第一电离能数值比Y大的元素有2种;Z元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是
;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是
 ;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是
;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是| A.电负性:X<Y<Z | B.键角: |
C. 的阴阳离子比为 的阴阳离子比为 | D.W元素位于元素周期表的ds区 |
您最近一年使用:0次
2023-01-01更新
|
521次组卷
|
2卷引用:浙江省镇海中学2022-2023学年高三上学期12月模拟考试化学试题
2022·浙江·模拟预测
解题方法
10 . 几种短周期元素的原子半径及主要化合价如表:
下列说法不正确的是
| 元素代号 | X | Y | Z | W | M | |
原子半径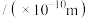 | 1.86 | 1.43 | 0.99 | 1.60 | 0.75 | |
| 主要化合价 | 最高正价 |  |  |  |  |  |
| 最低负价 | - | - |  | - |  | |
| A.M和Z简单氢化物的沸点:M>Z |
| B.X、Y、Z的最高价氧化物对应的水化物可相互反应 |
C.离子半径: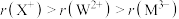 |
| D.W的单质与M的单质可反应生成离子化合物 |
您最近一年使用:0次



