名校
解题方法
1 . 某汽车安全气囊的产气药剂主要含有 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
(1) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。
① 的电子式为
的电子式为_______ 。
②Na与冷水常温下发生反应,请写出该反应的化学方程式_______ 。
(2) 含有的化学键类型为
含有的化学键类型为_______ 。
(3)从结构组成的分类, 属于
属于_______ (选填“离子化合物”或“共价化合物”),请写出鉴别离子化合物和共价化合物的方法:_______ 。
(4)某些安全气囊产气药剂中含 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: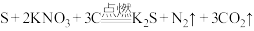
①标出该化学方程式电子转移的方向和数目_______ 。
②其中生成物 的电子式为
的电子式为_______ ; 的结构式为
的结构式为_______ 。
(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是_______ ,该元素单核负离子的结构示意图为_______ 。
 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:(1)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。①
 的电子式为
的电子式为②Na与冷水常温下发生反应,请写出该反应的化学方程式
(2)
 含有的化学键类型为
含有的化学键类型为(3)从结构组成的分类,
 属于
属于(4)某些安全气囊产气药剂中含
 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: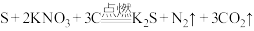
①标出该化学方程式电子转移的方向和数目
②其中生成物
 的电子式为
的电子式为 的结构式为
的结构式为(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是
您最近一年使用:0次
名校
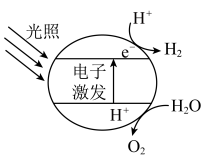
2 . 将半导体光催化剂浸入电解质溶液中,光照,可在表面得到产物。下图为原理示意图。 光解过程中断裂的化学键是___________。
光解过程中断裂的化学键是___________。
(2)若将该催化剂置于 溶液中,产物之一为
溶液中,产物之一为 ,另一产物为
,另一产物为___________ 。
 光解过程中断裂的化学键是___________。
光解过程中断裂的化学键是___________。| A.离子键 | B.共价键 | C.离子键和共价键 | D.氢键 |
(2)若将该催化剂置于
 溶液中,产物之一为
溶液中,产物之一为 ,另一产物为
,另一产物为
您最近一年使用:0次
名校
3 . 有下列物质:① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。
(1)上述物质中既含共价键又含离子键的是___________ (选填数字编号,下同);属于共价化合物的是___________ ;属于非极性分子的化合物是___________ 。
(2)④溶于水时破坏___________ ,固体⑦熔化时破坏___________ 。
A.离子键 B.共价键
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。(1)上述物质中既含共价键又含离子键的是
(2)④溶于水时破坏
A.离子键 B.共价键
您最近一年使用:0次
名校
解题方法
4 . 钠、铝等金属及其材料在人类文明进步和社会发展中发挥了重要的作用。
(1)请用一个离子方程式说明钠与铝的金属性强弱___________ 。
(2)叠氮化钠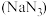 是一种无色结晶,其固体中正负离子的个数比为
是一种无色结晶,其固体中正负离子的个数比为 ,则该固体中含有的化学键是
,则该固体中含有的化学键是___________ (填化学键名称)。叠氮化钠受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32L(标准状况下)氮气,至少需要叠氮化钠___________ g。
(3)在含0.1molNaOH的溶液中不断地通入 ,得到溶质的质量为8.35g,则烧杯中生产的溶质是
,得到溶质的质量为8.35g,则烧杯中生产的溶质是___________ 。溶质的物质的量是___________ 。
(4)高锰酸根离子 水对人体危害极大,可用过碳酸钠
水对人体危害极大,可用过碳酸钠 改性赤泥进行处理,反应如下:
改性赤泥进行处理,反应如下:
___________ ___________
___________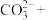 ___________
___________ ___________
___________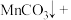 ___________
___________ ___________
___________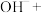 ___________H2O
___________H2O
补全并配平上述化学反应过程式___________ ;反应中,过碳酸钠起沉淀剂和___________ 剂作用;若将1L含Mn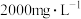 的含高锰酸根离子的废水处理至含Mn
的含高锰酸根离子的废水处理至含Mn ,则转移电子数为
,则转移电子数为___________ mol(保留2位小数)。
(1)请用一个离子方程式说明钠与铝的金属性强弱
(2)叠氮化钠
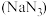 是一种无色结晶,其固体中正负离子的个数比为
是一种无色结晶,其固体中正负离子的个数比为 ,则该固体中含有的化学键是
,则该固体中含有的化学键是(3)在含0.1molNaOH的溶液中不断地通入
 ,得到溶质的质量为8.35g,则烧杯中生产的溶质是
,得到溶质的质量为8.35g,则烧杯中生产的溶质是(4)高锰酸根离子
 水对人体危害极大,可用过碳酸钠
水对人体危害极大,可用过碳酸钠 改性赤泥进行处理,反应如下:
改性赤泥进行处理,反应如下:___________
 ___________
___________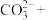 ___________
___________ ___________
___________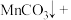 ___________
___________ ___________
___________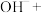 ___________H2O
___________H2O补全并配平上述化学反应过程式
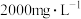 的含高锰酸根离子的废水处理至含Mn
的含高锰酸根离子的废水处理至含Mn ,则转移电子数为
,则转移电子数为
您最近一年使用:0次
名校
5 . 无机物可根据其组成和性质进行分类。现有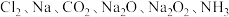 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
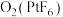 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由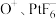 构成 构成 |
您最近一年使用:0次
名校
6 . 有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥氩气,回答下列问题(填序号):
⑥氩气,回答下列问题(填序号):
(1)不存在化学键的是___________
(2)只存在非极性键的是___________
(3)只存在离子键的是___________
(4)既存在离子键又存在极性键的是___________
(5)既存在离子键又存在非极性键的是___________
 ②
② ③
③ ④
④ ⑤
⑤ ⑥氩气,回答下列问题(填序号):
⑥氩气,回答下列问题(填序号):(1)不存在化学键的是
(2)只存在非极性键的是
(3)只存在离子键的是
(4)既存在离子键又存在极性键的是
(5)既存在离子键又存在非极性键的是
您最近一年使用:0次
名校
7 . 已知:氢化锂(LiH)是一种离子化合物,其中锂元素显+1价。在氢化锂中存在的化学键为_______ ;LiH中的两种离子半径大小比较_______ ;写出NaH的电子式_______
您最近一年使用:0次
名校
8 . 利用下列物质的序号填空
①HCl② ③Ne④
③Ne④ ⑤
⑤ ⑥NaOH⑦Ar
⑥NaOH⑦Ar
(1)不存在化学键的是___________ ;
(2)属于共价化合物的是___________ ;
(3)属于离子化合物的是___________ ;
(4)既含离子键,又含共价键的是___________ 。
①HCl②
 ③Ne④
③Ne④ ⑤
⑤ ⑥NaOH⑦Ar
⑥NaOH⑦Ar(1)不存在化学键的是
(2)属于共价化合物的是
(3)属于离子化合物的是
(4)既含离子键,又含共价键的是
您最近一年使用:0次
解题方法
9 . 从宏观和微观两个角度认识元素的单质及其化合物是学好中学化学的重要基础。
(1)组成 的三种元素,其对应的简单离子半径由小到大的顺序为
的三种元素,其对应的简单离子半径由小到大的顺序为___________ 。
(2) 、
、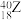 、
、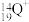 、
、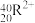 、
、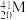 5种微粒,所属元素的种类有
5种微粒,所属元素的种类有___________ 种
(3)下列各组物质中,含有化学键类型都相同的是___________。
(4)将HCl和NaCl分别溶于水。下列说法正确的是___________。
(5)能用于比较Cl与S非金属性强弱的依据是___________。
(1)组成
 的三种元素,其对应的简单离子半径由小到大的顺序为
的三种元素,其对应的简单离子半径由小到大的顺序为(2)
 、
、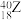 、
、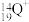 、
、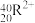 、
、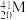 5种微粒,所属元素的种类有
5种微粒,所属元素的种类有(3)下列各组物质中,含有化学键类型都相同的是___________。
| A.HI和NaCl | B.NaF和KOH | C.CO和HCl | D. 和NaBr 和NaBr |
| A.HCl的离子键被破坏 | B.NaCl的共价键被破坏 |
| C.HCl和NaCl的化学键均遭破坏 | D.HCl和NaCl的化学键均未遭破坏 |
| A.熔沸点:硫单质>氯单质 | B.酸性: |
C.热稳定性: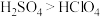 | D.氧化性: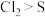 |
您最近一年使用:0次
名校
10 . 卤族元素在性质上具有相似性与递变性。为了验证卤族部分元素递变规律,设计如图装置进行实验。请回答下列问题。
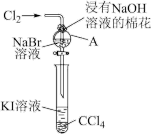
(1)A中发生反应的化学方程式是_______ 。
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为_______ 。
(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱_______ 。
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为_______ 。
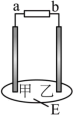
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是
(8)下图是用强光照射广口瓶中新制氯水时传感器所获得数据的图像,下列各项代表纵坐标的物理量,其中与图像不相符的是

(9)下列变化不需要破坏化学键的是

(1)A中发生反应的化学方程式是
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
| A.Cl-、Br-、I-的还原性逐渐增强 | B.Cl2、Br2、I2的熔点逐渐升高 |
| C.HCl、HBr、HI的酸性逐渐减弱 | D.HCl、HBr、HI的稳定性逐渐减弱 |
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应
 填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是

| A.b是阳极,a是阴极 | B.a是正极,b是负极 |
| C.乙是正极,甲是负极 | D.乙是阳极,甲是阴极 |

| A.溶液中氯离子的浓度 | B.溶液的 pH |
| C.瓶中氧气的体积分数 | D.溶液的导电能力 |
| A.液态水变为水蒸气 | B.HCl 气体溶于水 |
| C.NaHCO3 受热分解 | D.NaCl 熔化 |
您最近一年使用:0次



