1 . 按要求回答问题。
(1)1 mol HCHO分子中含有σ键的数目为___________ NA。
(2)CS2分子中,共价键的类型有___________ 。
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是___________ (填序号,下同),只存在非极性键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在极性共价键的是___________ ,既存在离子键又存在非极性共价键的是___________ 。
(4)第一电离能比较Mg___________ Al,解释原因___________ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是
(4)第一电离能比较Mg
您最近一年使用:0次
名校
2 . 下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。
(1)②表示的元素是___________ (填元素符号);
(2)①②⑤三种元素的原子半径从大到小排列为:___________ (填元素符号);
(3)③④两种元素的金属性强弱顺序为:③___________ ④(填“<”或“>”);
(4)③与②两种元素所形成化合物的阴阳离子个数比为___________ ;
(5)④和⑥两种元素组成的化合物中含有的化学键为___________ (填“离子键”或“共价键”)。
族 周期 | ⅠA | 0 | |||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | F | Ne | |||||
| 3 | ③ | Mg | ④ | Si | ⑤ | ⑥ | |||
(1)②表示的元素是
(2)①②⑤三种元素的原子半径从大到小排列为:
(3)③④两种元素的金属性强弱顺序为:③
(4)③与②两种元素所形成化合物的阴阳离子个数比为
(5)④和⑥两种元素组成的化合物中含有的化学键为
您最近一年使用:0次
名校
3 . 表为元素周期表中短周期元素的一部分,表中所列的字母分别代表一种元素。
(1)a、b、c、d、e、f六种元素的原子半径最大的是_______ (填元素符号)。
(2)d、e两种元素的最高价氧化物对应水化物的碱性较强的物质俗称为_______ , 、
、 的沸点较高的是
的沸点较高的是_______ (填化学式)。
(3)过量的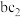 与
与 溶液能发生反应,写出反应的离子方程式:
溶液能发生反应,写出反应的离子方程式:_______ 。
(4)化学式为 的化合物属于
的化合物属于_______ (填“离子化合物”或“共价化合物”),其中含有的化学键的类型为_______ 。
| a | |||||||
| b | c | ||||||
| d | e | f |
(2)d、e两种元素的最高价氧化物对应水化物的碱性较强的物质俗称为
 、
、 的沸点较高的是
的沸点较高的是(3)过量的
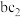 与
与 溶液能发生反应,写出反应的离子方程式:
溶液能发生反应,写出反应的离子方程式:(4)化学式为
 的化合物属于
的化合物属于
您最近一年使用:0次
4 . 在下列化合物中:H2O、Na2O、I2、NaCl、KOH、CO2、NH4Cl、Na2O2,请填空:
(1)含有极性共价键的离子化合物是_______
(2)只含有非极性共价键的是_______
(3)既有离子键又有非极性键的化合物是_______ 。
(1)含有极性共价键的离子化合物是
(2)只含有非极性共价键的是
(3)既有离子键又有非极性键的化合物是
您最近一年使用:0次
5 . X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为________________ 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______________ (写化学式),MY3
中所含化学键的类型是_________
(3)ZX的电子式为__________ ;ZX与水反应放出气体的化学方程式为_________________ 。
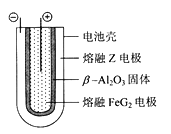
(4)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:2Z + FeG2 Fe + 2ZG
Fe + 2ZG
放电时,电池的正极反应式为__________________________ 。
(1)Y在元素周期表中的位置为
(2)上述元素的最高价氧化物对应的水化物酸性最强的是
中所含化学键的类型是
(3)ZX的电子式为

(4)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:2Z + FeG2
 Fe + 2ZG
Fe + 2ZG 放电时,电池的正极反应式为
您最近一年使用:0次



