名校
解题方法
1 . 如图表示不同类型共价键形成时电子云重叠情况:
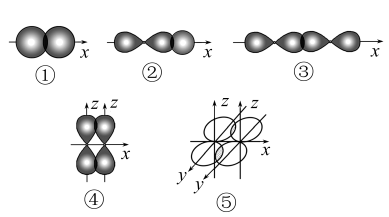
(1)其中形成的化学键属于轴对称的有_______ 。
(2)下列物质中,通过方式①化学键形成的是_______ ;通过方式②化学键形成的是_______ ;只通过方式③化学键形成的是_______ ;同时含有③、④、⑤三种方式化学键的物质是_______ 。
A.Cl2 B.HCl C.N2 D.H2
(3)某有机物分子的结构简式为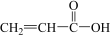 ,该分子中有
,该分子中有_______ 个σ键,有_______ 个π键,有_______ 种极性键,_______ (填“有”或“没有”)非极性键。

(1)其中形成的化学键属于轴对称的有
(2)下列物质中,通过方式①化学键形成的是
A.Cl2 B.HCl C.N2 D.H2
(3)某有机物分子的结构简式为
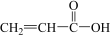 ,该分子中有
,该分子中有
您最近一年使用:0次
2021-12-25更新
|
999次组卷
|
4卷引用:云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题
云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题(已下线)2.1.1 共价键的类型-σ键和π键-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)2.1.1 共价键-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)第一章 有机化合物的结构特点与研究方法(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修3)
名校
2 . 元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
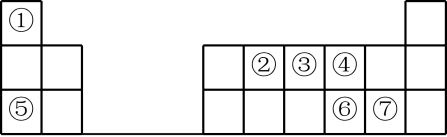
请回答下列问题:
(1)元素①的名称为_______ 。
(2)元素③的最高价氧化物的水化物为_______ (填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是_______ (填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为_______ 。
(5)⑤和⑦两种元素形成的化合物的电子式为_______ 。
(6)⑦的单质与⑤的最高价氧化物对应水化物反应的化学方程式为_______ 。

请回答下列问题:
(1)元素①的名称为
(2)元素③的最高价氧化物的水化物为
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是
(4)②和④两种元素形成的常见气态化合物中化学键类型为
(5)⑤和⑦两种元素形成的化合物的电子式为
(6)⑦的单质与⑤的最高价氧化物对应水化物反应的化学方程式为
您最近一年使用:0次
名校
3 . 氧、硫、硒(Se)、碲(Te)、钋(Po)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)硒(Se)的原子结构示意图为___________ 。
(2)氧和硫的氢化物性质的比较:
①热稳定性:H2O___________ H2S(填“>”或“<”),判断依据是___________ 。
②沸点:H2O___________ H2S(填“>”或“<”),判断依据是___________ 。
(3)H2O与NH3反应产物中所含化学键类型为___________ ;H2S与NH3反应的产物中所含化学键类型为___________ (填离子键或共价键)。
(4)钠的硫化物Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO 被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1∶13,则x的值为___________ 。
(1)硒(Se)的原子结构示意图为
(2)氧和硫的氢化物性质的比较:
①热稳定性:H2O
②沸点:H2O
(3)H2O与NH3反应产物中所含化学键类型为
(4)钠的硫化物Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO 被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1∶13,则x的值为
您最近一年使用:0次
2021-03-05更新
|
354次组卷
|
4卷引用:云南省下关第一中学2022-2023学年高一下学期期中考试化学试题
解题方法
4 . 在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4
(1)只存在非极性键的分子是___ ;既存在非极性键又存在极性键的分子是___ ;只存在极性键的分子是____ 。
(2)只存在单键的分子是___ ,存在叁键的分子是___ ,只存在双键的分子是____ ,既存在单键又存在双键的分子是____ 。
(3)只存在σ键的分子是___ ,既存在σ键又存在π键的分子是____ 。
(4)不存在化学键的是____ 。
(5)既存在离子键又存在极性键的是___ ;既存在离子键又存在非极性键的是___ 。
(1)只存在非极性键的分子是
(2)只存在单键的分子是
(3)只存在σ键的分子是
(4)不存在化学键的是
(5)既存在离子键又存在极性键的是
您最近一年使用:0次
2019-09-25更新
|
179次组卷
|
2卷引用:云南省广南县二中2019-2020学年高二上学期9月份考试化学试题
5 . 现有短周期A、B、C三种元素,原子序数依次增大,A元素的单质是密度最小的气体,B获得2个电子可达到稳定结构,C与A同主族。
(1)判断A、B、C各为何种元素(填名称)。
A________ ,B________ ,C________ 。
(2)用电子式表示三种元素原子之间可能构成的化合物的形成过程,并指出各自化学键的类型:
①A与B:__________________ 。
②A与C:________________ 。
③B与C:______________ 。
④A、B、C_________________ 。
(1)判断A、B、C各为何种元素(填名称)。
A
(2)用电子式表示三种元素原子之间可能构成的化合物的形成过程,并指出各自化学键的类型:
①A与B:
②A与C:
③B与C:
④A、B、C
您最近一年使用:0次
名校
6 . 下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:

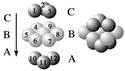
图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________ ,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为__________________________________ 。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________ ,H3BO3晶体中B原子个数与极性键个数比为____________ 。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________ 理论。
(4)三种晶体中熔点最低的是________ (填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为____________________________________________________________ 。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为_______________________________________ 。


图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用
(4)三种晶体中熔点最低的是
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为
您最近一年使用:0次
2018-09-26更新
|
449次组卷
|
16卷引用:云南省玉溪市通海县第二中学2019届高三9月月考化学试题
云南省玉溪市通海县第二中学2019届高三9月月考化学试题云南省西畴县第二中学2020届高三上学期开学考试化学试题云南省文山壮族苗族自治州砚山县第二中学2020届高三上学期开学考试化学试题云南省文山州马关县实验高中2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省宾川县三中2020届高三上学期开学考试化学试题云南省盈江县一中2020届高三上学期开学考试化学试题云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题云南省马关县第二中学2019-2020学年高三上学期期末考试理综化学试题云南省玉溪市新平县一中2019-2020学年高三上学期1月月考理综化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题云南省景东彝族自治县第一中学2021-2022学年高三下学期3月份考试化学试题云南省瑞丽市第一民族中学2021-2022学年高三下学期3月月考化学试题云南省广南县第一中学2021-2022学年高三下学期3月考试理综化学试题贵州省长顺县二中2019-2020学年高三上学期期末考试理综化学试题贵州省黔南布依族苗族自治州贵定县第二中学2019-2020学年高三上学期期末考试化学试题
解题方法
7 . 按要求填空:有下列物质:①O2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr,回答下列问题:
(1)只含有极性键的是________ ;
(2)只含有非极性键的是________ ;
(3)含有极性键和非极性键的是________ ;
(4)只含有离子键的离子化合物是________ ;
(5)含有非极性键的离子化合物是________ 。
(1)只含有极性键的是
(2)只含有非极性键的是
(3)含有极性键和非极性键的是
(4)只含有离子键的离子化合物是
(5)含有非极性键的离子化合物是
您最近一年使用:0次
2018-06-29更新
|
416次组卷
|
7卷引用:云南省曲靖市宣威市第三中学2017-2018学年高一下学期3月月考化学试题
云南省曲靖市宣威市第三中学2017-2018学年高一下学期3月月考化学试题2014-2015河北省正定中学高一下学期第一次月考化学试卷甘肃省武威第五中学2017-2018学年高一下学期第二次月考化学试题2020年人教版高中化学必修2第一章《物质结构 元素周期律》测试卷(已下线)第二单元 化学键与分子间作用力(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)山东省新泰市第二中学2020-2021学年高一下学期期中考试化学试题陕西省咸阳百灵学校2020-2021学年高一下学期第一次月考质量检测化学试题



