名校
解题方法
1 . 2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”元素Mc可由反应: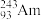 +
+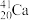 =
=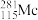 +3
+3 得到。
得到。
(1)该元素的质子数为___________ 。287Mc与288Mc互为________ 。
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:__________ ,该分子内存在的共价键类型有___________ 。
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为_______ ,+5价简单含氧酸的化学式为_________ 。
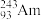 +
+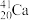 =
=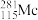 +3
+3 得到。
得到。(1)该元素的质子数为
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为
您最近一年使用:0次
名校
2 . 有下列物质:① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。
(1)上述物质中既含共价键又含离子键的是___________ (选填数字编号,下同);属于共价化合物的是___________ ;属于非极性分子的化合物是___________ 。
(2)④溶于水时破坏___________ ,固体⑦熔化时破坏___________ 。
A.离子键 B.共价键
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。(1)上述物质中既含共价键又含离子键的是
(2)④溶于水时破坏
A.离子键 B.共价键
您最近一年使用:0次
名校
3 . 随原子序数递增,八种短周期元素(用字母 等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
(1)f在周期表中的位置是_______ 。
(2) 、
、 两种元素的原子可构成一种碱性物质,该物质的电子式是
两种元素的原子可构成一种碱性物质,该物质的电子式是_______ 。
(3)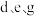 三者简单离子的半径由大到小顺序是(用离子符号表示):
三者简单离子的半径由大到小顺序是(用离子符号表示):_______ 。
(4)写出一个能证明 非金属性强弱的化学方程式:
非金属性强弱的化学方程式:_______ 。
(5)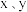 最简单化合物的空间构型为
最简单化合物的空间构型为_______ 。
(6)下列判断不正确的是_______。
 等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。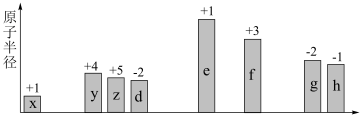
(1)f在周期表中的位置是
(2)
 、
、 两种元素的原子可构成一种碱性物质,该物质的电子式是
两种元素的原子可构成一种碱性物质,该物质的电子式是(3)
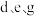 三者简单离子的半径由大到小顺序是(用离子符号表示):
三者简单离子的半径由大到小顺序是(用离子符号表示):(4)写出一个能证明
 非金属性强弱的化学方程式:
非金属性强弱的化学方程式:(5)
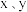 最简单化合物的空间构型为
最简单化合物的空间构型为(6)下列判断不正确的是_______。
A. 和 和 可以形成 可以形成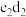 型化合物,正、负离子物质的量之比为 型化合物,正、负离子物质的量之比为 |
B.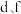 组成的化合物具有两性 组成的化合物具有两性 |
C. 的最高价氧化物对应水化物与 的最高价氧化物对应水化物与 的氢化物反应生成产物中既含有离子键又含有共价键 的氢化物反应生成产物中既含有离子键又含有共价键 |
D. 与 与 同主族,相差两个周期 同主族,相差两个周期 |
您最近一年使用:0次
名校
4 . 下列叙述正确的
A.区别 和葡萄糖的方法是熔融状态下能否导电 和葡萄糖的方法是熔融状态下能否导电 |
B. 中含有共价键,所以 中含有共价键,所以 属于共价化合物 属于共价化合物 |
| C.非金属元素组成的化合物中只含共价键 |
| D.某纯净物在常温常压下为气体,则组成该物质的微粒一定含共价键 |
您最近一年使用:0次
5 . 水是清洁、可持续的氢能来源。利用太阳能从水中获取氢气符合可持续发展的理念。
“太阳能直接热分解水制氢”通过集中阳光产生2000K以上高温,促使H2O分解为H2和O2;若温度进一步升高至5000K,H2与O2会分解为气态原子。
(1)H2O分解过程中断裂的化学键属于
A.离子键 B.极性共价键 C.非极性共价键
(2)在相同条件下,同时存在如下两个过程:
ⅰ.2H(g)+O(g)=H2O(g)
ⅱ.H2(g)+ O2(g)=H2O(g)
O2(g)=H2O(g)
比较下列量的相对大小(均从选项中选择):①放出热量
A.ⅰ>ⅱ B.ⅰ=ⅱ C.ⅰ<ⅱ
您最近一年使用:0次
解题方法
6 . 钠元素在自然界中分布很广,储量极为丰富,都以化合态存在,如氯化钠、碳酸钠、硫酸钠等。钠单质和钠的化合物在生产、生活中被广泛应用。请根据钠及其化合物性质按要求完成各题。
(1)钠原子在周期表中的位置为___________ ,钠离子的结构示意图___________ 。
(2)请选择下列物质中合适的物质,按要求填空:
NaOH、 CaCl2 、 SO2 、H2O 、 NH4Cl
只含有离子键的有___________ (填化学式,下同),既含有离子键又含有共价键的有___________ ,只含共价键的有___________ 。
(3)钠的化学性质活泼,暴露在空气中生成___________ 色Na2O,在空气中加热,生成___________ 色的Na2O2,Na2O2可用作呼吸面具、潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:___________ 。
(4)钠能在冷水中剧烈反应,该反应的实验现象中描述错误的是____。
(5)下列有关物质的性质描述正确的是____。
(6)Na2CO3和NaHCO3是常见的钠盐,且两者之间可以相互转化,请回答下列问题:
①下列有关碳酸钠和碳酸氢钠的说法正确的是____ 。
A.热稳定性:Na2CO3<NaHCO3
B.溶于水后,碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
C.相同条件下,与同种酸反应的剧烈程度:Na2CO3<NaHCO3
D.石碱风化是物理过程
②写出Na2CO3在水溶液中的电离方程式___________ ;
③向Na2CO3溶液中通入CO2可生成NaHCO3,该反应的化学方程式为___________ ;
④加热15.0g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为11.9g,则混合物中碳酸氢钠的质量分数为____ 。
A.42% B.44% C.56% D.58%
(1)钠原子在周期表中的位置为
(2)请选择下列物质中合适的物质,按要求填空:
NaOH、 CaCl2 、 SO2 、H2O 、 NH4Cl
只含有离子键的有
(3)钠的化学性质活泼,暴露在空气中生成
(4)钠能在冷水中剧烈反应,该反应的实验现象中描述错误的是____。
| A.钠熔化成银白色小球 | B.钠在水面上迅速游动 |
| C.发出嘶嘶的声响 | D.溶液逐渐变红色 |
| A.钠与氧气反应时的产物主要取决于氧气的用量及纯度 |
| B.钠投入硫酸铜溶液中有气体和蓝色沉淀产生 |
| C.Na2O和Na2O2分别溶于水中,所得的产物相同 |
| D.FeCl3溶液用于铜质印刷线路制作,原因是两者发生置换反应 |
①下列有关碳酸钠和碳酸氢钠的说法正确的是
A.热稳定性:Na2CO3<NaHCO3
B.溶于水后,碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
C.相同条件下,与同种酸反应的剧烈程度:Na2CO3<NaHCO3
D.石碱风化是物理过程
②写出Na2CO3在水溶液中的电离方程式
③向Na2CO3溶液中通入CO2可生成NaHCO3,该反应的化学方程式为
④加热15.0g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为11.9g,则混合物中碳酸氢钠的质量分数为
A.42% B.44% C.56% D.58%
您最近一年使用:0次
名校
解题方法
7 . 设 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.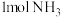 含有的共价键数目为 含有的共价键数目为 |
B.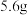 铁粉与 铁粉与 的 的 溶液充分反应,产生的气体分子数目为 溶液充分反应,产生的气体分子数目为 |
C. 和 和 的混合物中含 的混合物中含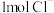 ,则混合物中质子数为 ,则混合物中质子数为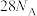 |
| D.两种物质的物质的量相同,则它们在标准状况下的体积相同 |
您最近一年使用:0次
名校
8 . 下列各组物质中,含有化学键类型都相同的是
A.HI和 | B. 和 和 |
C. 和 和 | D. 和 和 |
您最近一年使用:0次
名校
9 . 下列叙述正确的是
| A.醋酸溶液的导电能力可能比稀硫酸强 |
| B.硫磺是单质,不导电,因此硫磺是非电解质 |
| C.SO3溶于水,其水溶液能导电,故SO3是电解质 |
| D.强电解质都是离子化合物,因此NaCl是离子化合物 |
您最近一年使用:0次
名校
解题方法
10 . A、B、C、D、E五种原子序数均小于18的元素,且原子序数依次增大,其中B与C的电子层数相同,D与E的电子层数相同,A与D的最外层电子数相同,C与E的最外层电子数相同,E元素的原子最外层电子数是电子层数的2倍,D与其他具有相同电子层数的原子相比半径最大。又知由B元素组成的单质是空气中的主要成分。
(1)B的元素名称是___________ ,该元素的原子结构示意图为___________ ,用电子式表示B的简单氢化物的形成过程___________ 。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是___________ (用离子符号表示)。
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出2种得满分)___________ 。
(4)以下说法正确的是___________ 。
①B的氧化物均为酸性氧化物;
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键;
③由A、B、C形成的化合物中不可能存在离子键;
④D2E的熔沸点较高,硬度较大。
(1)B的元素名称是
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出2种得满分)
(4)以下说法正确的是
①B的氧化物均为酸性氧化物;
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键;
③由A、B、C形成的化合物中不可能存在离子键;
④D2E的熔沸点较高,硬度较大。
您最近一年使用:0次



