解题方法
1 . a、b、c、d为短周期主族元素,a的M层上有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d属于同周期元素,且d的原子半径小于c的原子半径。下列叙述错误的是
| A.四种元素中,元素d的非金属性最强 |
| B.元素a、b、c均能与氧元素形成两种或两种以上的化合物 |
| C.元素a分别与b、d元素形成的化合物均是离子化合物 |
| D.元素c、d分别与氢元素形成的最简单氢化物中的化学键均为非极性共价键 |
您最近一年使用:0次
名校
解题方法
2 . 下列关于晶体的说法不正确的是
①含有离子的晶体一定是离子晶体
②分子晶体若采取面心密堆积方式,其配位数是12
③含有共价键的晶体一定是共价晶体
④分子晶体的熔点一定比金属晶体的低
⑤MgO远比NaCl的熔点高
⑥共价键的强弱决定分子晶体熔、沸点的高低
①含有离子的晶体一定是离子晶体
②分子晶体若采取面心密堆积方式,其配位数是12
③含有共价键的晶体一定是共价晶体
④分子晶体的熔点一定比金属晶体的低
⑤MgO远比NaCl的熔点高
⑥共价键的强弱决定分子晶体熔、沸点的高低
| A.①③④⑥ | B.①②③⑤ | C.①②④ | D.②③④⑥ |
您最近一年使用:0次
名校
解题方法
3 . 下列叙述正确的是
| A.以极性键结合的分子,一定是极性分子 |
| B.由非金属元素组成的化合物不一定是共价化合物 |
| C.非极性分子中,各原子间都应以非极性键结合 |
| D.不同元素组成的多原子分子里的化学键一定都是极性键 |
您最近一年使用:0次
名校
解题方法
4 . 下列叙述错误的是
| A.分子晶体中不一定存在共价键 |
| B.离子晶体中一定含金属元素 |
| C.碘和干冰升华所克服的微粒间的作用相同 |
| D.现代科技已经实现了石墨制取金刚石,该过程属于化学变化 |
您最近一年使用:0次
名校
解题方法
5 . 下列各种说法错误的是
| A.KAl(SO4)2·12H2O不属于配合物 |
| B.NH4NO3中既有离子键又有共价键和配位键 |
| C.配位化合物中的配体可以是分子也可以是阴离子 |
| D.共价键的形成条件是成键原子必须有未成对电子 |
您最近一年使用:0次
解题方法
6 . X、Y、Z、W、R为五种短周期主族元素,原子序数依次增大。X原子半径最小,Y、Z处于同一周期,Y与X形成的简单化合物键角约为107°,基态Z原子有两个未成对电子。W是地壳中含量最高的金属元素,R的最高价氧化物对应的水化物是酸性最强的无机含氧酸。下列说法正确的是
| A.简单离子半径大小:R>W>Y>Z>X |
| B.基态原子第一电离能:Y>Z |
C.实验室可电解熔融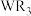 获得W的单质 获得W的单质 |
| D.X、Y、Z形成的化合物既含有离子键又含有共价键 |
您最近一年使用:0次
解题方法
7 . 利用含锰催化剂催化 脱硝的一种反应机理如图所示。下列说法正确的是
脱硝的一种反应机理如图所示。下列说法正确的是
 脱硝的一种反应机理如图所示。下列说法正确的是
脱硝的一种反应机理如图所示。下列说法正确的是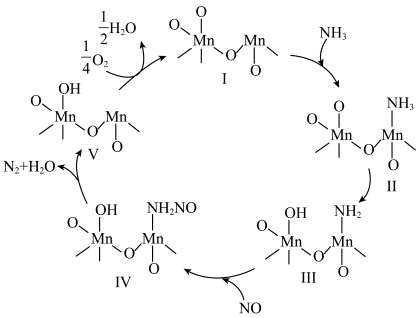
| A.II是催化剂 |
B.该过程发生的总反应为 |
| C.全程只涉及极性键、非极性键的断裂和极性键的生成 |
D.若将 替换为 替换为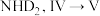 反应生成的水可能为 反应生成的水可能为 |
您最近一年使用:0次
解题方法
8 . 下列物质中只含有离子键的是
| A.CS2 | B.Na2O2 | C.CaO | D.CH4 |
您最近一年使用:0次
9 . 元素周期表是学习化学的重要工具。已知A、B、C、D、E均为短周期元素,原子半径依次增大,下列叙述正确的是
具体数值及主要化合价如下表:
具体数值及主要化合价如下表:
| 元素代号 | A | B | C | D | E |
| 原子半径/pm | 74 | 75 | 102 | 143 | 186 |
| 主要化合价 | -2 | -3、+5 | -2、+6 | +3 | +1 |
| A.简单氢化物的沸点:A>B>C | B.简单离子半径:A<C<D |
| C.C、D两种元素形成的常见化合物是共价化合物 | D.元素的金属性:D>E |
您最近一年使用:0次
10 . W、X、Y、Z、Q是核电荷数依次增大的五种短周期元素。W+的半径在所有离子中最小,X、Y、Z同周期且相邻,Z、Q位于同一主族且Z的核电荷数是Q的一半。下列说法正确的是
| A.X、Q的最高价氧化物对应水化物的酸性:Q<X |
| B.W、X、Y、Z四种元素不能形成离子化合物 |
| C.Z、Q元素的最高正价相同 |
| D.X、Y、Z分别与W形成的最简单化合物的沸点:Z>Y>X |
您最近一年使用:0次



