名校
解题方法
1 . 下列说法正确的是
| A.道尔顿、汤姆孙、卢瑟福和门捷列夫对原子结构模型的建立作出了卓越的贡献 |
| B.3f能级中最多可容纳14个电子 |
C.硫的基态原子的轨道表示式为 它违背了洪特规则 它违背了洪特规则 |
| D.s轨道的电子云形状为圆形的面,若2s的电子云半径比1s电子云半径大说明2s能级的电子比1s的多 |
您最近一年使用:0次
2 . 下列有关原子结构与性质的叙述中,错误的是
| A.原子轨道和电子云可用来形象地描述电子的运动状态 |
| B.电子从激发态跃迁到基态时能产生发射光谱 |
C. 、 、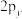 、 、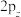 轨道相互垂直、能量不相等 轨道相互垂直、能量不相等 |
D.电子排布式 违反了洪特规则 违反了洪特规则 |
您最近一年使用:0次
名校
3 . 下列说法中正确的是
| A.测量接近沸点的水蒸气的相对分子质量大于18,是因为形成了“缔合分子” |
B.某原子核外电子由 ,原子放出能量 ,原子放出能量 |
| C.p-pσ键与s-pσ键的电子云对称性不同 |
D. 易溶于水只是因为相似相溶原理 易溶于水只是因为相似相溶原理 |
您最近一年使用:0次
4 . 下列有关化学用语的表述正确的是
A.基态 原子的价层电子排布式为 原子的价层电子排布式为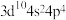 |
B.轨道表示式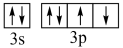 ,不满足泡利原理 ,不满足泡利原理 |
C.基态 原子的电子在 原子的电子在 轨道中的表示式为 轨道中的表示式为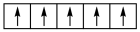 |
D.基态铍原子最外层电子的电子云轮廓图为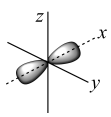 |
您最近一年使用:0次
2024-02-04更新
|
228次组卷
|
3卷引用:陕西省咸阳市2023-2024学年高二上学期期末考试化学试题
5 . 下列物质的结构或性质及其解释均正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 极性: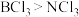 | B元素和Cl元素的电负性差值大于N元素和Cl元素的电负性差值 |
| B | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醇分子间范德华力更强 |
| C |  在水中的溶解度比在 在水中的溶解度比在 中的溶解度更大 中的溶解度更大 |  是弱极性分子 是弱极性分子 |
| D | 电子云半径3s>1s | 3s电子能量高,在离核更远的区域出现的概率大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 按要求回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是___ ,占据该能层电子的电子云轮廓图形状____ 。
(2)Fe成为阳离子时首先失去_______ 轨道电子,写出Fe2+简化核外电子排布_______ 。
(3)P位于元素周期表中第三周期_______ 族,基态P原子核外未成对电子有_______ 个。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)Fe成为阳离子时首先失去
(3)P位于元素周期表中第三周期
您最近一年使用:0次
2024-04-24更新
|
48次组卷
|
2卷引用:陕西省兴平市南郊高级中学2023-2024学年高二上学期第三次化学质量检测题
解题方法
7 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)写出BA3的电子式:_________ 。
(2)B元素基态原子中能量最高的电子,其电子云在空间有_____ 个取向,原子轨道呈___ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____ 。
(4)比较B和D的电负性_________ >_________ (填元素符号)。
(5)G的价电子轨道排布式为_________ 。
(6)H位于_________ 族,__________ 区,该元素的核外电子排布式为__________ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下:I1=738kJ/mol、I2=1451kJ/mol、I3=7733kJ/mol、I4=10540kJ/mol |
| D原子价电子层的p轨道半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G是所在周期中未成对电子最多的元素 |
| H在周期表的第七列 |
(1)写出BA3的电子式:
(2)B元素基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)比较B和D的电负性
(5)G的价电子轨道排布式为
(6)H位于
您最近一年使用:0次
8 . 下列有关原子轨道图的说法,错误的是

| A.s电子的原子轨道是球形的 |
B.能量大小: |
C.p能级有3个原子轨道,相互垂直,分别以 、 、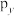 、 、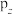 表示 表示 |
D.2 、2 、2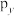 、2 、2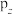 轨道的能量不相同 轨道的能量不相同 |
您最近一年使用:0次
2024-03-20更新
|
201次组卷
|
5卷引用:陕西省汉中市多校联考2023-2024学年高二下学期期中考试化学试卷
9 . 硫铁矿(主要成分FeS2)是接触法制硫酸的主要原料,请回答:
(1)基态下Fe2+共有_____ 种不同空间运动状态的电子。
(2)Fe2+形成的配合物亚铁氰化钾K4[Fe(CN)6]又称黄血盐,可用于检验Fe3+,与CN-互为等电子体的阴离子为_________ (任写一种);含有120molσ键的K4[Fe(CN)6]的物质的量为_____ mol。
(3)H 2SO4的酸性强于H2SO3酸性的原因是_______ 。
(4)FeS2晶体的晶胞结构如图所示。在晶胞中,Fe2+位于 所形成的
所形成的______ (填“正四面体”或“正八面体”)空隙;若晶胞参数为 a nm,密度为ρg∙cm−3,阿伏加德罗常数的值为NA ,则FeS2的摩尔质量 M=_______ (用含 a、ρ、 NA的代数式表示)。

(1)基态下Fe2+共有
(2)Fe2+形成的配合物亚铁氰化钾K4[Fe(CN)6]又称黄血盐,可用于检验Fe3+,与CN-互为等电子体的阴离子为
(3)H 2SO4的酸性强于H2SO3酸性的原因是
(4)FeS2晶体的晶胞结构如图所示。在晶胞中,Fe2+位于
 所形成的
所形成的
您最近一年使用:0次
名校
解题方法
10 . 下列有关叙述中正确的是
| A.原子轨道和电子云都是用来描述核外电子的空间运动状态 |
| B.各电子层的能级都是从s能级开始到f能级结束 |
C.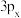 、 、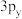 、 、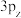 的差异之处在于三者中电子(基态)的能量不同 的差异之处在于三者中电子(基态)的能量不同 |
| D.电子云图上的每一个点都代表一个电子 |
您最近一年使用:0次
2023-12-25更新
|
251次组卷
|
4卷引用:陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题
陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题河北省衡水市枣强中学2023-2024学年高二下学期第一次调研考试化学试题(已下线)名校期中好题汇编-原子结构与性质(选择题)名校期中好题汇编-原子结构与性质(选择题)



