解题方法
1 . SeO2是一种常见的氧化剂,易被还原成 。根据X射线衍射分析,SeO2晶体是如下图所示的长链状结构:
。根据X射线衍射分析,SeO2晶体是如下图所示的长链状结构:
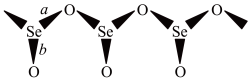
完成下列填空:
(1) 与S同属于VIA族,该族元素原子最外层电子的轨道表示式为
与S同属于VIA族,该族元素原子最外层电子的轨道表示式为_______ ,原子核外占据最高能级的电子云形状为_______ 形。
(2) SeO2在315℃时升华,蒸气中存在二聚态的SeO2,红外研究表明,二聚态的SeO2结构中存在四元环,写出该二聚态的结构式_______ 。
(3) SeO2属于_______ 晶体,其熔点远高于 的理由是
的理由是_______ 。解释键能 的原因
的原因_______ 。
(4) SeO2可将 的水溶液氧化成
的水溶液氧化成 ,反应的化学方程式为
,反应的化学方程式为_______ 。常温下,在稀溶液中硫酸的电离方式为: ;
; 。则在相同浓度
。则在相同浓度 与
与 的稀溶液中,
的稀溶液中, 的电离程度较大的是
的电离程度较大的是_______ ,两种溶液中 电离程度不同的原因是
电离程度不同的原因是_______ 。
 。根据X射线衍射分析,SeO2晶体是如下图所示的长链状结构:
。根据X射线衍射分析,SeO2晶体是如下图所示的长链状结构:
键长 | |
| a | 178 |
| b | 160.7 |
(1)
 与S同属于VIA族,该族元素原子最外层电子的轨道表示式为
与S同属于VIA族,该族元素原子最外层电子的轨道表示式为(2) SeO2在315℃时升华,蒸气中存在二聚态的SeO2,红外研究表明,二聚态的SeO2结构中存在四元环,写出该二聚态的结构式
(3) SeO2属于
 的理由是
的理由是 的原因
的原因(4) SeO2可将
 的水溶液氧化成
的水溶液氧化成 ,反应的化学方程式为
,反应的化学方程式为 ;
; 。则在相同浓度
。则在相同浓度 与
与 的稀溶液中,
的稀溶液中, 的电离程度较大的是
的电离程度较大的是 电离程度不同的原因是
电离程度不同的原因是
您最近一年使用:0次
解题方法
2 . A、B、C、D、E、F是前四周期的六种元素,原子序数依次增大。A、B、D三种元素分别位于不同短周期的不同主族。C、D对应的简单离子核外电子排布相同,A、B、C、D元素可形成一种新型漂白剂(结构如图),E元素正三价阳离子的3d轨道为半充满状态,F元素最外层只有一个电子,焰色反应为蓝绿色。

回答下列问题:
(1)基态A原子电子占据最高能级的电子云轮廓图为___________ 形。D元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。基态原子与F同周期且最外层电子数相等的元素还有___________ (填元素符号)。E元素位于元素周期表___________ 区。
(2)B元素名称是___________ 。新型漂白剂中C元素的化合价为___________ 。C元素能形成两种常见单质,其中沸点高的是___________ (填分子式),原因是___________ 。
(3)元素E与F的第二电离能 I2(F)>I2(E)的原因是___________ 。
(4)E的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是___________ (填字母序号) 。
。
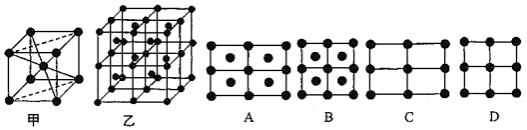

回答下列问题:
(1)基态A原子电子占据最高能级的电子云轮廓图为
(2)B元素名称是
(3)元素E与F的第二电离能 I2(F)>I2(E)的原因是
(4)E的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是
 。
。
您最近一年使用:0次
解题方法
3 . 碱金属及其化合物在生活、科研等领域用途广泛。回答下面相关问题:
(1)基态K原子核外有_______ 种不同的电子运动状态;下列碱金属原子核外电子发生如下变化时有可能会观察到焰色的是_______ (填字母代号)。
a.[Ar]4s1→[Ar]4p1
b.[Ne]3d1→[Ne]3s1
c.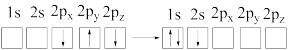
d.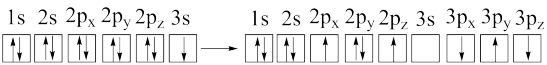
(2)碱金属易形成各种不同的盐,已知碱金属各种盐的沸点(℃)如表所示。
由此可以得出随质子数递增,碱金属形成化合物中化学键的离子性_______ (填“逐渐增强”“不变”或“逐渐减弱”);在硫酸盐和碳酸盐中,S,C原子的杂化形式分别为_______ 和_______ 。
(3)碱金属元素中,仅有Li可以直接与N2化合生成Li3N。已知该晶体中。存在锂、氮原子共同组成的锂、氮层,如图所示。

该结构中,在锂、氮层之间还应存在_______ (填“锂”或“氮”)层。理由是_______ 。
(4)氮化钼是制备锂离子电池的重要原材料,该晶胞结构如图所示。
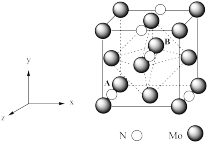
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若A的原子分数坐标为(0,0,0),则B的原子分数坐标为_______ 。
②N原子位于Mo原子立方晶格的_______ (填“四面体”“正方体”或“八面体”)空隙中,若Li位于该晶胞的八面体空隙中,则一个晶胞中最多能够填入_______ 个Li。
③若氮化钼的密度为 g·cm-3,晶胞中Mo为最紧密堆积。其原子半径为r。则Mo所围成的空隙中,所容纳的离子半径最大值为
g·cm-3,晶胞中Mo为最紧密堆积。其原子半径为r。则Mo所围成的空隙中,所容纳的离子半径最大值为_______ nm。(用含有 ,NA的代数式表示。设NA表示阿伏加德罗常数的值)
,NA的代数式表示。设NA表示阿伏加德罗常数的值)
(1)基态K原子核外有
a.[Ar]4s1→[Ar]4p1
b.[Ne]3d1→[Ne]3s1
c.

d.
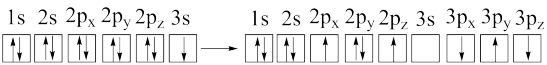
(2)碱金属易形成各种不同的盐,已知碱金属各种盐的沸点(℃)如表所示。
| Li | Na | K | |
| 氧化物 | 613 | 801 | 771 |
| 硫酸盐 | 859 | 880 | 1069 |
| 碳酸盐 | 720 | 858 | 901 |
由此可以得出随质子数递增,碱金属形成化合物中化学键的离子性
(3)碱金属元素中,仅有Li可以直接与N2化合生成Li3N。已知该晶体中。存在锂、氮原子共同组成的锂、氮层,如图所示。

该结构中,在锂、氮层之间还应存在
(4)氮化钼是制备锂离子电池的重要原材料,该晶胞结构如图所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若A的原子分数坐标为(0,0,0),则B的原子分数坐标为
②N原子位于Mo原子立方晶格的
③若氮化钼的密度为
 g·cm-3,晶胞中Mo为最紧密堆积。其原子半径为r。则Mo所围成的空隙中,所容纳的离子半径最大值为
g·cm-3,晶胞中Mo为最紧密堆积。其原子半径为r。则Mo所围成的空隙中,所容纳的离子半径最大值为 ,NA的代数式表示。设NA表示阿伏加德罗常数的值)
,NA的代数式表示。设NA表示阿伏加德罗常数的值)
您最近一年使用:0次



