解题方法
1 . 硫及其化合物有许多用途。相关物质的物理常数如表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______ ,基态S原子电子占据最高能级的电子云轮廓图为______ 形。
(2)根据价层电子对互斥理论,H2S,SO2,SO3的气态分子中,中心原子价层电子对数不同于其他分子的是______ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为____ 。
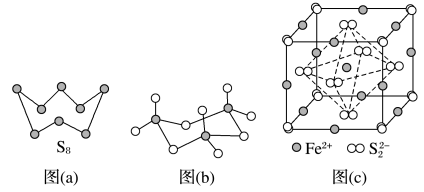
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为______ 形,其中共价键的类型有______ 种;固体三氧化硫中存在如图(b)所示的三聚分子。该分子中S原子的杂化轨道类型为______ 。
(5)FeS2晶体的晶胞如图(c)所示,该晶胞中FeS2个数___________ ,晶胞边长为anm,FeS2相对式量为M、阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为_____ g/cm3.(写出表达式) ;晶胞中Fe2+位于S22-所形成的八面体的体心,该正八面体的边长为______ nm。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S,SO2,SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图(c)所示,该晶胞中FeS2个数
您最近一年使用:0次
解题方法
2 . 下列描述中正确的是( )
| A.CS2 为空间构型为V形的极性分子 |
| B.双原子或多原子形成的气体单质中,一定有σ键,可能有π键 |
| C.氢原子电子云的一个小黑点表示一个电子 |
| D.HCN、SiF4 的中心原子均为sp3杂化 |
您最近一年使用:0次
名校
解题方法
3 . 下列描述中正确的是
| A.CS2 为空间构型为 V 形的极性分子 |
| B.双原子或多原子形成的气体单质中,一定有σ键,可能有π键 |
| C.氢原子电子云的一个小黑点表示一个电子 |
| D.HCN、SiF4 和 SO32- 的中心原子均为 sp3 杂化 |
您最近一年使用:0次
2018-01-18更新
|
407次组卷
|
8卷引用:【全国百强校】内蒙古北方重工业集团有限公司第三中学2017-2018学年高二下学期期末考试化学试题
【全国百强校】内蒙古北方重工业集团有限公司第三中学2017-2018学年高二下学期期末考试化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校2017-2018学年高二上学期期末考试化学试题【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期开学考试化学试题【全国百强校】福建省厦门第一中学2018-2019学年高二上学期期中考试化学试题安徽省淮北师范大学附属实验中学2018-2019学年高二下学期第二次月考化学试题辽宁省六校协作体2019-2020高二下学期期初考试化学试卷辽宁省大连市普兰店市第三十八中学2021届高三第一学期开学考试化学试题(已下线)第二单元 化学键与分子间作用力(能力提升卷)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)



