名校
解题方法
1 . 下列说法中,正确的是

| A.1s电子云轮廓图呈球形,处在该轨道上的电子只能在球壳内运动 |
| B.电子云轮廓图中的小黑点密度大,说明该原子核外空间电子数目多 |
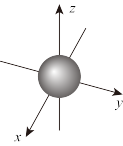
| C.ns能级的原子轨道的电子云轮廓图如图所示 |
| D.3d6表示3d能级有6个原子轨道 |
您最近一年使用:0次
2022-04-04更新
|
251次组卷
|
2卷引用:福建省福州第一中学2021-2022学年高二上学期期末考试化学试题
2 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
(2)基态V原子中具有_______ 种不同能量的电子,具有_______ 种不同空间运动状态的电子,具有_______ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为_______ ,基态Se原子的价电子轨道表示式为_______ ,基态Mn2+的价电子排布式为_______ 。
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为_______ kJ·mol-1,O=O键键能为_______ kJ·mol-1。
(1)下列有关说法错误的是_______。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为
您最近一年使用:0次
2022-04-04更新
|
568次组卷
|
3卷引用:湖南省湖南师范大学附属中学2021-2022学年高二上学期期末考试化学试题
湖南省湖南师范大学附属中学2021-2022学年高二上学期期末考试化学试题四川省成都市武侯高级中学2021-2022学年高二下学期期中考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
名校
解题方法
3 . 下列说法正确的是
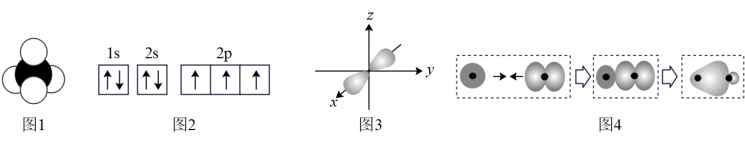

| A.图1为CH4分子的球棍模型 |
| B.图2为基态氮原子的电子排布图 |
| C.图3为铍原子最外层的电子云图 |
| D.图4为用原子轨道描述氢气分子中化学键的形成 |
您最近一年使用:0次
2022-04-03更新
|
350次组卷
|
2卷引用:重庆市第八中学2021-2022学年高二上学期期末考试化学试题
4 . 下列说法中正确的是
| A.电子云示意图中的每个小黑点都表示一个电子 |
| B.钠原子由1s22s22p63s1→1s22s22p63p1时,释放能量,由基态转化成激发态 |
| C.第四周期最外层电子数为1,且内层电子全部排满的原子是钾原子 |
| D.C2H4分子中的碳原子为sp2杂化,其中C=C键是由两个碳原子的sp2杂化轨道形成一个σ键和未参与杂化的p轨道形成一个π键构成的 |
您最近一年使用:0次
名校
解题方法
5 . 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)某元素原子基态核外电子有14种不同的运动状态,该元素位于第____ 周期第____ 族,属于____ 区,占据最高能级的电子云轮廓图为____ 形。
(2)1~36号元素中基态原子核外电子排布中未成对电子数最多的元素的核外电子排布式是____ ,其价电子轨道表示式为____ 。
(3)价电子排布式为3d54s2的原子,其原子结构示意图为____ ,其最高正价为____ 价。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为____ ,C原子的杂化方式为____ 。
(1)某元素原子基态核外电子有14种不同的运动状态,该元素位于第
(2)1~36号元素中基态原子核外电子排布中未成对电子数最多的元素的核外电子排布式是
(3)价电子排布式为3d54s2的原子,其原子结构示意图为
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
您最近一年使用:0次
名校
6 . 下列说法正确的是
| A.已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,该元素属于ds区 |
| B.最外层电子数为ns2的元素都在元素周期表第2列 |
C.2p 表示2px能级有两个轨道 表示2px能级有两个轨道 |
| D.氢原子的电子云图中小黑点的疏密表示电子在核外单位体积内出现机会的多少 |
您最近一年使用:0次
名校
解题方法
7 . 下列表达式正确的是
A.sp2杂化轨道模型: |
B.碳原子的L层电子轨道表示式: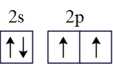 |
| C.基态溴原子的价电子排布式是3d104s24p5 |
D. H原子的电子云图,由图可见H原子核外靠近核运动的电子多 H原子的电子云图,由图可见H原子核外靠近核运动的电子多 |
您最近一年使用:0次
2022-03-15更新
|
248次组卷
|
4卷引用:福建省龙岩第一中学2021-2022学年高二(实验班)下学期第一次月考化学试题
名校
8 . 下列说法正确的是
| A.键长:N-N<C-C<Si-Si |
| B.p电子云是平面“8”字形的 |
| C.L能层包含2s、2p、2d三个能级 |
| D.2p能级有一个未成对电子的基态原子的电子排布式一定为1s22s22p5 |
您最近一年使用:0次
名校
9 . 人们常用HX表示卤化氢(x代表F、Cl、Br、I),下列说法中,正确的是
| A.HX中共价键的电子云是轴对称的 | B.H-F形成的是p-pσ键 |
| C.H-F的键长是H-X中最长的 | D.H-F的键能是H-X中最小的 |
您最近一年使用:0次
2022-03-15更新
|
654次组卷
|
3卷引用:陕西省宝鸡市渭滨区2021-2022学年高二下学期期末考试化学试题
解题方法
10 . 下列说法正确的是
| A.M能层有3s、3p、3d三个原子轨道 |
| B.同一原子中,2p、3p、4p能级的原子轨道数依次增多 |
| C.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| D.在氢原子基态电子的概率分布图中,小黑点的疏密程度表示电子在该单位体积内出现概率的大小 |
您最近一年使用:0次



