解题方法
1 . 下列基态原子或离子的电子排布式(图)正确的是______ (填序号,下同),违反能量最低原理的是______ ,违反洪特规则的是______ ,违反泡利原理的是______ .
① :
:
② :
:
③P: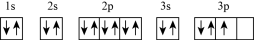
④Cr:
⑤Fe:
⑥ :
:
⑦O: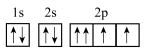
①
 :
:
②
 :
:
③P:

④Cr:

⑤Fe:

⑥
 :
:
⑦O:

您最近一年使用:0次
2 . 根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式___________________________________ ,写出基态24Cr原子的价电子排布式________________________ ;
(2)写出基态N的原子核外电子排布图:__________________ ;
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了_______________________ ;
(4)Fe3+比Fe2+的稳定性更________ (填“强”或“弱”),从结构上分析原因是____________________________________________________________________________ 。
(1)写出基态S原子的核外电子排布式
(2)写出基态N的原子核外电子排布图:
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了
(4)Fe3+比Fe2+的稳定性更
您最近一年使用:0次
2018-09-26更新
|
844次组卷
|
5卷引用:【全国百强校】四川省绵阳市南山中学2018-2019学年高二9月月考化学试题
3 . 推导下列元素,回答有关问题:
(1)具有1个4p电子的元素为________ (写元素名称,下同),简化电子排布式为________ 。
(2)N层只有1个电子的主族元素是________ ,其氯化物的焰色反应呈________ 色,其原子核外有________ 种不同运动状态的电子。
(3)3d能级全充满,4s能级只有1个电子的元素为________ ,原子序数为________ 。
(4)离子M2+的3d轨道中有5个电子,则M原子的最外层电子数和未成对电子数分别为_____ 和___ 。
(5)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是____ ,X在参与化学反应时,1个原子失去的电子数为_____ 。
(1)具有1个4p电子的元素为
(2)N层只有1个电子的主族元素是
(3)3d能级全充满,4s能级只有1个电子的元素为
(4)离子M2+的3d轨道中有5个电子,则M原子的最外层电子数和未成对电子数分别为
(5)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是
您最近一年使用:0次
4 . 下列原子或离子的电子排布式或排布图正确的是________ (填序号,下同),违反能量最低原理的是____________ ,违反洪特规则的是________ ,违反泡利原理的是________ 。
①Ca2+:1s22s22p63s23p6 ②F-:1s22s23p6
③P: ④Cr:1s22s22p63s23p63d44s2
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2 ⑥Mg2+:1s22s22p6⑦C: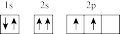
①Ca2+:1s22s22p63s23p6 ②F-:1s22s23p6
③P:
 ④Cr:1s22s22p63s23p63d44s2
④Cr:1s22s22p63s23p63d44s2⑤Fe:1s22s22p63s23p63d64s2 ⑥Mg2+:1s22s22p6⑦C:
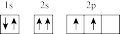
您最近一年使用:0次
2018-02-11更新
|
514次组卷
|
3卷引用:宁夏吴忠市2017-2018学年高二人教版选修3化学同步练习:第1章 原子结构与性质综合练习1
5 . 中国营养学会修订颁布的“每日膳食营养素供给量”将硒(Se)列为15种每日膳食营养素之一,提出一个成年人每天对硒的适宜摄入量是50 ~250μg。回答下列有关问题:
(1) Se 原子的价电子排布式为_______ ,基态78 Se 原子中,核外存在______ 对自旋方向相反的电子。
(2)碱金属的硒化物溶液能够溶解硒,生成多硒化合物(M2Sex)。如多硒化钠Na2Se8,该物质中,化学键类型是________ ,Se原子之间形成的空间构型为_________________ 。
(3)As、S在元素周期表中均与Se 相邻,其氢化物分别是AsH3、H2Se和H2S其氢化物的稳定性强弱顺序为______________________ 。
(4)SeCl2和BeCl2均为1:2组成的分子,SeCl2中Se的轨道杂化类型是_______ ,BeCl2中Be的轨道杂化类型是_________________ 。
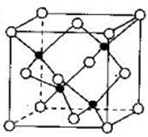
(5)Zn与Se同周期,S与Se同主族。由Zn与S形成的ZnS可用于制白色的颜料及玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS晶胞结构如图所示,黑球代表的原子在晶胞内,白球代表的原子除在顶点外,其余的原子在晶胞_________ (填“内部”“棱上”或“面心”),若该晶体的密度为ρg·㎝-3,阿伏伽德罗常数为NA mol-1,则立方晶胞的棱长=_____ ㎝(用含p、NA的代数式表示)。
(1) Se 原子的价电子排布式为
(2)碱金属的硒化物溶液能够溶解硒,生成多硒化合物(M2Sex)。如多硒化钠Na2Se8,该物质中,化学键类型是
(3)As、S在元素周期表中均与Se 相邻,其氢化物分别是AsH3、H2Se和H2S其氢化物的稳定性强弱顺序为
(4)SeCl2和BeCl2均为1:2组成的分子,SeCl2中Se的轨道杂化类型是
(5)Zn与Se同周期,S与Se同主族。由Zn与S形成的ZnS可用于制白色的颜料及玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS晶胞结构如图所示,黑球代表的原子在晶胞内,白球代表的原子除在顶点外,其余的原子在晶胞
您最近一年使用:0次
11-12高二上·湖北宜昌·期末
6 . 在原子结构理论中,有四个原理,分别是①构造原理,②泡利原理,③洪特规则,④能量最低原理。在以下的现象中主要决定的因素是(填序号,各只填一项)
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍_____________ ;
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3___________ ;
(3)最外层电子数不会超过8个,次外层电子数不会超过18个_____________ ;
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2________ ;
(5)磷原子的基态原子结构中,有3个未成对的单电子____________ 。
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3
(3)最外层电子数不会超过8个,次外层电子数不会超过18个
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2
(5)磷原子的基态原子结构中,有3个未成对的单电子
您最近一年使用:0次



